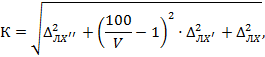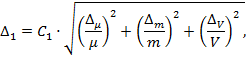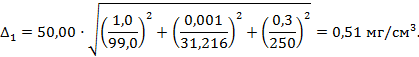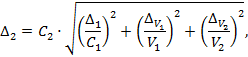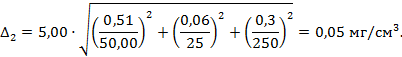|
МИНИСТЕРСТВО
ПРИРОДНЫХ РЕСУРСОВ И ЭКОЛОГИИ Федеральная
служба по гидрометеорологии и мониторингу окружающей среды |
|
|
РУКОВОДЯЩИЙ ДОКУМЕНТ |
РД 52.24.403-2018 |
МАССОВАЯ КОНЦЕНТРАЦИЯ ИОНОВ КАЛЬЦИЯ В ВОДАХ
Методика измерений титриметрическим методом с трилоном Б
Ростов-на-Дону
2018
Предисловие
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением «Гидрохимический институт» (ФГБУ «ГХИ»)
2 РАЗРАБОТЧИКИ Ю.А. Андреев, канд. хим. наук (ответственный исполнитель), Т.С. Евдокимова
3 СОГЛАСОВАН с Федеральным государственным бюджетным учреждением «Научно-производственное объединение «Тайфун» (ФГБУ «НПО «Тайфун») 26.12.2017 и Управлением мониторинга загрязнения окружающей среды, полярных и морских работ (УМЗА) Росгидромета 09.01.2018
4 УТВЕРЖДЕН Руководителем Росгидромета 10.01.2018
ВВЕДЁН В ДЕЙСТВИЕ приказом Росгидромета от 14.02.2018 № 61
5 МЕТОДИКА ИЗМЕРЕНИЙ АТТЕСТОВАНА ФГБУ «ГХИ»
Свидетельство об аттестации № 403.RA.RU.311345-2017 от 28.08.2017
6 ЗАРЕГИСТРИРОВАН ФГБУ «НПО «Тайфун» от 26.01.2018 за номером РД 52.24.403-2018
7 ВЗАМЕН РД 52.24.403-2007 «Массовая концентрация кальция в водах. Методика выполнения измерений титриметрическим методом с трилоном Б»
8 СРОК ПЕРВОЙ ПРОВЕРКИ 2028 год
ПЕРИОДИЧНОСТЬ ПРОВЕРКИ 10 лет
СОДЕРЖАНИЕ
Введение
Кальций является одним из самых распространенных элементов земной коры. В связи с высокой химической активностью в природе кальций встречается только в виде соединений. Карбонат кальция СаСО3 - одно из самых распространенных на земле соединений. Он встречается в виде многих минералов - кальцита, мела, мрамора, известняка, доломита и др.
Основными источниками поступления кальция в природные воды являются процессы химического выветривания и растворения содержащих кальций минералов, прежде всего известняков, доломитов, гипса и других осадочных и метаморфических пород. Растворению способствуют микробиальные процессы разложения органических веществ, сопровождающиеся понижением pH. Большие количества кальция выносятся со сточными водами силикатной, металлургической, стекольной, химической промышленности и стоками с сельскохозяйственных угодий, особенно при использовании кальцийсодержащих минеральных удобрений.
В естественных условиях изменение концентрации растворенного кальция обусловлено главным образом равновесием углекислых солей и двуокиси углерода. В минерализованных водах, содержащих значительное количество сульфатов, концентрация растворенного кальция понижается за счет образования малорастворимого CaSО4.
В водных объектах кальций в заметных количествах может выпадать в осадок в виде СаСО3 при испарении воды, а также в условиях активизации фотосинтеза, сопровождающегося повышением pH воды. Характерной особенностью кальция является его склонность образовывать в поверхностных водах довольно устойчивые пересыщенные растворы СаСО3. Ионная форма кальция характерна только для маломинерализованных вод. При увеличении минерализации ионы кальция образуют нейтральные (CaSО4 и СаСО3) или заряженные (СаНСО3+) ионные пары. Довольно устойчивые комплексные соединения кальций образует с содержащимися в воде органическими веществами.
В речных и озёрных водах концентрация ионов кальция в большинстве случаев находится в пределах от 10 до 100 мг/дм3. При контакте вод с минералами, содержащими кальций, его содержание может повышаться до нескольких сотен миллиграммов в кубическом дециметре.
Предельно допустимая концентрация (ПДК) кальция в воде водных объектов рыбохозяйственного значения составляет 180 мг/дм3, для водных объектов хозяйственно-питьевого водопользования ПДК не установлена.
|
РУКОВОДЯЩИЙ ДОКУМЕНТ |
|
МАССОВАЯ
КОНЦЕНТРАЦИЯ ИОНОВ КАЛЬЦИЯ В ВОДАХ |
Дата введения - 2018-10-01
1 Область применения
1.1 Настоящий руководящий документ устанавливает методику измерений (далее - методика) массовой концентрации ионов кальция в пробах природных и очищенных сточных вод в диапазоне от 1,0 до 2000 мг/дм3 титриметрическим методом с трилоном Б.
1.2 Настоящий руководящий документ предназначен для использования в лабораториях, осуществляющих анализ природных и очищенных сточных вод.
2 Нормативные ссылки
В настоящем руководящем документе использованы ссылки на следующие нормативные документы:
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 17.1.5.04-81 Охрана природы. Гидросфера. Приборы и устройства для отбора, первичной обработки и хранения проб природных вод. Общие технические условия
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков
ГОСТ 31861-2012 Вода. Общие требования к отбору проб
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
МИ 2881-2004 Государственная система обеспечения единства измерений. Методики количественного химического анализа. Процедуры проверки приемлемости результатов анализа
Примечания
1 Ссылки на остальные нормативные документы приведены в разделах 4, Б.3 и Б.4 (приложение Б).
2 При пользовании настоящим руководящим документом целесообразно проверять действие национальных стандартов - в информационной системе общего пользования - на официальном сайте национального органа Российской Федерации по стандартизации в сети Интернет или по ежегодно издаваемому информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году.
3 Если ссылочный нормативный документ заменен (изменен), то при пользовании настоящим руководящим документом следует руководствоваться замененным (измененным) нормативным документом. Если ссылочный нормативный документ отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Требования к показателям точности измерений
3.1 При соблюдении всех регламентируемых методикой условий проведения измерений характеристики погрешности результата измерения с вероятностью 0,95 не должны превышать значений, приведенных в таблице 1.
Таблица 1 - Диапазон измерений, показатели повторяемости, воспроизводимости, правильности и точности при принятой вероятности Р = 0,95
|
Диапазон измерения массовой концентрации ионов кальция X, мг/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости) σr, мг/дм3 |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) σR, мг/дм3 |
Показатель правильности (границы систематической погрешности) ±Δс, мг/дм3 |
Показатель точности (границы абсолютной погрешности) ±Δ, мг/дм3 |
|
От 1,0 до 2000 включ. |
0,1 + 0,004·X |
0,1 + 0,031·X |
0,1 + 0,018·X |
0,2 + 0,063·X |
Предел обнаружения ионов кальция титриметрическим методом составляет 0,6 мг/дм3.
3.2 Значения показателя точности методики используют при:
- оформлении результатов измерений, выдаваемых лабораторией;
- оценке деятельности лабораторий на качество проведения измерений;
- оценке возможности использования результатов измерений при реализации методики в конкретной лаборатории.
4 Требования к средствам измерений, вспомогательным устройствам, реактивам, материалам
4.1 Средства измерений, вспомогательные устройства
4.1.1 Весы неавтоматического действия (лабораторные) специального (I) класса точности по ГОСТ Р 53228-2008 или ГОСТ OIML R 76-1-2011, действительная цена деления (шкалы) 0,0001 г.
4.1.2 Весы неавтоматического действия (лабораторные) высокого (II) класса точности по ГОСТ Р 53228-2008 или ГОСТ OIML R 76-1-2011, действительная цена деления (шкалы) 0,001 г или 0,01 г.
4.1.3 Государственный стандартный образец состава водного раствора ионов кальция ГСО 8065-94 или аналогичный с относительной погрешностью аттестованного значения 1 % (далее - ГСО).
4.1.4 Колбы мерные 2-го класса точности исполнения 2 или 2а по ГОСТ 1770-74 вместимостью: 250 см3 - 4 шт., 500 см3 - 2 шт.
4.1.5 Бюретки 2-го класса точности исполнения 1, 3 по ГОСТ 29251-91 вместимостью: 5 см3 - 1 шт., 10 см3 - 1 шт., 25 см3 - 1 шт.
4.1.6 Пипетки градуированные 2-го класса точности исполнения 1 или 2 по ГОСТ 29227-91 вместимостью: 1 см3 - 5 шт., 2 см3 - 3 шт., 5 см3 - 1 шт., 10 см3 - 1 шт.
4.1.7 Пипетки с одной отметкой 2-го класса точности исполнения 2 по ГОСТ 29169-91 вместимостью: 10 см3 - 2 шт., 25 см3 - 2 шт., 50 см3 - 2 шт., 100 см3 - 2 шт.
4.1.8 Цилиндры мерные 2-го класса точности исполнения 1 или 3 по ГОСТ 1770-74 вместимостью: 25 см3 - 1 шт., 50 см3 - 1 шт., 100 см3 - 2 шт., 500 см3 - 1 шт., 1000 см3 - 1 шт.
4.1.9 Пробирки конические исполнения 1 по ГОСТ 1770-74 вместимостью 10 см3 - 2 шт.
4.1.10 Колбы конические Кн исполнения 2 по ГОСТ 25336-82 вместимостью: 250 см3 - 10 шт., 500 см3 - 2 шт.
4.1.11 Воронки лабораторные типа В по ГОСТ 25336-82 диаметром: 56 мм - 1 шт., 75 мм - 4 шт.
4.1.12 Стаканы В-1, ТХС, по ГОСТ 25336-82 вместимостью: 100 см3 - 3 шт., 250 см3 - 2 шт., 400 см3 - 2 шт., 600 см3 - 2 шт., 1000 см3 - 2 шт.
4.1.13 Стакан полипропиленовый вместимостью 250 см3.
4.1.14 Стаканчики для взвешивания СВ-19/9 и СВ-24/10 по ГОСТ 25336-82 - 4 шт.
4.1.15 Ступка № 3 или № 4 по ГОСТ 9147-80.
4.1.16 Чашка типа ЧБН (Петри) исполнения 2 по ГОСТ 25336-82.
4.1.17 Колонка хроматографическая диаметром от 1,5 до 2,0 см и длиной от 25 до 30 см.
4.1.18 Посуда стеклянная для хранения растворов вместим остью 100, 250, 500 и 1000 см3 из светлого и темного стекла.
4.1.19 Посуда полиэтиленовая для хранения проб воды и растворов вместимостью 250, 500 см3.
4.1.20 Эксикатор исполнения 2 с диаметром корпуса 190 мм по ГОСТ 25336-82.
4.1.21 Устройство для фильтрования проб с использованием мембранных или бумажных фильтров.
4.1.22 Шкаф сушильный общелабораторного назначения.
4.1.23 Электроплитка с закрытой спиралью по ГОСТ 14919-83.
Примечание - Допускается использование других типов средств измерений, посуды и вспомогательного оборудования, в том числе импортных, с характеристиками не хуже, чем у приведенных в 4.1.
4.2 Реактивы и материалы
4.2.1 Кальций углекислый (карбонат кальция) по ГОСТ 4530-76, х.ч.
4.2.2 Соль динатриевая этилендиамин-N,N,N',N'-тетрауксусной кислоты, 2-водная (трилон Б) по ГОСТ 10652-73, ч.д.а. или стандарт-титр трилон Б с молярной концентрацией c(1/2C10H14N2O8Na2·2H2O) = 0,1 моль/дм3 по ТУ 2642-001-33813273-97.
4.2.3 Цинк гранулированный по ТУ 6-09-5294-86, ч.д.а.
4.2.4 Стандарт-титр магний сернокислый 7-водный с молярной концентрацией c(1/2MgSO4·7H2O) = 0,1 моль/дм3 по ТУ 2642-001-33813273-97.
4.2.5 Стандарт-титр цинк сернокислый 7-водный с молярной концентрацией c(1/2ZnSO4·7H2O) = 0,1 моль/дм3 по ТУ 2642-001-33813273-97.
4.2.6 Аммоний хлористый (хлорид аммония) по ГОСТ 3773-72, ч.д.а.
4.2.7 Аммиак водный по ГОСТ 3760-79, ч.д.а.
4.2.8 Натрий хлористый (хлорид натрия) по ГОСТ 4233-77, х.ч.
4.2.9 Натрия гидроокись (гидроксид натрия) по ГОСТ 4328-77, ч.д.а.
4.2.10 Натрий сернистый 9-водный (сульфид натрия) по ГОСТ 2053-77, ч.д.а. или натрия N,N-диэтилдитиокарбамат 3-водный (диэтилдитиокарбамат натрия) по ГОСТ 8864-71, ч.д.а.
4.2.11 Кислота соляная по ГОСТ 3118-77, х.ч.
4.2.12 Мурексид (аммоний пурпуровокислый 1-водный) по ТУ 6-09-13-945-94, ч.д.а.
4.2.13 Нафтоловый зеленый Б по ТУ 6-09-3542-84, ч.
4.2.14 Эриохром черный Т по ТУ 6-09-1760-87, ч.д.а.
4.2.15 Гидроксиламина гидрохлорид по ГОСТ 5456-79, ч.д.а.
4.2.16 Квасцы алюмокалиевые по ГОСТ 4329-77, ч.д.а.
4.2.17 Барий хлорид 2-водный (хлорид бария) по ГОСТ 4108-72, ч.д.а.
4.2.18 Вода дистиллированная по ГОСТ 6709-72.
4.2.19 Фильтры бумажные обеззоленные «белая лента» и «синяя лента» по ТУ 6-09-1678-95.
4.2.20 Фильтры мембранные «Владипор МФАС-ОС-2», 0,45 мкм, по ТУ 6-55-221-1-29-89 или другого типа с равноценными характеристиками.
4.2.21 Универсальная индикаторная бумага (pH от 0 до 12) по ТУ 2642-054-23050963-2008.
4.2.22 Уголь активный БАУ-А по ГОСТ 6217-74.
Примечание - Допускается использование реактивов и материалов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже указанной в 4.2.
5 Метод измерений
Выполнение измерений основано на способности ионов кальция образовывать с трилоном Б малодиссоциируемое, устойчивое в щелочной среде соединение. Конечная точка титрования определяется по изменению окраски индикатора (мурексида) из розовой в красно-фиолетовую. Для увеличения четкости перехода окраски предпочтительнее использовать смешанный индикатор (мурексид + нафтоловый зелёный Б). При этом в конечной точке титрования окраска изменяется от грязно-зеленой до синей.
Магний в условиях анализа осаждается в виде гидроксида и не мешает определению.
6 Требования безопасности, охраны окружающей среды
6.1 При выполнении измерений массовой концентрации ионов кальция в пробах природных и очищенных сточных вод соблюдают требования безопасности, установленные в государственных стандартах и соответствующих нормативных документах.
6.2 По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся ко 2-му, 3-му классам опасности по ГОСТ 12.1.007.
6.3 Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных ПДК в соответствии с ГОСТ 12.1.005.
6.4 Особых требований по экологической безопасности не предъявляется.
7 Требования к квалификации операторов
К выполнению измерений и обработке их результатов допускают лиц с высшим или средним профессиональным образованием, имеющих стаж работы в лаборатории не менее 6 мес и освоивших методику.
8 Требования к условиям измерений
При выполнении измерений соблюдают следующие условия:
|
- температура окружающего воздуха, °С |
22 ± 5; |
|
- атмосферное давление, кПа (мм рт. ст.) |
от 84,0 до 106,7 (от 630 до 800); |
|
- влажность воздуха при температуре 25 °С, %, не более |
80; |
|
- напряжение в сети, В |
220 ± 22; |
|
- частота переменного тока в сети питания, Гц |
50 ± 1. |
9 Подготовка к выполнению измерений
9.1 Отбор и хранение проб
Отбор проб для определения ионов кальция производится в соответствии с ГОСТ 17.1.5.05 и ГОСТ 31861. Оборудование для отбора проб должно соответствовать ГОСТ 17.1.5.04 и ГОСТ 31861. Пробы помещают в стеклянную или пластиковую посуду. Пробы, содержащие взвешенные вещества, фильтруют через мембранный фильтр 0,45 мкм или бумажный фильтр «синяя лента», отбрасывая первую порцию фильтрата.
Пробы не консервируют, хранят при комнатной температуре не более 6 мес. Объем отбираемой пробы должен составлять не менее 500 см3.
9.2 Приготовление растворов
9.2.1 Раствор трилона Б с молярной концентрацией c(1/2C10H14N2O8Na2), равной 0,02 моль/дм3
В мерной колбе вместимостью 1000 см3 растворяют 3,72 г трилона Б в 100 см3 дистиллированной воды, доводят объем раствора до метки на колбе и перемешивают.
Допускается приготовление раствора трилона Б с концентрацией 0,02 моль/дм3 из стандарт-титров (фиксаналов) трилона Б. Для этого растворяют содержимое ампулы в мерной колбе вместимостью 500 см3, далее отбирают пипеткой с одной отметкой 100 см3 полученного раствора и переносят в мерную колбу вместимостью 1000 см3, доводят до метки на колбе дистиллированной водой и перемешивают.
Точную молярную концентрацию раствора устанавливают по раствору соли цинка или магния в соответствии с 9.3 не реже 1 раза в мес.
Срок хранения при комнатной температуре в плотно закрытой посуде не ограничен.
9.2.2 Раствор хлорида цинка с молярной концентрацией c(1/2ZnCl2), равной 0,02 моль/дм3
В стаканчик для взвешивания отбирают около 0,35 г металлического цинка, смачивают его небольшим количеством концентрированной соляной кислоты и сразу же промывают дистиллированной водой. Цинк сушат в сушильном шкафу при температуре 105 °С в течение 1 ч, затем охлаждают и взвешивают на весах специального класса точности с точностью до четвертого знака после запятой.
Навеску цинка количественно переносят в мерную колбу вместимостью 500 см3, в которую предварительно вносят 10 см3 дистиллированной воды и 1,5 см3 концентрированной соляной кислоты. Цинк растворяют. После растворения объем раствора доводят до метки на колбе дистиллированной водой и перемешивают.
Рассчитывают точную концентрацию хлорида цинка c(1/2ZnCl2), моль/дм3, в полученном растворе по формуле
|
|
(1) |
где q - масса навески металлического цинка, г;
32,69 - молярная масса (1/2Zn2+), г/моль;
V - вместимость мерной колбы, дм3.
При расчете значение c(1/2ZnCl2) округляют до четырех значащих цифр.
Раствор хлорида цинка хранят при комнатной температуре в плотно закрытой посуде не более 6 мес.
9.2.3 Раствор сульфата цинка с молярной концентрацией c(1/2ZnSO4), равной 0,02000 моль/дм3
Содержимое ампулы растворяют в мерной колбе вместимостью 500 см3, далее отбирают пипеткой с одной отметкой 100,0 см3 полученного раствора и переносят в мерную колбу вместимостью 1000 см3, доводят до метки на колбе дистиллированной водой и перемешивают. Растворы хранят при комнатной температуре в плотно закрытой посуде не более 6 мес.
9.2.4 Раствор сульфата магния с молярной концентрацией c(1/2MgSO4), равной 0,02000 моль/дм3
Содержимое ампулы растворяют в мерной колбе вместимостью 500 см3, далее отбирают пипеткой с одной отметкой 100,0 см3 полученного раствора и переносят в мерную колбу вместимостью 1000 см3, доводят до метки на колбе дистиллированной водой и перемешивают.
Растворы хранят при комнатной температуре в плотно закрытой посуде не более 6 мес.
9.2.5 Аммонийно-аммиачный буферный раствор
В мерной колбе вместимостью 500 см3 растворяют в 100 см3 дистиллированной воды 7,0 г хлорида аммония и добавляют 75 см3 концентрированного раствора аммиака. Объем раствора доводят до метки на колбе дистиллированной водой и тщательно перемешивают. Срок хранения раствора в полиэтиленовой посуде не более 2 мес.
9.2.6 Индикатор эриохром черный Т
В ступке с 50 г хлорида натрия тщательно растирают 0,5 г эриохрома черного Т. Срок хранения в склянке из темного стекла не более 6 мес.
9.2.7 Индикатор мурексид
В ступке со 100 г хлорида натрия тщательно растирают 0,2 г мурексида. Срок хранения в склянке из темного стекла не более 6 мес.
9.2.8 Смешанный индикатор
В ступке со 100 г хлорида натрия тщательно растирают 0,2 г мурексида и 0,4 г нафтолового зеленого Б. Срок хранения в склянке из темного стекла не более 6 мес.
9.2.9 Раствор нафтолового зеленого Б, 0,8 %-ный
В 50 см3 дистиллированной воды растворяют 0,4 г нафтолового зеленого Б. Срок хранения раствора в склянке из темного стекла не более 3 мес.
9.2.10 Раствор нафтолового зеленого Б, 0,08 %-ный
К 5 см3 0,8 %-ного раствора нафтолового зеленого Б добавляют 45 см3 дистиллированной воды и перемешивают. Срок хранения раствора в склянке из темного стекла не более 3 дней.
9.2.11 Раствор гидроксида натрия, 20 %-ный
Растворяют 20 г гидроксида натрия в 80 см3 дистиллированной воды. Срок хранения раствора в полиэтиленовой посуде не ограничен.
9.2.12 Раствор гидроксида натрия, 8 %-ный
Растворяют 40 г гидроксида натрия в 460 см3 дистиллированной воды. Срок хранения раствора в полиэтиленовой посуде не ограничен.
9.2.13 Раствор гидроксида натрия, 0,4 %-ный
Растворяют 2 г гидроксида натрия в 500 см3 дистиллированной воды. Срок хранения раствора в полиэтиленовой посуде не более 6 мес.
9.2.14 Раствор гидроксида натрия, 1 моль/дм3
Растворяют 20 г гидроксида натрия в 500 см3 дистиллированной воды. Срок хранения раствора в плотно закрытой полиэтиленовой посуде не ограничен.
9.2.15 Раствор сульфида натрия
В 50 см3 дистиллированной воды растворяют 2 г сульфида натрия. Срок хранения раствора в плотно закрытой полиэтиленовой посуде в холодильнике не более недели.
9.2.16 Раствор диэтилдитиокарбамата натрия
В 50 см3 дистиллированной воды растворяют 5 г диэтилдитиокарбамата натрия. Срок хранения раствора в холодильнике в плотно закрытой склянке не более 2 недель.
9.2.17 Раствор гидрохлорида гидроксиламина
В 100 см3 дистиллированной воды растворяют 5 г гидрохлорида гидроксиламина. Срок хранения раствора в холодильнике в плотно закрытой склянке из темного стекла не более 1 мес.
9.2.18 Раствор соляной кислоты, 4 моль/дм3
В 330 см3 дистиллированной воды растворяют 170 см3 концентрированной соляной кислоты. Срок хранения раствора в плотно закрытой склянке не ограничен.
9.2.19 Суспензия гидроксида алюминия
Растворяют 63 г алюмокалиевых квасцов в 500 см3 дистиллированной воды в стакане вместимостью 1 дм3, нагревают раствор до 60 °С и при постоянном перемешивании медленно прибавляют 28 см3 аммиака водного. Дают смеси отстояться в течение 1 ч, а затем промывают несколько раз дистиллированной водой, сливая жидкость над осадком. Последняя промывная вода не должна давать положительной реакции на хлориды (проба с 10 %-ным раствором нитрата серебра). Полученную суспензию хранят при комнатной температуре под слоем дистиллированной воды в защищенном от света месте не более 3 мес.
9.2.20 Раствор нитрата серебра, 10%-ный
Растворяют 10 г нитрата серебра в 90 см3 дистиллированной воды и прибавляют 1 - 2 капли концентрированной азотной кислоты. При появлении мутности раствор отстаивают не менее 1 сут, затем осторожно сливают прозрачную жидкость. Срок хранения раствора в плотно закрытой склянке из темного стекла не ограничен.
9.2.21 Активный уголь
Подготовку к работе и регенерацию активного угля осуществляют в соответствии с приложением А.
9.3 Установление точной молярной концентрации раствора трилона Б
Для установления точной молярной концентрации раствора трилона Б в коническую колбу вместимостью 250 см3 с помощью пипетки с одной отметкой вносят 10,0 см3 раствора хлорида цинка (9.2.2), добавляют мерным цилиндром 90 см3 дистиллированной воды, градуированной пипеткой 5 см3 аммонийно-аммиачного буферного раствора и от 70 до 100 мг индикатора эриохрома черного Т. Содержимое колбы тщательно перемешивают и титруют из бюретки вместимостью 25 см3 раствором трилона Б до перехода окраски из фиолетово-красной в голубую (синюю) до отсутствия красного оттенка. Титрование повторяют и, при отсутствии расхождения в объёмах раствора трилона Б более 0,05 см3, за результат принимают среднее арифметическое значение. В противном случае повторяют титрование до получения результатов, отличающихся не более, чем на 0,05 см3.
Концентрацию раствора трилона Б, c(1/2C10H14N2O8Na2), моль/дм3, рассчитывают по формуле
|
|
(2) |
где с(1/2ZnСl2) - концентрация раствора хлорида цинка, моль/дм3;
![]() - среднее арифметическое значение
объема раствора трилона Б, израсходованного на титрование раствора хлорида
цинка, см3;
- среднее арифметическое значение
объема раствора трилона Б, израсходованного на титрование раствора хлорида
цинка, см3;
VZn - объем раствора хлорида цинка, отобранный для титрования см3.
Рассчитанное значение молярной концентрации раствора трилона Б округляют до четырех значащих цифр.
Допускается установление точной концентрации раствора трилона Б по растворам сульфата цинка (9.2.3) или сульфата магния (9.2.4), приготовленных из стандарт-титров (фиксаналов).
10 Порядок выполнения измерений
10.1 Выбор условий титрования
Объём аликвоты пробы воды для выполнения измерений массовой концентрации ионов кальция выбирают исходя из известной жёсткости воды или по результатам оценочного титрования.
Для оценочного титрования отбирают пипеткой 10 см3 воды, добавляют 0,2 см3 8 %-ного раствора гидроксида натрия, около 25 мг индикатора мурексида и титруют раствором трилона Б до перехода окраски из розовой в красно-фиолетовую. По израсходованному на титрование объему раствора трилона Б выбирают из таблицы 2 соответствующий объем аликвоты пробы воды для выполнения измерений массовой концентрации ионов кальция.
Таблица 2 - Объем пробы воды, рекомендуемый для выполнения измерений массовой концентрации ионов кальция
|
Значение жесткости воды, °Ж |
Объем раствора трилона Б, израсходованный при оценочном титровании, см3 |
Рекомендуемый объем аликвоты пробы воды, см3 |
|
Менее 5 |
Менее 2 |
100 |
|
От 5 до 10 включ. |
От 2 до 4 включ. |
50 |
|
Св. 10 до 20 включ. |
Св. 4 до 8 включ. |
25 |
|
Св. 20 |
Св. 8 |
10 |
В зависимости от концентрации ионов кальция титрование следует проводить из бюретки подходящей вместимости. Если по результатам оценочного титрования объем трилона Б менее 0,4 см3 или жесткость менее 1 °Ж, используют бюретку вместимостью 5 см3; при объеме трилона Б менее 0,8 см3 или жесткости от 1 до 2 °Ж - бюретку вместимостью 10 см3; при более высокой концентрации ионов кальция или жесткости - бюретку вместимостью 25 см3. При отсутствии бюретки вместимостью 10 см3 можно использовать бюретку вместимостью 25 см3; допускается замена бюретки вместимостью 5 см3 бюреткой вместимостью 10 см3, однако замена бюретки вместимостью 5 см3 бюреткой вместимостью 25 см3 недопустима.
10.2 Титрование
10.2.1 В коническую колбу вместимостью 250 см3 отмеривают пипеткой требуемый объем аликвоты пробы, доводят, если необходимо, до 100 см3 дистиллированной водой, добавляют градуированной пипеткой 2 см3 8 %-ного раствора гидроксида натрия, около 0,25 г индикатора мурексида (см. 9.2.7) или смешанного индикатора (см. 9.2.8) и титруют раствором трилона Б до перехода окраски из розовой в красно-фиолетовую при использовании мурексида или из грязно-зелёной в синюю при титровании со смешанным индикатором. Повторяют титрование и, если расхождение объемов трилона Б между параллельными титрованиями не превышает приведенных в таблице 3, то проводят оперативный контроль повторяемости по 13.2. В случае неудовлетворительного результата оперативного контроля повторяемости повторяют титрование до получения допустимого расхождения результатов.
Таблица 3 - Допустимые расхождения между параллельными титрованиями в зависимости от объема раствора трилона Б
|
Объем раствора трилона Б, израсходованный на титрование, см3 |
Допустимое расхождение объемов трилона Б, см3 |
|
До 3 включ. |
0,05 |
|
Св. 3 до 8 включ. |
0,10 |
|
Св. 8 до 12 включ. |
0,15 |
|
Св. 12 |
0,20 |
10.2.2 Если в период хранения в пробе выпал осадок карбоната кальция, непосредственно перед выполнением измерений прозрачную часть пробы декантируют (или сливают посредством сифона) в чистую сухую колбу. Оставшийся в склянке осадок растворяют, добавив от 0,5 до 1 см3 концентрированной соляной кислоты. Затем прозрачную часть пробы и жидкость с растворенным осадком соединяют вместе и нейтрализуют 20 %-ным раствором гидроксида натрия, добавляя его по каплям и контролируя pH по индикаторной бумаге. Далее отбирают аликвоту полученного раствора и проводят титрование.
10.2.3 Для получения достаточно четкого перехода окраски при титровании со смешанным индикатором важно соотношение мурексида и нафтолового зеленого в смеси. Для разных партий индикаторов это соотношение может быть разным. Если при использовании сухого смешанного индикатора не удается получить четкий переход окраски в конечной точке титрования, следует использовать нафтоловый зеленый в виде 0,08 %-ного раствора (см. 9.2.10). Титрование проводят следующим образом. Отбирают аликвоту воды в коническую колбу, добавляют градуированной пипеткой 2 см3 8 %-ного раствора гидроксида натрия, около 0,25 г индикатора мурексида (см. 9.2.7), перемешивают и приливают раствор нафтолового зеленого Б до тех пор, пока раствор приобретет грязно-зеленую окраску (всего идет примерно от 0,9 до 1,2 см3 раствора). После этого титруют пробу в соответствии с 10.2.1.
10.3 Устранение мешающих влияний
10.3.1 Выполнению измерений массовой концентрации ионов кальция мешают ионы железа (более 10 мг/дм3), кобальта, никеля (более 0,1 мг/дм3), алюминия (более 10 мг/дм3), меди (более 0,05 мг/дм3), вызывая нечеткое изменение окраски в точке эквивалентности, либо полностью исключая возможность индикации конечной точки титрования.
Другие катионы, например, свинец, кадмий, марганец (II), цинк, стронций, барий при высоких концентрациях (как правило, не встречающихся в природных водах) могут частично титроваться вместе с кальцием и магнием и повышать расход трилона Б. Для устранения или уменьшения мешающего влияния катионов металлов к пробе перед титрованием прибавляют градуированной пипеткой 0,5 см3 раствора сульфида или диэтилдитиокарбамата натрия и 0,5 см3 раствора гидрохлорида гидроксиламина.
10.3.2 Результаты титрования могут быть искажены в присутствии значительных количеств анионов (НСO3ˉ, СO32-, РO43-, SiO32-). Для уменьшения их влияния пробу следует титровать сразу после добавления гидроксида натрия и индикатора.
10.3.3 Мешающее влияние взвешенных веществ устраняется фильтрованием пробы.
10.3.4 Если проба воды заметно окрашена за счёт присутствия веществ природного или антропогенного происхождения, затрудняется фиксация конечной точки титрования. В этом случае пробу перед выполнением измерений следует пропустить со скоростью от 3 до 5 см3/мин через хроматографическую колонку, заполненную активным углем (высота слоя не менее 15 см). Первые 25 см3 пробы, прошедшей через колонку, отбрасывают.
Как правило, окрашенные соединения антропогенного происхождения сорбируются активным углем практически полностью, в то время как природного (гумусовые вещества) - лишь частично. При неустраняемой активным углем цветности пробы, обусловленной гумусовыми веществами, определение конечной точки титрования значительно облегчается использованием для сравнения слегка перетитрованной пробы этой же воды (пробы-свидетеля).
10.3.5 Если высокая цветность не позволяет установить конечную точку титрования, для устранения цветности можно использовать суспензию гидроксида алюминия.
Для этого в стакан вместимостью 400 или 600 см3 с помощью пипетки вместимостью 100 см3 помещают 200 см3 пробы, приливают к ней градуированной пробиркой 6 см3 суспензии гидроксида алюминия, перемешивают до обесцвечивания пробы и дают отстояться. Фильтруют пробу через бумажный фильтр «белая лента», промытый дистиллированной водой, в мерную колбу вместимостью 250 см3. Осадок в стакане и фильтр промывают 3 раза небольшими порциями дистиллированной воды, собирая промывные воды в ту же колбу. После этого доводят раствор в колбе до метки, перемешивают, отбирают из колбы необходимую аликвоту и титруют ее в соответствии с 10.2.
10.3.6 При достаточно высокой концентрации ионов кальция устранить мешающие влияния можно разбавлением пробы дистиллированной водой.
11 Обработка результатов измерений
11.1 Массовую концентрацию ионов кальция X, мг/дм3, в анализируемой пробе воды рассчитывают по формуле
|
|
(3) |
где 20,04 - молярная масса (1/2Са2+), мг/ммоль;
c(1/2C10H14N2O8Na2) - молярная концентрация раствора трилона Б, моль/дм3;
Vт - объем раствора трилона Б, израсходованный на титрование пробы воды, см3;
Vпp - объем пробы воды, взятый для титрования, см3.
11.2 Если для устранения цветности использовали суспензию гидроксида алюминия, то в полученный результат следует ввести поправку на разбавление - умножить результат на коэффициент 1,25.
12 Оформление результатов измерений
12.1 Результат измерения в документах, предусматривающих его использование, представляют в виде
|
|
(4) |
где ![]() - среднее
арифметическое значение двух результатов, разность между которыми не превышает
предела повторяемости rn (2,77·σr), мг/дм3, при превышении предела
повторяемости поступают согласно 13.2;
- среднее
арифметическое значение двух результатов, разность между которыми не превышает
предела повторяемости rn (2,77·σr), мг/дм3, при превышении предела
повторяемости поступают согласно 13.2;
±Δ - границы абсолютной погрешности результатов измерений для данной массовой концентрации ионов кальция, мг/дм3 (см. таблицу 1).
Абсолютные погрешности результатов измерений представляют числом, содержащим не более двух значащих цифр. Наименьшие разряды числовых значений результатов измерений принимают такими же, как и наименьшие разряды числовых значений абсолютных погрешностей результатов измерений.
12.2 Допустимо представлять результат в виде
|
|
(5) |
где ±ΔЛ - границы абсолютной погрешности результатов анализа, установленные при реализации методики в лаборатории и обеспечиваемые контролем стабильности результатов измерений, мг/дм3.
12.3 Результаты измерения оформляют протоколом или записью в журнале по формам, приведенным в Руководстве по качеству лаборатории.
13 Контроль качества результатов измерений при реализации методики в лаборатории
13.1 Общие положения
13.1.1 Контроль качества результатов измерений при реализации методики в лаборатории предусматривает:
- оперативный контроль исполнителем процедуры выполнения измерений (на основе оценки повторяемости и погрешности при реализации отдельно взятой контрольной процедуры);
- контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, погрешности).
13.1.2 Периодичность оперативного контроля исполнителем процедуры выполнения измерений, а также реализуемые процедуры контроля стабильности результатов выполняемых измерений регламентируются в Руководстве по качеству лаборатории.
13.2 Алгоритм оперативного контроля повторяемости
13.2.1 Оперативный контроль повторяемости осуществляют для каждого из результатов измерений, полученных в соответствии с методикой. Для этого отобранную пробу воды делят на две части и выполняют анализ в соответствии с разделом 10.2.
13.2.2 Результат контрольной процедуры rк, мг/дм3, рассчитывают по формуле
|
|
(6) |
где Х1, Х2 - результаты параллельных измерений массовой концентрации ионов кальция в пробе, мг/дм3.
13.2.3 Предел повторяемости rn, мг/дм3, рассчитывают по формуле
|
rn = 2,77·σr, |
(7) |
где σr - показатель повторяемости для массовой концентрации ионов кальция, равной (Х1 + Х2)/2, мг/дм3 (см. таблицу 1).
13.2.4 Результат контрольной процедуры должен удовлетворять условию
|
rк ≤ rn. |
(8) |
13.2.5 При несоблюдении условия (8) выполняют еще два измерения и сравнивают разницу между максимальным и минимальным результатами с нормативом контроля. В случае превышения предела повторяемости, поступают в соответствии с ГОСТ Р ИСО 5725-6 (раздел 5).
13.3 Алгоритм оперативного контроля процедуры выполнения измерений с использованием метода добавок совместно с методом разбавления проб
13.3.1 Оперативный контроль процедуры выполнения измерений с использованием метода добавок совместно с методом разбавления пробы проводят, если массовая концентрация ионов кальция в рабочей пробе составляет 10 мг/дм3 и более. В противном случае оперативный контроль проводят с использованием метода добавок согласно 13.4. Для введения добавок используют ГСО или аттестованные растворы ионов кальция, методика приготовления которых приведена в приложении Б.
13.3.2 Оперативный контроль исполнителем процедуры выполнения измерений проводят путем сравнения результатов отдельно взятой контрольной процедуры Кк с нормативом контроля К.
13.3.3 Результат контрольной процедуры Кк, мг/дм3, рассчитывают по формуле
|
|
(9) |
где ![]() - среднее арифметическое значение
результатов контрольных измерений массовой концентрации ионов кальция в пробе,
разбавленной в
- среднее арифметическое значение
результатов контрольных измерений массовой концентрации ионов кальция в пробе,
разбавленной в ![]() раз, с известной добавкой, мг/дм3;
раз, с известной добавкой, мг/дм3;
![]() - среднее арифметическое значение
результатов контрольных измерений массовой концентрации ионов кальция в пробе,
разбавленной в
- среднее арифметическое значение
результатов контрольных измерений массовой концентрации ионов кальция в пробе,
разбавленной в ![]() раз, мг/дм3;
раз, мг/дм3;
![]() - среднее арифметическое значение
результатов контрольных измерений массовой концентрации ионов кальция в рабочей
пробе, мг/дм3;
- среднее арифметическое значение
результатов контрольных измерений массовой концентрации ионов кальция в рабочей
пробе, мг/дм3;
Сд - концентрация добавки, мг/дм3.
13.3.4 Норматив контроля К, мг/дм3, рассчитывают по формуле
|
|
(10) |
где ΔЛХ" (ΔЛХ', ΔЛХ) - значения абсолютных погрешностей результатов измерений, установленные при реализации методики в лаборатории, соответствующие массовой концентрации ионов кальция в разбавленной пробе с добавкой (разбавленной пробе, рабочей пробе), мг/дм3.
Примечание - Допустимо для расчета норматива контроля использовать значения абсолютных погрешностей, полученные расчетным путем по формулам ΔЛХ" = 0,84·ΔХ", ΔЛХ' = 0,84·ΔХ' и ΔЛХ = 0,84·ΔХ, где ΔХ", (ΔХ', ΔХ) - значения абсолютных погрешностей результатов измерений, соответствующие концентрации ионов кальция в разбавленной пробе с добавкой (разбавленной пробе, рабочей пробе), мг/дм3.
13.3.5 Если результат контрольной процедуры удовлетворяет условию
|
|Кк| ≤ К, |
(11) |
процедуру анализа признают удовлетворительной.
При невыполнении условия (11) контрольную процедуру повторяют. При повторном невыполнении условия (11) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
13.4 Алгоритм оперативного контроля процедуры выполнения измерений с использованием метода добавок
13.4.1 Оперативный контроль исполнителем процедуры
выполнения измерений проводят путем сравнения результатов отдельно взятой
контрольной процедуры ![]() с нормативом контроля К1.
с нормативом контроля К1.
13.4.2 Результат
контрольной процедуры ![]() , мг/дм3, рассчитывают по
формуле
, мг/дм3, рассчитывают по
формуле
|
|
(12) |
где ![]() - среднее арифметическое значение
результатов контрольных измерений массовой концентрации ионов кальция в пробе с
известной добавкой, мг/дм3.
- среднее арифметическое значение
результатов контрольных измерений массовой концентрации ионов кальция в пробе с
известной добавкой, мг/дм3.
13.4.3 Норматив контроля погрешности К1, мг/дм3, рассчитывают по формуле
|
|
(13) |
где ΔЛХ"', (ΔЛХ) - значения абсолютных погрешностей результатов измерений, установленные при реализации методики в лаборатории, соответствующие массовой концентрации ионов кальция в пробе с добавкой (рабочей пробе), мг/дм3.
Примечание - Допустимо для расчета норматива контроля использовать значения абсолютных погрешностей, полученные расчетным путем по формулам ΔЛХ"' = 0,84·ΔХ"' и ΔЛХ = 0,84·ΔХ, где ΔХ"', ΔХ - приписанные методике значения абсолютных погрешностей, соответствующие массовой концентрации ионов кальция в пробе с добавкой и рабочей пробе, мг/дм3, соответственно.
13.4.4 Если результат контрольной процедуры удовлетворяет условию
|
|
(14) |
процедуру признают удовлетворительной.
При невыполнении условия (14) контрольную процедуру повторяют. При повторном невыполнении условия (14) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
14 Проверка приемлемости результатов, полученных в условиях воспроизводимости
14.1 Расхождение между результатами измерений, полученными в двух лабораториях, не должно превышать предела воспроизводимости. При выполнении этого условия приемлемы оба результата измерений и в качестве окончательного может быть использовано их общее среднее значение. Значение предела воспроизводимости R, мг/дм3, рассчитывают по формуле
|
R = 2,77·σR, |
(15) |
где σR - показатель воспроизводимости, мг/дм3 (см. таблицу 1).
14.2 При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов измерений согласно ГОСТ Р ИСО 5725-6 (раздел 5) или МИ 2881.
14.3 Проверка приемлемости проводится при необходимости сравнения результатов измерений, полученных двумя лабораториями.
Приложение А
Активный уголь помещают в термостойкую коническую колбу вместимостью 500 см3 (слой угля должен быть не более 1/3 высоты колбы), добавляют 150 см3 раствора соляной кислоты, 4 моль/дм3, и кипятят 2 ч, накрыв колбу часовым стеклом. Если раствор кислоты окрашивается, то его сливают и повторяют процедуру до тех пор, пока он не останется бесцветным. Уголь отмывают дистиллированной водой до значения pH, соответствующего pH дистиллированной воды по универсальной индикаторной бумаге. Воду сливают, добавляют 150 см3 раствора гидроксида натрия, 1 моль/дм3, и выдерживают не менее 8 ч. Если появляется окраска, раствор гидроксида натрия сливают и процедуру повторяют до тех пор, пока он не останется бесцветным.
Очищенный уголь отмывают дистиллированной водой до нейтральной реакции по универсальной индикаторной бумаге. Хранят в склянке под слоем дистиллированной воды не более 6 мес.
После пропускания каждой пробы воды уголь в колонке регенерируют промыванием 0,4 %-ным раствором гидроксида натрия до исчезновения окраски последнего, затем дистиллированной водой до нейтральной реакции.
Приложение Б
Методика приготовления аттестованных растворов ионов
кальция
АР1-Са и АР2-Са
Б.1 Назначение и область применения
Настоящая методика регламентирует процедуру приготовления аттестованных растворов ионов кальция, предназначенных для контроля точности результатов измерений массовой концентрации ионов кальция в природных и очищенных сточных водах титриметрическим методом.
Б.2 Метрологические характеристики
Метрологические характеристики аттестованных растворов приведены в таблице Б.1
Таблица Б.1 - Метрологические характеристики аттестованных растворов ионов кальция
|
Наименование характеристики |
Значения характеристик для аттестованного раствора |
|
|
AP1-Ca |
AP2-Ca |
|
|
Аттестованное значение массовой концентрации ионов кальция, мг/см3 |
50,00 |
5,00 |
|
Границы погрешности установления аттестованного значения массовой концентрации ионов кальция (Р = 0,95), мг/см3 |
±0,51 |
±0,05 |
Б.3 Средства измерений, вспомогательные устройства
Б.3.1 Весы неавтоматического действия (лабораторные) специального (I) класса точности по ГОСТ Р 53228-2008 или ГОСТ OIML R 76-1-2011, действительная цена деления (шкалы) 0,0001 г.
Б.3.2 Колбы мерные 2-го класса точности исполнения 2, 2а по ГОСТ 1770-74 вместимостью 250 см3 - 2 шт.
Б.3.3 Пипетка с одной отметкой 2-го класса точности исполнения 2 по ГОСТ 29169-91 вместимостью 25 см3.
Б.3.4 Цилиндр мерный 2-го класса точности исполнения 1 или 3 по ГОСТ 1770-74 вместимостью 250 см3.
Б.3.5 Стакан химический полипропиленовый вместимостью 250 см3.
Б.3.6 Стакан В-1, ТХС, по ГОСТ 25336-82 вместимостью 250 см3.
Б.3.7 Воронка лабораторная типа В по ГОСТ 25336-82 диаметром 56 мм.
Б.3.8 Стекло часовое.
Б.4 Исходные компоненты аттестованных растворов
Б.4.1 Кальций углекислый (карбонат кальция) по ГОСТ 4530-76, х.ч. Основной компонент - СаСО3, массовая доля которого не менее 99 %, молярная масса - 100,09 г/моль.
Б.4.2 Кислота соляная по ГОСТ 3118-77, х.ч.
Б.4.3 Вода дистиллированная по ГОСТ 6709-72.
Б.4.4 Раствор соляной кислоты 1:1 (для приготовления раствора смешивают равные объёмы дистиллированной воды и концентрированной соляной кислоты).
Б.5 Процедура приготовления аттестованных растворов
Б.5.1 Приготовление аттестованного раствора ионов кальция АР1-Са
На весах специального класса точности взвешивают в полипропиленовом стакане вместимостью 250 см3 с точностью до четвертого знака после запятой 31,216 г карбоната кальция. Навеску смачивают дистиллированной водой и при перемешивании добавляют постепенно 120 см3 соляной кислоты (1:1). Накрывают стакан чистым часовым стеклом и оставляют стоять до растворения.
После растворения осторожно, по палочке, переносят раствор через воронку в мерную колбу вместимостью 250 см3. Три раза ополаскивают стакан и воронку дистиллированной водой и переносят смывы в ту же колбу. Доводят раствор в колбе дистиллированной водой до метки и перемешивают.
Полученному раствору приписывают массовую концентрацию ионов кальция 50,00 мг/см3.
При отборе навески карбоната кальция, отличной от значения 31,216 г, концентрации и погрешности аттестованного раствора АР1-Са рассчитывают по Б.6.
Б.5.2 Приготовление аттестованного раствора кальция АР2-Са
В мерную колбу вместимостью 250 см3 пипеткой с одной отметкой вносят 25,0 см3 раствора кальция АР1-Са. Объем раствора доводят до метки на колбе дистиллированной водой и перемешивают.
Полученному раствору приписывают массовую концентрацию ионов кальция 5,00 мг/см3.
Б.6 Расчет метрологических характеристик аттестованных растворов
Б.6.1 Расчет метрологических характеристик аттестованного раствора АР1-Са
Аттестованное значение массовой концентрации ионов кальция С1, мг/см3, рассчитывают по формуле
|
|
(Б.1) |
где т - масса навески карбоната кальция, г;
V - вместимость мерной колбы, см3;
1000 - коэффициент пересчета, мг/г;
40,08 и 100,09 - молярная масса кальция и карбоната кальция, соответственно, г/моль;
Аттестованное значение массовой концентрации ионов кальция в растворе АР1-Са равно
|
|
Расчет предела возможных значений погрешности установления массовой концентрации ионов кальция в растворе АР1-Са Δ1, мг/см3, проводится по формуле
|
|
(Б.2) |
где Δμ - предельное значение возможного отклонения массовой доли основного вещества в реактиве от приписанного значения μ, %;
μ - массовая доля основного вещества (СаСО3) в реактиве, приписанная реактиву квалификации «х.ч.», %;
Δm - предельная возможная погрешность взвешивания, г;
ΔV - предельное значение возможного отклонения объема мерной колбы от номинального значения, см3.
Погрешность установления массовой концентрации ионов кальция в растворе АР1-Са равна
|
|
|
Б.6.2 Расчет метрологических характеристик аттестованного раствора АР2-Са
Аттестованное значение массовой концентрации ионов кальция С2, мг/см3, рассчитывают по формуле
|
|
(Б.3) |
где V1 - объем раствора АР1-Са, отбираемый пипеткой, см3;
V2 - вместимость мерной колбы, см3.
Аттестованное значение массовой концентрации ионов кальция в растворе АР2-Са равно
|
|
|
Расчет предела возможных значений погрешности установления массовой концентрации ионов кальция в растворе АР2-Са Δ2, мг/см3, проводится по формуле
|
|
(Б.4) |
где ![]() - предельное значение возможного
отклонения объема V1 от номинального
значения, см3;
- предельное значение возможного
отклонения объема V1 от номинального
значения, см3;
![]() - предельное значение возможного
отклонения вместимости мерной колбы от номинального значения, см3.
- предельное значение возможного
отклонения вместимости мерной колбы от номинального значения, см3.
Погрешность установления массовой концентрации ионов кальция в растворе АР2-Са равна
|
|
|
Б.7 Требования безопасности
Необходимо соблюдать общие требования техники безопасности при работе в химических лабораториях.
Б.8 Требования к квалификации исполнителей
Аттестованные растворы может готовить специалист с высшим или средним профессиональным образованием, прошедший специальную подготовку и имеющий стаж работы в химической лаборатории не менее 6 мес.
Б.9 Требования к маркировке
На флакон с аттестованными растворами должна быть наклеена этикетка с указанием условного обозначения аттестованного раствора, величины массовой концентрации ионов кальция в растворе, погрешности ее установления и даты приготовления.
Б.10 Условия хранения
Аттестованный раствор АР1-Са хранят в склянке с притертой стеклянной или пластиковой пробкой при комнатной температуре не более года.
Аттестованный раствор АР2-Са хранят в склянке с притертой стеклянной или пластиковой пробкой при комнатной температуре не более 3 мес.
|
Ключевые слова: ионы кальция, методика измерений, природная вода, титрование, массовая концентрация |
Лист регистрации изменений
|
Номер изменения |
Номер страницы |
Номер документа (ОРН) |
Подпись |
Дата |
||||
|
измененной |
замененной |
новой |
аннулированной |
внесения изм. |
введения изм. |
|||
|
|
|
|
|
|
|
|
|
|