МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ,
МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
(ISC)
|
Межгосударственный |
ГОСТ |
ПРОДУКТЫ ПИЩЕВЫЕ,
ПРОДОВОЛЬСТВЕННОЕ СЫРЬЕ
Метод определения остаточного содержания
метаболитов карбадокса и олаквиндокса с помощью
высокоэффективной жидкостной хроматографии
с масс-спектрометрическим детектором
|
|
Москва Стандартинформ 2016 |
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены»
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГБУ «ВГНКИ»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 25 октября 2016 г. № 92-П)
За принятие проголосовали:
|
Краткое наименование страны по MK (ИСО 3166) 004-97 |
Код страны по MK (ИСО 3166) 004-97 |
Сокращенное наименование национального органа по стандартизации |
|
Армения |
AM |
Минэкономики Республики Армения |
|
Казахстан |
KZ |
Госстандарт Республики Казахстан |
|
Киргизия |
KG |
Кыргызстандарт |
|
Россия |
RU |
Росстандарт |
(Поправка).
4 Приказом Федерального агентства по техническому регулированию и метрологии от 15 ноября 2016 г. № 1692-ст межгосударственный стандарт ГОСТ 33971-2016 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2018 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок - в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
Содержание
ГОСТ 33971-2016
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ, ПРОДОВОЛЬСТВЕННОЕ СЫРЬЕ
Метод определения остаточного содержания
метаболитов карбадокса и олаквиндокса
с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим
детектором
Food products, food raw materials.
Method for determination of residual metabolites of carbadox and olaquindox
using
high-performance liquid chromatography with mass spectrometric detector
Дата введения -2018-01-01
1 Область применения
Настоящий стандарт распространяется на непереработанные пищевые продукты: мясо животных всех видов, в том числе мясо птицы, субпродукты (печень, почки) и устанавливает метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием (далее - ВЭЖХ-МС/МС) для определения остаточного содержания метаболитов карбадокса и олаквиндокса в диапазоне измерений от 0,5 до 8,0 мкг/кг.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты*
* В Российской Федерации действует ГОСТ Р 12.1.019-2009 «Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты».
ГОСТ 12.2.085-2002 Сосуды, работающие под давлением. Клапаны предохранительные. Требования безопасности
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 2603-79 Реактивы. Ацетон. Технические условия
ГОСТ ИСО 5725-6-2003 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике**
** В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике».
ГОСТ 5848-73 Реактивы. Кислота муравьиная. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
ГОСТ 7269-2015 Мясо. Методы отбора образцов и органолептические методы определения свежести
ГОСТ 9293-74 (ИСО 2435-73) Азот газообразный и жидкий. Технические условия
ГОСТ 22300-76 Реактивы. Эфиры этиловый и бутиловый уксусной кислоты. Технические условия
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 31467-2012 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка их к испытаниям
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Сущность метода
Метод основан на экстракции метаболитов карбадокса и олаквиндокса раствором сульфосалициловой кислоты, переэкстракции в этилацетат, концентрировании и перерастворении полученного экстракта, с последующим их количественным определением методом ВЭЖХ-МС/МС в режиме мониторинга множественных реакций (MRM). Количественное определение остаточного содержания метаболитов карбадокса и олаквиндокса (аналитов) проводят методом внутреннего стандарта.
4 Требования безопасности и условия выполнения измерений
4.1 Применяемые в работе реактивы относятся к веществам 1-го и 2-го классов опасности по ГОСТ 12.1.007, при работе с ними необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005.
4.2 Помещения, в которых проводят анализ и подготовку проб, должны быть оборудованы приточно-вытяжной вентиляцией.
4.3 Приготовление градуировочных растворов проводят в вытяжном шкафу.
4.4 При выполнении измерений с использованием жидкостного хроматографа соблюдают правила по электробезопасности по ГОСТ 12.1.019 и правила безопасной эксплуатации сосудов, работающих под давлением по ГОСТ 12.2.085.
4.5 Утилизацию отходов проб и реактивов осуществляют в соответствии с требованиями законодательства государства, принявшего стандарт.
4.6 К выполнению измерений методом ВЭЖХ-МС/МС допускаются лица, владеющие техникой ВЭЖХ-МС/МС и изучившие инструкции по эксплуатации применяемой аппаратуры.
4.7 При выполнении измерений соблюдают следующие условия:
- температура окружающего воздуха...................от 15 °С до 30 °С;
- атмосферное давление ........................................от 84 до 106 кПа;
- относительная влажность воздуха......................от 20 % до 80 %.
(Поправка, ИУС 7-2017)
5 Средства измерений, аппаратура, материалы, посуда и реактивы
5.1 Для определения остаточного содержания метаболитов карбадокса и олаквиндокса применяют следующие средства измерений, аппаратуру, материалы и посуду:
- весы неавтоматического действия высокого класса точности по ГОСТ OIML R 76-1 с пределом допускаемой абсолютной погрешности ±0,01 г;
- весы специального класса точности по ГОСТ OIML R 76-1 с действительной ценой деления шкалы не более 0,1 мг;
- масс-спектрометр с квадрупольным анализатором диапазоном измерений от 50 до 300 атомных единиц массы (а. е. м.), массовым разрешением не менее 1 а. е. м. на полувысоте пика, с пределами допускаемой абсолютной погрешности не более ±0,5 а. е. м., с режимом получения и анализа фрагментных ионов (режим МС/МС);
- рН-метр или универсальный иономер диапазоном измерения от 4 до 9 ед. рН с погрешностью измерения ±0,05 ед. рН;
- баню ультразвуковую с рабочей частотой не менее 20 Гц и объемом не менее 1 дм3;
- встряхиватель (шейкер) вибрационный для пробирок орбитального типа движения с амплитудой встряхивания 3 мм и диапазоном скоростей от 150 до 2500 об/мин;
- встряхиватель (шейкер) переворачивающий орбитального типа, с адаптером для пробирок и диапазоном скорости от 20 до 100 об/мин;
- генератор азота высокой чистоты;
- измельчитель-гомогенизатор лабораторный погружной;
- камеру лабораторную морозильную с цифровым контроллером температуры и рабочим диапазоном температур от минус 15 °С до минус 25 °С;
- колонку хроматографическую длиной 150 мм, диаметром 2 мм, с обращено-фазным сорбентом С18 и диаметром частиц сорбента не более 5 мкм;
- компьютер с установленным программным обеспечением для управления масс-спектрометром и обработки результатов измерений, аттестованный в установленном порядке;
- систему высокоэффективную жидкостную хроматографическую, состоящую из бинарного насоса со смесителем, системы фильтрования и дегазации подвижных фаз, термостата хроматографическои колонки, обеспечивающего температуру нагрева до (50 ± 1) °С;
- систему получения деионизированной воды высокой чистоты с удельным сопротивлением 18 МОм · см;
- систему концентрирования растворителей, обеспечивающую поддержание температуры не менее (50 ± 1) °С;
- холодильник бытовой с цифровым контроллером температуры и рабочим диапазоном температур от 2 °С до 8 °С;
- центрифугу лабораторную рефрижераторную со скоростью вращения не менее 4000 об/мин и диапазоном температур от 4 °С до 20 °С с адаптерами для пробирок вместимостью 15 и 50 см3;
- центрифугу лабораторную с диапазоном скоростей от 300 до 15000 об/мин и адаптером для микроцентрифужных пробирок;
- шкаф сушильный с максимальной температурой нагрева не менее 110 °С и погрешностью поддержания заданной температуры не более 5 °С;
- пробы, подготовленные и проанализированные ранее в соответствии с требованиями разделов 7 и 8, в зависимости от типа исследуемой матрицы, в которых не выявлено наличие метаболитов карбадокса и олаквиндокса («чистые» пробы)*;
* Срок хранения «чистых» проб при температуре от минус 15 °С до минус 25 °С - не более трех месяцев.
- фильтры нейлоновые мембранные с порами диаметром от 0,2 до 0,45 мкм;
- виалы (флаконы) стеклянные вместимостью 2 см3 с завинчивающимися крышками и тефлоновы-ми прокладками 9 мм;
- колбы 1-10(50,1000)-2 по ГОСТ 1770;
- пипетки 2-2-1- 5(10) по ГОСТ 29227;
- пипетки одноканальные переменной вместимости 5 - 25, 20 - 100, 200 - 1000 мм3 с допустимой относительной погрешностью дозирования по метанолу и ацетонитрилу не более ±1 %;
- пробирки микроцентрифужные вместимостью 1,5 см3;
- пробирки полипропиленовые вместимостью 15 и 50 см3 с завинчивающимися крышками;
- цилиндры 1-500-1 по ГОСТ 1770.
(Поправка).
5.2 При определении остаточного содержания метаболитов карбадокса и олаквиндокса применяют следующие реактивы:
- азот газообразный марки 60 по ГОСТ 9293, ос. ч.;
- ацетон по ГОСТ 2603;
- ацетонитрил для ВЭЖХ-МС с массовой долей основного вещества не менее 99,9 %;
- воду деионизированную для ВЭЖХ, полученную с использованием системы производства ультрачистой воды из дистиллированной воды по ГОСТ 6709;
- кислоту муравьиную по ГОСТ 5848, ч. д. а.;
- метанол по ГОСТ 6995, х. ч.;
- н-гексан, х. ч.;
- кислоту сульфосалициловую с массовой долей основного вещества не менее 95 %;
- эфир этиловый уксусной кислоты (этилацетат) по ГОСТ 22300, ч. д. а.
5.3 При определении остаточного содержания метаболитов карбадокса и олаквиндокса в качестве образцов сравнения применяют следующие соединения:
1) для приготовления исходных растворов:
-1,4-бисдезоксикарбадокс с массовой долей основного вещества не менее 95,0 %;
- 3-метилхиноксалин-2-карбоновую кислоту с массовой долей основного вещества не менее 95,0 %;
- хиноксалин-2-карбоновую кислоту с массовой долей основного вещества не менее 97,0 %;
2) для приготовления исходных растворов внутренних стандартов:
- 1,4-бисдезоксикарбадокс-D3 с массовой долей основного вещества не менее 99,0 %;
- хиноксалин-2-карбоновую кислоту-D4 с массовой долей основного вещества не менее 97,0 %.
5.4 Допускается применение других средств измерений и посуды, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающим необходимую точность измерения, а также аппаратуры, реактивов и материалов по качеству не хуже вышеуказанных.
6 Подготовка к проведению измерений
6.1 Подготовка лабораторной посуды и реактивов
6.1.1 Мойку и сушку посуды проводят в отдельном помещении, оборудованном приточно-вытяжной вентиляцией. Для сушки лабораторной посуды и подготовки реактивов необходимо использовать отдельные сушильные шкафы.
6.1.2 Стеклянную посуду подвергают стандартной процедуре очистки лабораторной посуды с последующей последовательной промывкой органическими растворителями: этилацетатом (однократно), ацетоном (дважды).
6.1.3 Процедуру промывки органическими растворителями следует проводить в вытяжном шкафу. Рекомендуется на стадиях промывки использовать ультразвуковую баню. Окончательную сушку посуды проводят в сушильном шкафу, установленном в вытяжном шкафу, при температуре от 105 °С до 110 °С.
6.1.4 Каждую новую партию реактивов проверяют на отсутствие контаминации анализируемыми соединениями путем проведения холостого опыта в соответствии с процедурой анализа.
6.2 Приготовление растворов
6.2.1 Приготовление подвижных фаз А и Б
6.2.1.1 Приготовление подвижной фазы А
В мерную колбу вместимостью 1000 см3 приливают 500 см3 деионизированной воды, добавляют 1 см3 муравьиной кислоты и доводят объем раствора деионизированной водой до метки. Срок хранения раствора при комнатной температуре - не более 1 мес.
6.2.1.2 Приготовление подвижной фазы Б
В мерную колбу вместимостью 1000 см3 приливают 500 см3 метанола, добавляют 1 см3 муравьиной кислоты и доводят объем до метки метанолом.
Срок хранения раствора при комнатной температуре - не более 6 мес.
6.2.2 Приготовление 3 %-ного раствора сульфосалициловой кислоты
В мерную колбу вместимостью 1000 см3 вносят 30 г сульфосалициловой кислоты, добавляют 500 см3 деионизированной воды, перемешивают до полного растворения вещества и доводят до метки деионизированной водой.
Раствор используют свежеприготовленным.
6.2.3 Приготовление 0,5 %-ного раствора муравьиной кислоты
В мерную колбу вместимостью 50 см3 вносят 0,25 см3 муравьиной кислоты, доводят деионизированной водой до метки, перемешивают.
Срок хранения раствора при комнатной температуре - не более 1 мес.
6.3 Приготовление градуировочных растворов
6.3.1 Приготовление исходных стандартных растворов метаболитов карбадокса и олаквиндокса массовой концентрацией 1000 мкг/см3 (растворы С0)
Для приготовления исходных стандартных растворов С0 концентрацией 1000 мкг/см3 для каждого аналита рассчитывают необходимую массу i-го вещества, эквивалентную 10,0 мг анализируемого соединения, исходя из содержания основного вещества, по формуле
|
(1) |
где mi - масса навески i-го вещества, мг;
10 - требуемая масса чистого вещества, мг;
100 - коэффициент перевода процентов в относительное значение;
Рi - содержание основного вещества в аналитическом стандарте, %.
В мерные колбы вместимостью 10 см3 вносят по отдельности рассчитанные массы хиноксалин-2-карбоновой кислоты, 3-метилхиноксалин-2-карбоновой кислоты, 1,4-бисдезоксикарбадокса, добавляют по 5 см3 метанола, перемешивают и помещают в ультразвуковую баню на 5 мин, затем доводят до верхней метки метанолом.
Срок хранения растворов при температуре от минус 15 °С до минус25 °С - не более одного года. Перед применением растворы выдерживают при комнатной температуре в темном месте не менее 30 мин.
6.3.2 Приготовление рабочих стандартных растворов C1, С2, С3
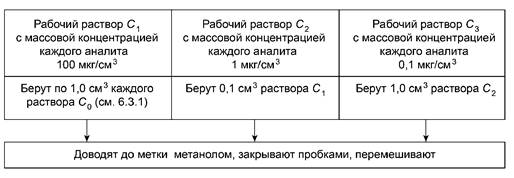
Рабочие растворы C1, С2, С3 готовят в мерных колбах вместимостью 10 см3 согласно рисунку 1.
Рисунок 1 - Приготовление рабочих растворов С1, С2, С3
Растворы C1, С2, С3 хранят при температуре от минус 15 °С до минус25 °С. Срок хранения раствора С1 - не более одного года, С2 - не более 6 мес, С3 - не более 3 мес.
Перед применением растворы выдерживают при комнатной температуре в темном месте не менее 30 мин.
6.3.3 Приготовление исходных растворов внутренних стандартов метаболитов карбадокса и олаквиндокса массовой концентрацией 1000 мкг/см3 (растворы D0)
Для приготовления исходных растворов внутренних стандартов D0 массовой концентрацией 1000 мкг/см3 для каждого аналита рассчитывают необходимую массу i-го вещества, эквивалентную 10,0 мг чистого вещества внутреннего стандарта, по формуле (1).
В мерные колбы вместимостью 10 см3 вносят по отдельности рассчитанную массу хиноксалин-2-карбоновой кислоты-D4 и 1,4-бисдезоксикарбадокса-D3, добавляют по 5 см3 метанола, перемешивают и помещают в ультразвуковую баню на 5 мин, затем доводят до верхней метки метанолом.
Срок хранения растворов при температуре от минус 15 °С до минус25 °С - не более одного года.
Перед применением растворы выдерживают при комнатной температуре в темном месте не менее 30 мин.
Внутренние стандарты для метаболитов карбадокса и олаквиндокса выбирают в соответствии с таблицей 1.
Таблица 1 - Соответствие между аналитами и внутренними стандартами
|
Наименование определяемого аналита |
Наименование внутреннего стандарта определяемого аналита |
|
Хиноксалин-2-карбоновая кислота |
Хиноксалин-2-карбоновая кислота-D4 |
|
3-Метилхиноксалин-2-карбоновая кислота |
|
|
1,4-Бисдезоксикарбадокс |
1,4-Бисдезоксикарбадокс-D3 |
6.3.4 Приготовление рабочих растворов внутренних стандартов D1, D2
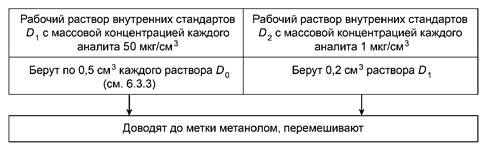
Рабочие растворы D1: D2 готовят в мерных колбах вместимостью 10 см3 согласно рисунку 2.
Рисунок 2 - Приготовление рабочих растворов внутренних стандартов D1, D2
Растворы D1, D2 хранят при температуре от минус 15 °С до минус 25 °С. Срок хранения раствора D1 - не более одного года, D2 - не более 3 мес.
Перед применением растворы выдерживают при комнатной температуре в темном месте не менее 30 мин.
6.3.5 Приготовление матричных градуировочных растворов G1 - G4
Матричные градуировочные растворы G1 - G4 готовят в полипропиленовых пробирках вместимостью 50 см3 из «чистых» проб массой 5,00 г, в которые вносят рабочий раствор внутренних стандартов D2 (см. 6.3.4) и рабочий раствор определяемых аналитов С3 (см. 6.3.2) объемом в соответствии с таблицей 2.
Таблица 2 - Приготовление матричных градуировочных растворов G1 - G4
|
Обозначение и массовая |
Концентрация в пересчете на исследуемый образец, мкг/кг |
Вносимый объем рабочего раствора, см3 |
|
|
С3 |
D2 |
||
|
G1 (2,5 нг/см3) |
0,5 |
0,025 |
0,1 |
|
G2(10 нг/см3) |
2,0 |
0,100 |
0,1 |
|
G3 (20 нг/см3) |
4,0 |
0,200 |
0,1 |
|
G4 (40 нг/см3) |
8,0 |
0,400 |
0,1 |
Пробирки встряхивают в шейкере 1 мин, выдерживают в темноте при комнатной температуре в течение 10 мин и проводят дальнейшую обработку проб согласно разделу 7, указанную на рисунке 3. Растворы G1 - G4 используют свежеприготовленными.
7 Отбор и подготовка проб
7.1 Отбор проб
7.1.1 Отбор проб мяса, печени, почек - по ГОСТ 7269.
7.1.2 Отбор проб мяса птицы, печени и продуктов из мяса птицы - по ГОСТ 31467.
7.1.3 Пробы, отобранные по 7.1.1, 7.1.2, при отсутствии возможности анализа в день отбора замораживают и хранят при температуре минус 25 °С до проведения анализа, но не более 90 сут.
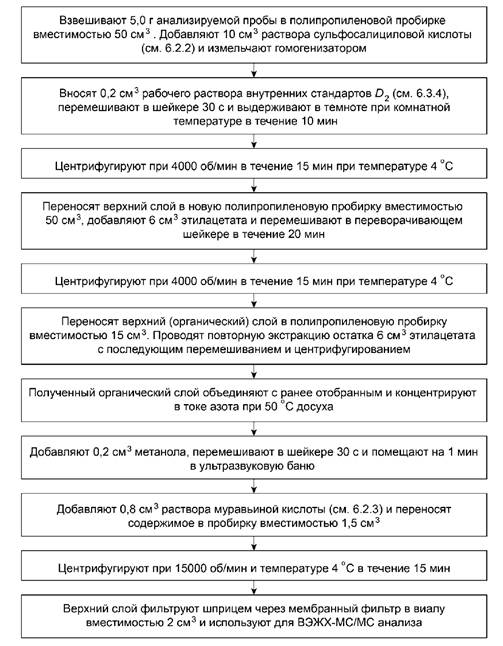
7.2 Подготовка проб мяса, печени, почек, включая мясо и печень птицы
Мышечную ткань предварительно очищают от грубой соединительной ткани. Обработку анализируемой пробы проводят в соответствии с рисунком 3.
Рисунок 3 - Подготовка проб мяса, печени, почек, включая мясо и печень птицы
8 Порядок выполнения анализа
8.1 Условия хроматографических измерений
8.1.1 Хромато-масс-спектрометр включают в соответствии с руководством (инструкцией) по эксплуатации и устанавливают параметры рабочих режимов масс-спектрометрического детектирования и хроматографического разделения.
8.1.2 Например, для колонки диаметром 2 мм, длиной 150 мм, с обращеннофазным сорбентом С18 с размером частиц не более 5,0 мкм соблюдают следующие условия хроматографирования:
- температура колонки - 40 °С;
- скорость потока подвижной фазы - 0,25 см3/мин;
- температура в отсеке устройства ввода проб - 10 °С;
- объем вводимой пробы - 40 мм3.
Разделение проводят в режиме градиентного элюирования (приготовление подвижных фаз А и Б по 6.2.1) в соответствии с таблицей 3.
Таблица 3 - Условия градиентного элюирования
|
Время, мин |
Подвижная фаза А, % |
Подвижная фаза Б, % |
|
0,0 |
100 |
- |
|
1,4 |
100 |
- |
|
37,0 |
30 |
70 |
|
37,1 |
100 |
- |
|
46,0 |
100 |
- |
8.1.3 Параметры воздействия на ионы в режиме мониторинга множественных реакций (MRM) приведены в таблице 4.
Таблица 4 - Параметры воздействия на ионы в режиме MRM при ионизации электрораспылением с регистрацией положительных ионов
|
Аналит |
Ион-предшественник m/z |
Ион-продукт m/z |
|
|
Хиноксалин-2-карбоновая кислота |
175 |
131 |
129 |
|
3-Метилхиноксалин-2-карбоновая кислота |
189 |
145 |
92 |
|
1,4-Бисдезоксикарбадокс |
231 |
199 |
143 |
|
Хиноксалин-2-карбоновая кислота-D4* |
179 |
133 |
151 |
|
1,4-Бисдезоксикарбадокс-D3* |
234 |
199 |
143 |
|
* Внутренний стандарт. |
|||
Примечание - Приведенные параметры хроматографического разделения и масс-спектрометрическо-го детектирования могут отличаться в зависимости от используемого оборудования.
8.1.4 Параметры настройки масс-спектрометрического детектора:
- температура источника - 500 °С;
- напряжение на распыляющем капилляре (IS) - 4500 В;
- разрешение квадруполей Q1/Q3 - единичное.
Примечание - Приведенные выше параметры хроматографического разделения и масс-спектрометрического детектирования могут отличаться в зависимости от используемой аппаратуры.
8.1.5 Контроль чувствительности хромато-масс-спектрометра осуществляют введением в инжектор хроматографа 40 мм3 градуировочных растворов G2 и G3 (см. 6.3.5) в зависимости от типа анализируемой матрицы. Полученное соотношение сигнал/шум для каждого аналита должно быть не менее трех к одному.
8.2 Построение градуировочной характеристики
Построение и расчет градуировочной характеристики проводят в каждой серии анализов с помощью программного обеспечения хромато-масс-спектрометра.
8.2.1 Проводят измерения не менее трех градуировочных растворов, приготовленных по 6.3.5, в порядке возрастания их концентраций.
8.2.2 Вычисление площади пика проводят для каждого иона-продукта анализируемых метаболитов карбадокса и олаквиндокса и их внутренних стандартов. Допускается проведение количественных измерений по одному, наиболее интенсивному, иону-продукту.
8.2.3 При построении градуировочной характеристики используют линейную регрессию (прямая должна проходить через ноль), при этом коэффициент корреляции должен быть не менее 0,98.
8.2.4 Построение линейного градуировочного графика и расчет концентрации метаболитов карбадокса и олаквиндокса в анализируемых пробах выполняется системой обработки данных в автоматическом режиме.
8.3 ВЭЖХ-МС/МС измерение
8.3.1 Для определения содержания аналитов проводят ВЭЖХ-МС/МС анализ в соответствии с руководством (инструкцией) по эксплуатации применяемого оборудования.
8.3.2 ВЭЖХ-МС/МС анализ выполняют в виде серии измерений, включающей следующие образцы:
- подвижную фазу А;
- «чистую пробу»;
- градуировочные растворы (см. 6.3.5);
- экстракты анализируемых проб, приготовленных по 7.2.
8.3.3 В инжектор хроматографа вводят 40 мм3 пробы, подготовленной в соответствии с разделом 7, и проводят измерения.
8.3.4 Определяют и регистрируют на хроматограмме время удерживания пиков двух ионов-продуктов каждого аналита, соответствующее времени удерживания, найденному при измерении градуировочных растворов.
9 Обработка результатов измерений
9.1 В соответствии с данными, полученными при анализе градуировочных растворов, проводят количественную обработку хроматограмм с использованием программного обеспечения, получая значения концентрации аналитов в анализируемой пробе.
9.2 Содержание i-го аналита Xi, мкг/кг, вычисляют по формуле
|
|
(2) |
где Сi - концентрация аналита в анализируемой пробе, найденная по градуировочному графику, нг/см3;
V - объем, до которого разбавлена проба, см3;
т - масса анализируемой пробы, г.
9.3 Расхождение результатов двух параллельных определений, выполненных в условиях повторяемости, не должно превышать предела повторяемости (сходимости) r, приведенного в таблице 5 при доверительной вероятности Р = 0,95. В случае превышения предела повторяемости г полученные результаты отбрасывают и вновь проводят параллельное измерение.
За окончательный результат содержания метаболитов карбадокса и олаквиндокса принимают среднеарифметическое значение результатов вычислений двух параллельных измерений, выполненных в условиях повторяемости, округленное до первого десятичного знака и выраженное в микрограммах на килограмм (мкг/кг).
10 Метрологические характеристики
Установленный в настоящем стандарте метод обеспечивает выполнение определения содержания метаболитов карбадокса и олаквиндокса с расширенной неопределенностью результатов аналитических измерений при коэффициенте охвата k = 2, указанной в таблице 5.
Таблица 5 - Показатели качества метода
|
Наименование аналита |
Диапазон измерений |
Значение относительной расширенной |
Показатель повторяемости (относительное стандартное отклонение повторяемости) Ur, % |
Показатель воспроизводимости (относительное стандартное отклонение воспроизводимости) UR, % |
Предел повторяемости r, % |
|
Хиноксалин-2-карбоновая кислота |
От 0,5 до 1,0 включ. |
64 |
15 |
31 |
42 |
|
Св. 1,0 до 8,0 включ. |
40 |
8 |
19 |
22 |
|
|
3-метилхиноксалин-2-карбоновая кислота |
От 0,5 до 1,0 включ. |
45 |
14 |
21 |
39 |
|
Св. 1,0 до 8,0 включ. |
40 |
11 |
17 |
30 |
|
|
1,4-бисдезоксикарбадокс |
От 0,5 до 1,0 включ. |
60 |
14 |
28 |
39 |
|
Св. 1,0 до 4,0 включ. |
35 |
8 |
15 |
22 |
|
|
Св. 4,0 до 8,0 включ. |
22 |
6 |
9 |
17 |
11 Оформление результатов измерений
Содержание i-го метаболита карбадокса или олаквиндокса, мкг/кг, представляют в виде
|
|
(3) |
где ![]() i - среднеарифметическое
значение результатов вычислений двух параллельных измерений содержания i-го аналита в анализируемой пробе по 9.2, мкг/кг;
i - среднеарифметическое
значение результатов вычислений двух параллельных измерений содержания i-го аналита в анализируемой пробе по 9.2, мкг/кг;
Ui - значение относительной расширенной неопределенности содержания i-го аналита для соответствующего диапазона измерений, % (в соответствии с таблицей 5).
12 Контроль стабильности результатов измерений
Контроль стабильности результатов измерений в пределах лаборатории осуществляют по ГОСТ ИСО 5725-6 с использованием контрольных карт Шухарта.
Ключевые слова: пищевые продукты, продовольственное сырье, остаточное содержание, метаболиты карбадокса и олаквиндокса, метод определения содержания с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием