Государственное санитарно-эпидемиологическое
нормирование
Российской Федерации
4.2.
МЕТОДЫ КОНТРОЛЯ. БИОЛОГИЧЕСКИЕ
И МИКРОБИОЛОГИЧЕСКИЕ ФАКТОРЫ
Методы лабораторного культивирования
трех видов иксодовых клещей группы
ricinus/persulcatus
Методические указания
МУК 4.2.1480-03
Минздрав
России
Москва 2004
1. Методические указания разработаны Институтом медицинской паразитологии и тропической медицины им. Е.И. Марциновского ММА им. И.М. Сеченова Минздрава России (Р.Л. Наумов, И.С. Васильева, Л.А. Ганушкина, В.П. Гутова, А.С. Ершова); Биологическим научно-исследовательским институтом санкт-петербургского университета (В.Н. Белозеров); Федеральным центром государственного санитарно-эпидемиологического надзора (Е.А. Арумова); Кафедрой паразитологии, паразитарных и тропических болезней ММА им. И.М. Сеченова (В.П. Сергиев, Е.А. Черникова).
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию при Министерстве здравоохранения Российской Федерации (протокол № 18 от 27 март 2003 г.).
3. Утверждены Главным государственным санитарным врачом Российской Федерации - Первым заместителем Министра здравоохранения Российской Федерации 29 июня 2003 г.
4. Введены впервые.
СОДЕРЖАНИЕ
|
УТВЕРЖДАЮ Главный
государственный санитарный _____________________________ Г.Г. Онищенко 29 июня 2003 г. Дата введения: 30 июня 2003 г. |
4.2.
МЕТОДЫ КОНТРОЛЯ. БИОЛОГИЧЕСКИЕ И
МИКРОБИОЛОГИЧЕСКИЕ ФАКТОРЫ
Методы
лабораторного культивирования трех видов
иксодовых клещей группы ricinus/persulcatus
Методические указания
МУК 4.2.1480-03
1. Область применения
1.1. Методические указания устанавливают методы культивирования и содержания клещей - переносчиков возбудителей болезней человека.
1.2. Методические указания предназначены для органов и учреждений государственной санитарно-эпидемиологической службы Российской Федерации, юридических лиц и индивидуальных предпринимателей, осуществляющих свою деятельность в установленном порядке по изучению клещей - переносчиков возбудителей зоонозов и средств борьбы с ними.
2. Общие положения
Клещи рода Ixodes служат важнейшими переносчиками вируса клещевого энцефалита и боррелий группы burgdorferi, а также эрлихий и бабезий. Для организации лабораторных экспериментов необходимо создание специальных эпизоотических моделей, важное место в которых занимает лабораторная культура переносчиков.
Известно, что многократное пассирование ряда возбудителей на питательных средах ведет к изменению у них некоторых важных свойств, вплоть до потери патогенности для теплокровных. Чтобы избежать этого, недопустимого для многих исследований явления, необходимо длительно содержать возбудителей в условиях, приближенных к естественным, то есть при пассировании по схеме: клещ → прокормитель → клещ → прокормитель. На любом этапе этого пассирования (из клеща или из теплокровного животного) можно взять для опыта материал, содержащий возбудителя и быстро нарастить необходимую для опыта биомассу за 2 - 3 пассажа на питательной среде или с использованием лабораторного животного. Для следующего опыта нужно снова брать материал из эпизоотической модели и снова накапливать возбудителя на подходящей среде, чтобы в любом опыте использовать возбудителей не более, чем после второго или третьего пассажей.
Таким образом, ведение эпизоотической модели и культуры клещей как ее основы для молекулярно-биологических исследований и изучения различных сторон эпизоотологии зоонозов представляется совершенно необходимым условием. При этом, модель должна соответствовать ряду необходимых требований. Среди них -массовость и жизнеспособность культуры клещей-переносчиков, максимальная длительность сохранения незаряженных и зараженных клещей, максимальный уровень зараженности клещей, минимальные трудозатраты на поддержание модели и минимальная ее стоимость. Важны также условия содержания и заражающего кормления клещей (вид хозяина, техника кормления), определяющие регламенты, а также трудовые и материальные затраты на создание и поддержание зараженной и незараженной лабораторной культуры переносчиков.
3. Особенности биологии трех видов клещей
р. Ixodes (Acarina, Ixodidae), важные для культивирования
К числу основных переносчиков возбудителей указанных выше зоонозов относятся три вида клещей - евроазиатские Ixodes ricinus и I. persulcatus и американский I. scapularis. Последний вид, хотя и не встречается в Евразии, но очень близок по экологическим параметрам к двум предыдущим и может стать очень удобным объектом для лабораторного культивирования и проведения экспериментов. Всем трем указанным видам клещей свойственны сезонно-циклические адаптации, выполняющие важнейшую роль в их приспособлении к сезонности климата. При культивировании клещей в лабораторных условиях эти адаптации создают серьезные помехи, обусловленные возникновением пассивного (покоящегося) состояния клещей, которое у голодных особей проявляется в отказе от нападения на хозяина и присасывания к нему (поведенческая диапауза), а у сытых - в виде длительных задержек развития или размножения (морфогенетическая и репродуктивная диапаузы).
Особенно богат спектр этих адаптаций у лесного клеща (I. ricinus). Ему свойственны: поведенческая диапауза личинок, нимф и имаго (отсутствие агрессивности с отказом присасываться к хозяину), морфогенетическая диапауза сытых личинок и нимф (задержка развития), репродуктивная диапауза сытых самок (задержка оогенеза) и яйцевая диапауза (задержка эмбриогенеза).
Таежный клещ (I. persulcatus) отличается от лесного отсутствием репродуктивной диапаузы самок и яйцевой (эмбриональной) диапаузы. Кроме того, у таежного клеща имагинальная поведенческая диапауза, возникающая после линьки, носит облигатный характер и поэтому преодолевается труднее, чем факультативная поведенческая диапауза лесного клеща.
Американский клещ I. scapularis, так же как и европейский лесной клещ I. ricinus, обладает репродуктивной диапаузой, но у него гораздо слабее, чем у двух других видов, выражена поведенческая диапауза (не только у имаго, но также у личинок и нимф). Это определяет большую по сравнению с двумя другими видами простоту его культивирования, хотя ему свойственна морфогенетическая диапауза сытых личинок и нимф.
Диапаузы у клещей существенно увеличивают срок развития от питания до линьки на каждой фазе, вызывая также повышение гибели клещей. Для достижения бездиапаузного развития или выведения клещей из диапаузы нужны специальные условия температуры и фотопериода (длины светового дня). Кроме специальных мер для получения бездиапаузного и максимально короткого срока развития клещей, большое значение имеют условия содержания, определяющие длительность их жизни на каждой фазе и сохранение естественных реакций. Оптимальные условия содержания клещей представлены в табл. 1.
Условия содержания клещей для максимального ускорения их
развития
(без диапауз)
|
№ |
Период |
Параметры |
I. persulcatus |
I. ricinus |
I. scapularis |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
1 |
Длительное содержание голодных имаго |
Температура, °С |
2 - 4 |
2 - 4 |
2 - 4 |
|
Длина светового дня |
темнота |
темнота |
темнота |
||
|
Длительность периода |
до года |
до года |
до года |
||
|
2 |
Содержание имаго перед питанием |
Температура, °С |
10 - 14 |
10 - 14 |
10 - 14 |
|
Длина светового дня, часы |
18 - 20 |
12 - 18 |
18 - 20 |
||
|
Длительность периода, сутки |
7 - 10 |
7 - 10 |
7 - 10 |
||
|
3 |
Содержание имаго во время питания |
Температура, °С |
18 - 20 |
18 - 20 |
18 - 20 |
|
Длина светового дня |
темнота |
темнота |
темнота |
||
|
Длительность периода, сутки |
7 - 11 |
7 - 11 |
7 - 11 |
||
|
4 |
Содержание имаго до окончания кладки |
Температура, °С |
18 - 20 |
18 - 20 |
18 - 20 |
|
Длина светового дня |
темнота |
темнота |
темнота |
||
|
Длительность периода, сутки |
30 - 40 |
30 - 40 |
30 - 40 |
||
|
5 |
Содержание кладки до вылупления |
Температура, °С |
18 - 20 |
18 - 20 |
18 - 20 |
|
Длина светового дня, часы |
18 - 20 |
18 - 20 |
18 - 20 |
||
|
Длительность периода, сутки |
30 - 40 |
30 - 40 |
30 - 40 |
||
|
6 |
Доразвитие личинок после вылупления |
Температура, °С |
18 - 20 |
18 - 20 |
18 - 20 |
|
Длина светового дня, часы |
18 - 20 |
18 - 20 |
18 - 20 |
||
|
Длительность периода, сутки |
10 - 15 |
10 - 15 |
10 - 15 |
||
|
7 |
Длительное содержание голодных личинок и нимф - как в п. 1 |
||||
|
8 |
Содержание личинок и нимф перед кормлением * |
Температура, °С |
18 - 20 |
18 - 20 |
18 - 20 |
|
Длина светового дня, часы |
18 - 20 |
18 - 20 |
18 - 20 |
||
|
Длительность периода сутки |
7 - 15 |
7 - 15 |
7 - 15 |
||
|
9 |
Содержание личинок и нимф во время питания |
Температура, °С |
18 - 20 |
18 - 20 |
18 - 20 |
|
Длина светового дня, часы |
18 - 20 |
18 - 20 |
18 - 20 |
||
|
Длительность периода, сутки |
5 - 6 |
5 - 6 |
5 - 6 |
||
|
10 |
Содержание сытых личинок и нимф до линьки |
Температура, °С |
18 - 20 |
18 - 20 |
18 - 20 |
|
Длина светового дня, часы |
18 - 20 |
18 - 20 |
18 - 20 |
||
|
Длительность периода, сутки |
60 - 90 |
60 - 90 |
60 - 90 |
||
|
11 |
Послелиночное доразвитие нимф и имаго |
Температура, °С |
18 - 20 |
18 - 20 |
18 - 20 |
|
Длина светового дня, часы |
18 - 20 |
18 - 20 |
18 - 20 |
||
|
Длительность периода, сутки |
10 - 15 |
10 - 15 |
10 - 15 |
||
|
12 |
Длительное содержание голодных нимф и имаго - как в п. 1 |
||||
|
* В связи со сложностью реакций нимф на фотопериод (длину дня), их, во избежание возникновения диапаузы, следует из режима длительного содержания перевести сначала на 2 недели в режим короткодневного фотопериода (12 часов света в сутки) и 18 - 20 °С, а затем перед кормлением выдержать в течение недели при длинно дневном фото периоде (см. строку 8). |
|||||
Все изложенные выше требования к культуре клещей, условиям ее ведения и содержания остаются актуальными и при использовании клещей для токсикологических экспериментов. Ниже излагаются методические приемы для создания и поддержания лабораторной культуры наиболее «трудного» для культивирования вида - таежного клеща - и приводятся некоторые сведения по двум другим указанным видам, если при их культивировании необходимо учитывать те эколого-биологические особенности, которые отличают их от таежного клеща.
4. Имаго клещей: кормление и получение потомства
В лабораторной культуре таежного клеща нимфы второго лабораторного поколения (F2) отличаются от нимф F1 меньшей активностью и меньшей агрессивностью по отношению к хозяину. Кроме того, при микроскопическом исследовании самцов F2 на наличие боррелий обнаружено, что более половины особей содержат дефектные проспермии, составляющие до 10 - 30 % от числа просмотренных. В природных популяциях дефектные проспермии встречаются единично и не более чем у 10 % самцов.
Учитывая столь существенные морфологические изменения и этологические отличия нимф и имаго второго лабораторного поколения, при постановке ряда поведенческих лабораторных экспериментов следует рекомендовать работу с клещами только первого лабораторного поколения. Возможно, это относится также и к двум другим видам клещей.
Для культивирования таежного клеща весной проводится сбор имаго на флаг в природе. Клещей обоего пола помещают в пробирку дифференцированной влажности, где их содержат при комнатной температуре до выпуска на хозяина. В пробирке происходит копуляция клещей, благодаря способности самок и самцов этого вида копулировать вне хозяина. Это избавляет от необходимости в лаборатории запускать на хозяина самок вместе с самцами, что облегчает процедуру (не присасывающиеся надолго самцы при манипуляциях с хозяином расползаются, что требует дополнительных мер предосторожности). Способность к копуляции у клещей проявляется очень рано - через несколько дней после линьки. Таким образом, при необходимости получить в лабораторных условиях неоплодотворенных самок, необходим ежедневный или через день просмотр линяющих нимф и разделение по разным пробиркам свежеперелинявших (светлоногих) самок и самцов. С этой же целью можно рекомендовать разделение свеженапитавшихся нимф - женских (более крупных) и мужских (более мелких), что почти предотвращает возможность копуляции самок и самцов после вылупления (метод разделения сытых нимф не безупречен, так как иногда среди самцов оказываются мелкие самки).
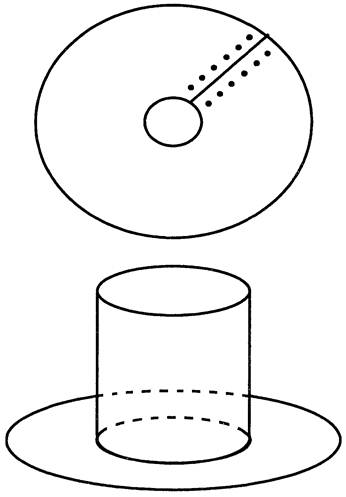
В качестве хозяина для самок клещей используется кролик или обыкновенный еж. При использовании кролика ему на спине выстригают шерсть и наклеивают сшитый из легкой хлопчатобумажной ткани цилиндр диаметром около 10 см и высотой около 15 см (рис. 1). Для удобства приклеивания к нижней части цилиндра подшивают плотным швом кольцо из такой же ткани шириной 1 - 1,5 см. Клей («Момент» или аналогичный быстро высыхающий клей) ровным слоем наносят на нижнюю сторону кольца и приклеивают к коже спины. На шею кролику надевают воротник в виде диска из легкой белой жести или пластиковый промышленного изготовления с отверстием посередине, который не позволяет ему содрать лапами наклейку с клещами. Наружный диаметр диска - 23 - 27 см, внутреннего отверстия - 6 - 7 см, в зависимости от размеров кролика. Внутренний и наружный края диска оклеивают пластырем во избежание травматизма. Диск разрезают по радиусу и вдоль радиального разреза по обеим его сторонам проделывают отверстия. Диск надевают на шею кролику, соединяя края радиального разреза внахлест и скрепляя их скрепками из мягкой проволоки, продевая их в заранее проделанные отверстия. После полного высыхания клея в матерчатый цилиндр запускают до 30 - 40 самок клещей, верхний край цилиндра подворачивают и закрепляют обхватом. Проверку состояния клещей проводят дважды в день, начиная с конца пятых суток, так как длительное (около суток) пребывание напитавшейся и отпавшей самки внутри цилиндра приводит к ее гибели от высокой температуры и низкой влажности под наклейкой в цилиндре. Сразу после окончания кормления клещей матерчатый цилиндр срезают настолько полно, насколько это позволяет не травмировать кожу. Оставшиеся части цилиндра срезают позже, когда они приподнимутся над кожей отрастающей шерстью.
При отсутствии кроликов, клещей можно кормить на ежах. Самое сложное в использовании ежей - это привязать их для напуска клещей. Для этого ежа кладут на стол и потихоньку сдвигают его назад, на край стола. Когда под задними лапами ежа не оказывается опоры, он опускает их и тогда один человек крепко берет его за заднюю лапу и оттягивает ее вниз, удерживая ежа на столе второй рукой в рукавице. Второй человек накидывает на ногу петлю из скрученного бинта. Такая же процедура повторяется со второй задней лапой. Затем за привязанные к задним лапам бинты осторожно приподнимают заднюю часть ежа и тогда он приподнимается на передних лапах. Быстрым и точным движением ежа берут за переднюю лапу и тоже набрасывают петлю из бинта. Такую же процедуру повторяют со второй передней лапой. Затем ежа, как и любое другое мелкое или среднее лабораторное животное, привязывают животом вверх к двойной крестовине, напоминающей букву «Н». Крестовину укладывают на кювету, которую помещают в емкость с водой, и на живот ежу выпускают клещей. Если клещи покидают ежа или собираются присосаться в неподходящем месте (на кончике морды, в ухе и т.д.), их возвращают на живот. Обычно клещи присасываются в течение 30 мин. Редко отдельные особи ползают, не присосавшись, до 40 мин. Когда клещи присосались, ежа освобождают от завязок, фиксировавших его на крестовине, и помещают в клетку или ящик с решетчатым дном или на решетку, которую прикрывают коробкой (в последнем случае удобно использовать пластиковый контейнер для мышей). Ящик или решетку помещают над емкостью с водой. Поскольку еж очень сильное животное, ящик следует закрывать крышкой с дополнительным грузом и коробку тоже придавливать грузом. В природе еж весом 800 - 1200 г способен одновременно прокармливать до сотни имаго и значительное число (сотни) нимф. В лаборатории на ежах при щадящем режиме выкармливают до 40 - 50 самок. Отход имаго клещей на ежах незначителен, не более 2 - 3 %. Самки хорошо напитываются, не хуже чем на кролике. Отпавших с ежа в воду самок промывают чистой водой, подсушивают на фильтровальной бумаге и помещают, как и самок с кролика, по одной в пробирку дифференцированной влажности. Длительность питания самок - 6 - 9 дней, отдельных особей - до 11 дней.
Наиболее простой метод получения напитавшихся самок, если позволяют условия, - сбор их во время дойки с коров, выпасаемых в лесах и на закустаренных пастбищах. При механизированных способах доения коров помещают на время дойки в тесные стойла, где их удобно осматривать. Напитавшихся клещей осторожно вытаскивают, выкручивая из кожи и стараясь не помять пальцами. Если клеща не выкручивать, а выдергивать, то часто хоботок остается в коже и клещ погибает.
Можно также собирать клещей с собак и с отловленных в природе ежей. В последнем случае ежей желательно выдерживать несколько дней над водой, как описано выше, чтобы паразитирующие на нем клещи нормально напитались.
Для кормления имаго использовали и других лабораторных животных - морских свинок, белых и хлопковых крыс и даже белых мышей. Однако этих животных следует использовать лишь в специальных целях. Для получения массовой культуры они неудобны.
Напитавшихся самок помещают по одной в пробирки и содержат при комнатной температуре (табл. 1). Самки ползают по стенкам пробирки в течение нескольких дней и затем начинают откладку яиц. Перед этим полезно поместить самку около фильтра, передним концом тела вниз. Тогда самка, совершая откладку яиц, отодвигается в сторону пробки и ее по окончании процедуры легко вынуть из пробирки, а не нарушенная кладка останется внизу в благоприятных условиях влажности. Кладки, отложенные в верхней части пробирки (ближе к пробке) часто полностью или частично высыхают. Среди разрушенных на отдельные куски кладок также резко возрастает гибель яиц. На теле откладывающей яйца самки появляются желто-белые пятна сначала на нижней стороне тела, а потом, увеличиваясь, переходят и на спинную сторону. К концу кладки площадь желтого пятна составляет около 70 % поверхности тела.
Начало и ход вылупления личинок из яиц контролируют под бинокулярной лупой. Вылупление личинок можно считать законченным, когда в пробирке имеются лишь темноокрашенные клещи, а свежевылупившихся личинок со светлыми ногами не удается обнаружить. От момента отпадения самки до окончания вылупления личинок при комнатной температуре проходит около двух месяцев. У лесного клеща этот период может растянуться на несколько месяцев в случае наступления яйцевой диапаузы.
Через 2 - 4 недели после окончания вылупления личинок (когда они покинули кладку и расползлись по пробирке) можно кормить на хозяине для получения следующей фазы - нимф. Лучшие результаты получаются, если личинок через 2 - 3 недели после окончания вылупления на 1 - 2 месяца поместить в холодильник (около 4 °С). В этих условиях они могут сохранять способность к присасыванию не менее 4 - 5 месяцев, а при удовлетворительном состоянии пробирок (наличие воды и отсутствие плесени) - до года. Столь длительное сохранение личинками жизнеспособности благоприятствует планированию опытов, освобождая экспериментатора от зависимости от времени года.
Ixodes ricinus. Этот вид отличается от таежного клеща наличием репродуктивной диапаузы сытых самок. Чтобы предотвратить диапаузу и тем самым сократить сроки откладки яиц и их последующего развития, самок необходимо содержать до питания в условиях короткого светового дня (12 ч света в сутки) при комнатной температуре. На напитавшихся самках фотопериод не сказывается. Для яйцекладки и развития яиц благоприятны температуры в пределах 15 - 25 °С. Все остальные процедуры и технические приемы - те же, что и для таежного клеща. Жизнеспособность и продолжительность жизни лесного клеща значительно выше, чем таежного, что дает ему преимущество при токсикологических экспериментах (лучшая выживаемость клещей в опытах как с лабораторными, так и с природными клещами).
Ixodes scapularis. Манипуляции с имаго I. scapularis почти ничем не отличаются от описанных для таежного клеща. Единственное отличие в том, что самцы этого вида, так же как и самцы лесного клеща, менее охотно, чем у таежного клеща, копулируют с самками вне хозяина. Поэтому вместе с самками на хозяина нужно выпускать и самцов. Длительность питания самок, сроки откладки яиц и вылупления личинок у этого вида практически не отличаются от таежного клеща.
5. Личинки и нимфы клещей: кормление, линька и содержание
5.1. Техника кормления личинок и нимф
Техника кормления и содержания личинок и нимф может быть различной в зависимости от целей и необходимого количества материала. При небольших количествах необходимого материала или в случаях, когда нужно подсчитать число напитавшихся (и заразившихся в ходе питания) клещей, удобнее всего использовать мышей (или других мелких лабораторных животных - крыс, хлопковых крыс и др.). Для этого на мышей надевают воротник из тонкого, не очень жесткого картона или пластика. В последнем случае края отверстия оклеивают пластырем. Размеры воротника: диаметр - 5 см, диаметр внутреннего отверстия - 13 - 15 мм. Радиальный разрез позволяет изменять диаметр внутреннего отверстия путем большего или меньшего наложения краев разреза друг на друга. Наложенные друг на друга края воротника сшивают ниткой или тонкой мягкой проволокой, скрепляют тугой скрепкой или соединяют липкой лентой. Мышей с воротником помещают в стеклянную банку объемом 0,8 - 1,0 л с дисками фильтровальной бумаги на дне. Личинок или нимф кисточкой переносят из пробирки или садка на спину мыши. Затем банку закрывают куском мельничного сита или мягкой мелкой металлической сеткой и закрепляют резиновым обхватом или мягкой (медной) проволокой. Иногда мыши прогрызают мельничное сито, закрывающее банку. Поэтому банку (банки) желательно накрывать поверх сита или марли металлической пластиной с небольшими отверстиями. Нередко личинки или нимфы после посадки на хозяина покидают его и расползаются по банке. Для повторного их наползания на хозяина и присасывания требуется несколько часов. Чаще всего это происходит, если клещи еще не переварили большую часть пищевого субстрата, оставшегося в кишечнике после линьки, или если культура клещей очень старая, малоактивная. Чтобы добиться присасывания максимального числа клещей, мышей в банках оставляют до утра следующего дня, а корм - кусочек белого хлеба (лучше - хлеб с отрубями) 2×2×2 см, смоченный водой, помещают в банку к концу первого дня, через 5 - 6 ч после выпуска на мышь клещей. Утром следующего дня мышей переводят в клетки из металлической сетки на ножках. Клетки устанавливают в кюветы с водой. Размер клеток: длина - 11 - 13 см, высота - 7 - 8 см. Размер ячеек сетки должен быть достаточным для свободного проползания напитавшихся нимф - не менее 4 мм. Сквозь верхнюю сторону клетки пропускают сосок стандартной поилки, совмещенной с пенициллиновым пузырьком.
5.2. Длительность питания клещей
При содержании мышей в режиме длинного светового дня личинки и нимфы, посаженные на мышь в 10 - 12 ч, начинают отпадать к вечеру третьего дня (личинки) или в начале четвертого дня (нимфы). При посадке клещей в понедельник максимум отпадения приходится на полуденные часы четверга и пятницы, а при посадке в пятницу - в понедельник и вторник. На пятый день (субботу или среду соответственно) остаются единичные особи. Обычно второй подъем отпадения (пятница или вторник) выражен значительно слабее первого, и средняя продолжительность питания личинок составляет 71 - 77 ч. Изредка второй подъем оказывается соизмерим с первым, и средняя длительность питания возрастает даже до 83 - 85 ч. Существенных различий в длительности питания личинок всех трех видов Ixodes не выявлено. Не обнаружено также связи между продолжительностью питания с одной стороны и временем года или числом питающихся на зверьке клещей - с другой. Совершенно определенно на длительность питания влияет место присасывания личинки или нимфы: клещи, присосавшиеся к кончику морды, ушам или хвосту питаются очень долго и, как правило, не могут полностью напитаться. На длительность питания влияет и температура в помещении. При понижении температуры длительность питания увеличивается.
Нимфы отпадают примерно в те же сроки, что и личинки, только вторая волна отпадения у них несколько выше и за счет этого несколько выше средняя продолжительность питания (79 - 80 ч, изредка - больше). Наличие двух «волн» отпадения напитавшихся личинок и нимф объясняется фотопериодической настройкой завершения ими питания в определенное время суток.
При необходимости получить большое число напитавшихся нимф или личинок удобно использовать ежа. На мышах весом 15 - 17 г может напитаться 300 - 500 личинок или 40 - 50 нимф, на мышах весом 20 г может напитаться до 700 - 800 личинок. Но при этих предельных значениях числа питающихся клещей часть мышей (около 10 %) может погибнуть от интоксикации. Особенно токсичен для мышей таежный клещ. Питание двух других видов, как правило, не приводит мышей к гибели. Вопрос о числе клещей, способных прокормиться на одном зверьке, важен потому, что у зверьков вырабатывается антитоксический («противоклещевой») иммунитет и вторая партия клещей обычно хуже питается и слабее накармливается. Поэтому лабораторных животных желательно использовать для кормления клещей однократно или с большим перерывом между двумя кормлениями, что не всегда удобно.
На еже весом 1,0 - 1,5 кг может напитаться партия в 15 - 20 тыс. личинок или 1,5 - 2,0 тыс. нимф. Перед напуском клещей ежа помещают в сосуд высотой около 40 см, расположенный в кювете с водой. На дно сосуда предварительно укладывают 3 - 4 листа фильтровальной бумаги размером по диаметру дна сосуда. Клещей переносят на спину ежа кисточкой. Затем сосуд накрывают мельничным ситом, а сверху - сеткой или металлическим листом, фанерой, пластиком с отверстиями и придавливают грузом. Утром следующего дня ежа переносят в ящик с решетчатым дном или на решетку под ящик, как описывалось выше.
Темпы отпадения личинок и нимф и степень их насыщения на ежах примерно такие же, как и при питании на мышах. Для облегчения сбора клещей необходимо позаботиться о правильном питании ежа: у ежа не должно быть поноса (который, как правило, бывает после употребления молока), а в помете не должно быть крупных твердых частиц и шерсти. Лучше всего кормить ежа мясом. Кусок мяса привязывают шпагатом или мягкой проволокой и подвешивают в клетке так, чтобы он не касался пола. Ежу средних размеров достаточно 30 - 50 г мяса в сутки. Обязательно должна быть вода в чашке Петри или другой емкости. При сборе напитавшихся и отпавших клещей из воды сначала пинцетом извлекают помет, а затем воду с клещами выливают в маленький сачок из мельничного крупноячеистого сита и промывают струей воды комнатной температуры. Сачок кладут на фильтровальную бумагу для удаления лишней влаги и затем клещей переносят в садок (см. ниже).
5.3. Содержание клещей
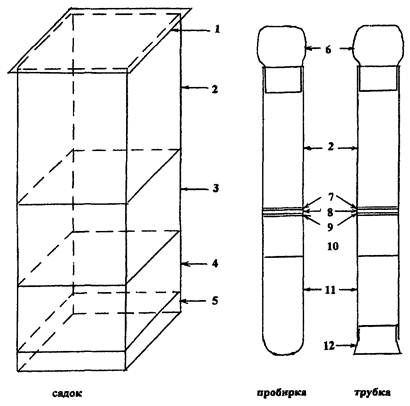
При работе с небольшими партиями клещей их удобнее содержать в пробирках дифференцированной влажности Нельзиной, в которых примерно треть объема заполнена дистиллированной или кипяченой водой, затем следует тугой ватный тампон, полностью погруженный в воду, тонкий слой промытого и прокаленного песка, тонкий слой ваты и фильтровальный диск (рис. 2). Вода не должна выступать над диском. Закрывают пробирку ватно-марлевой пробкой. Если опыты рассчитаны на длительное время, удобнее пользоваться не пробирками, а стеклянными трубками, нижний конец которых не запаян, как у пробирки, а плотно закрыт корковой или резиновой (не из черной резины!) пробкой. Вода со временем высыхает, и клещей из пробирок приходится пересаживать в новые. Если в пробирках находятся голодные личинки (из кладок), сделать это практически невозможно. В трубке же можно открыть пробку и добавить воды, не тревожа личинок. В пробирках (трубках) можно содержать голодных личинок из одной кладки, не более 200 сытых личинок или около 50 сытых нимф. Большее число клещей в пробирке создает немалые трудности. На фильтре накапливаются экскременты клещей, образуя черную липкую массу, к которой клещи прилипают и гибнут. На этом субстрате развивается плесень, что также приводит к увеличению отхода клещей. Пробирки (трубки) следует хранить в наклонном положении под углом 15 - 30°, чтобы вода в пробирке постоянно касалась тампона.
Наиболее эффективно и экономично содержание клещей в садках. Садки изготавливают из оргстекла толщиной 4 - 5 мм. Размеры - 5×5 см или более, высотой 15 - 20 см. Верхний край садка зашлифовывается так, чтобы к нему по всей поверхности стенок плотно прилегала крышка из стекла с закругленными на наждачной бумаге краями. К наружным поверхностям двух противоположных стенок чуть ниже их верхнего края приклеивается по два кусочка оргстекла со скошенным нижним краем. За эти выступы зацепляется 2 резиновых обхвата, которые придавливают стеклянную крышку. В дне садка просверливают отверстие диаметром 0,5 - 0,8 мм. Очень важно правильно заполнить садок. На дно насыпают мелкий промытый речной песок слоем 1,0 - 1,5 см. Затем идет слой уплотненного лесного перегноя толщиной около 2 см. Перегной лучше всего брать из ельников около комлей старых деревьев. Его слой располагается между почвой и верхним плохо перегнившим слоем опада. В перегное не должны быть видны не перепревшие иголки. Последний слой в садке - смесь того же перегноя с нарезанными стеблями сфагнума - до 5 - 6 см. Этот слой лишь слегка уплотняют. Через отверстие в дне садка в случае необходимости можно увлажнять субстрат, опуская садок на некоторое время в емкость с водой на глубину 1,5 - 2 см. Субстрат должен быть влажным, но не мокрым. Если в местах прикосновения частиц перегноя или сфагнума к стенкам садка собирается капельная влага, которая хорошо видна сквозь стекло при просмотре садка чуть сбоку и против света или в лупу, то садок нужно открыть и оставить для подсушивания. Когда лишняя влага будет удалена, в садок можно запускать клещей. Клещи очень быстро рассредоточиваются по садку. Первые 2 - 3 дня после отпадения с хозяина значительная часть клещей находится на стенках и крышке садка. Затем все они уходят в подстилку на глубину до 2 см, в редких случаях - до 5 см, где в положенный срок линяют. У свежеперелинявших клещей светлые ноги, которые постепенно темнеют. О завершении линьки можно судить по исчезновению в садке свежеперелинявших светлоногих клещей. За ходом линьки можно следить сквозь боковые стенки садка с помощью бинокулярной лупы. При развитии в садке отход клещей в 2 - 3 раза ниже, чем в пробирках, выше продолжительность их жизни. В нашей практике нимфы, содержавшиеся после линьки в садке в холодильнике, сохраняли жизнеспособность более года, не требуя от экспериментатора никаких усилий. Небольшая часть особей доживала до двух лет. Увлажнять садок приходится не чаще, чем раз в полгода. В садке площадью 5×5 см могут развиваться 3 - 4 тыс. напитавшихся личинок или около 500 нимф.
5.4. Сроки развития клещей
Знание сроков развития клещей важно для планирования длительных (многомесячных) опытов и планирования операций с культурой клещей для подготовки ее к нужному времени. Сроки развития клещей зависят от температуры. Оптимальная температура для их содержания 18 - 20 °С. Для ускорения процесса развития клещей температуру можно увеличить до 25 °С. Более высокая температура отрицательно сказывается на клещах. При температуре 23 - 25 °С половина личинок таежного клеща линяют к 40 дню, остальные - к 80, нимфы линяют на 10 - 15 дней позже.
I. scapularis развиваются чуть быстрее таежного клеща и у них такой же или чуть больший выход. Эти различия в значительной мере связаны с тем, что в партиях таежного клеща при любых ухищрениях оказывается большая или меньшая доля диапаузирующих личинок или нимф, что увеличивает средние сроки развития клещей и их гибель.
При массовом культивировании клещей, как уже говорилось выше, удобнее пользоваться садками. При меньшем суммарном объеме камер (пробирки занимают гораздо больше места, чем садки) и значительно меньших трудозатратах можно получить существенно больше клещей. У садков есть только один недостаток по сравнению с пробирками - в нем нельзя или очень трудно подсчитать перелинявших клещей. Но по числу активировавшихся и выползающих из подстилки на стенки садка нимф (которых изымали для опытов), можно утверждать, что потери клещей в садке не превышают 20 %.
6. Культивирование клещей в природе
Для проведения экспериментально-полевых исследований биологии клещей или эпизоотологии часто бывает необходимо использование большого числа особей местной популяции, развивавшихся в естественных условиях и с одинаковой историей развития. В природе собрать таких клещей не представляется возможным, поскольку природная популяция имаго состоит из особей нескольких (обычно трех) генераций, которые развивались по любому из четырех вариантов: без диапауз, с одной диапаузой - личиночной или нимфальной или с двумя диапаузами и имеют возраст от 3 до 5 или 6 (для лесного клеща) лет. Выходом из положения может быть создание специальных полевых садков - акарариумов, обеспечивающих поддержание необходимой культуры клещей.
Главный элемент акарариума - цилиндр диаметром до 50 - 80 см и высотой 70 - 80 см (обрезок стальной трубы с толщиной стенок 3 - 5 мм), который врезается в землю на глубину 7 - 10 см. Вместо цилиндра можно использовать элементы иной формы (квадрат, прямоугольник и пр.), согнутые из кровельного железа или других подручных материалов. Подбирая материал для этих цилиндров необходимо помнить, что конструкция должна сохраниться по крайней мере в течение 5 лет. Число цилиндров должно соответствовать числу вариантов культур клещей.
Площадку для акарариума выбирают в естественных местах обитания клещей. Цилиндры размещают под пологом леса, где хорошо развит травяной покров, но нет кустов, ветки которых касались бы стенок цилиндра или свешивались за его пределы. Если в течение сезона трава внутри цилиндра будет вырастать до его края, такую траву следует постричь. Цилиндры сверху оставляют открытыми. Во избежание выползания клещей из цилиндра верхний его край с внутренней стороны на ширину около 5 см смазывают клейким веществом, которое сохраняется липким в течение всего теплого периода (например, смола ЭД-20). Принято считать, что на значительную высоту поднимаются только имаго клещей, а личинки и нимфы находятся в приземном слое. Действительно, личинки в акарариуме обычно располагаются на высоте до 5 - 8 см, нимфы - до 20 см, но бывали случаи, когда нимфы в акарариуме в массе поднимались по траве и стенкам на высоту до 50 см и более. Какова бы ни была причина такой нетрадиционной активности, эти случаи показывают, что меры, препятствующие расползанию клещей, следует принимать не только в отношении имаго, но и нимф.
Сытых клещей, накормленных в лаборатории или собранных с животных, выпускают в цилиндр. В один цилиндр можно выпускать до 100 сытых самок, до 3000 сытых личинок или до 500 сытых нимф. Наличие нескольких цилиндров позволяет иметь одновременно культуру клещей на всех фазах развития, с разными сроками питания и продолжительностью развития. Сбор активных клещей в цилиндрах проводят акварельной кисточкой или маленьким флажком. Если личинок или нимф собирают для последующего кормления, то лучше их собирать сразу на мышь. Для этого мышь с надетым на нее воротничком держат за хвост и проводят ею несколько раз по траве около земли, каждый раз визуально контролируя число нападающих нимф, пока они держатся на поверхности шерсти. Если мышь просто выпустить в цилиндр, она может собрать столько клещей, что не сможет их выкормить и погибнет.
Цилиндры располагают в лесу в тени или полутени так, чтобы на них не падали долгое время прямые солнечные лучи. От повреждения зверем или скотом цилиндры защищают забором из проволоки или сетки. Но лучше цилиндры защищать от любых теплокровных животных, особенно если культуру клещей предполагается использовать для заражения патогенами. Для этого над цилиндрами устанавливают сварной или на болтах каркас из труб или уголка, заглубленный в землю не менее чем на 40 см. Каркас накрывают сеткой рабицей с ячеей 2 см и края сетки вкапывают на глубину 40 см. Сетка должна препятствовать проникновению в акарариум мелких млекопитающих и птиц. Дверь в акарариум должна запираться на замок.
Культивирование клещей в акарариуме не более трудоемко, чем в применявшихся ранее для этих целей садках, стеклянных трубках, мешочках из мельничного сита и пр. Кроме того, это единственный способ получить массовую одновозрастную природную культуру клещей, где каждая особь имеет возможность выбора своего микробиотопа и развитие которой не зависит от технических недоработок исследователя (при использовании садков, трубок, мешочков), его знаний и опыта.
Библиографические данные
1. Федеральный закон «О санитарно-эпидемиологическом благополучии населения» от 30 марта 1999 г. № 52-ФЗ.
2. Приказ МЗ РФ № 58 от 26.02.01 «Номенклатура основных паразитологических исследований в лабораториях ЦГСЭН».
3. СП 1.2.731-99 «Безопасность работы с микроорганизмами III - IV групп патогенности и гельминтами».
4. СанПиН 3.2.569-96 «Профилактика паразитарных болезней на территории Российской Федерации».
Приложение 1
Список материалов и оборудования, необходимых
для культивирования и содержания клещей
1. Вата.
2. Марля.
3. Фильтровальная бумага.
4. Бязь белая.
5. Быстро сохнущий клей (типа «Момент», БФ-2, БФ-6).
6. Нитки.
7. Иголки.
8. Мельничное сито.
9. Тонкий (0,3 - 0,5 мм) картон.
10. Вафельная ткань или белая байка для флагов.
11. Тонкая (0,2 - 0,3 мм) белая жесть.
12. Оргстекло толщиной 4 - 5 мм.
13. Дихлорэтан для изготовления клея для оргстекла.
14. Наждачная шкурка для шлифовки верхнего края садков.
15. Тонкая медная проволока (из телефонного провода).
16. Металлические листы или жесткий пластик с отверстиями, металлическая решетка или сетка (на каркасе).
17. Пластырь или другая липкая лента на тканевой основе.
18. Химические пробирки и (или) стеклянные трубки такого же размера.
19. Пенициллиновые пузырьки.
20. Поилки для лабораторных животных.
21. Глазные пинцеты, желательно с расклепанными (плоскими) концами бранш.
22. Акварельные кисточки № 1 (желательно колонковые).
23. Кюветы 18×24 см и 48×48 см.
24. Клетки из металлической сетки с ячеей 4 мм размером (11 - 13)×(7 - 8)×(7 - 8) см на ножках.
25. Стеклянные банки 0,8 - 1,0 л.
26. Стеклянные банки 10 - 30 л (для запуска личинок и нимф на ежей).
27. Клетка (ящик) с решетчатым дном для кормления имаго на ежах.
28. Виварные клетки для кроликов и мышей.
29. Реле времени для автоматического поддержания светового дня нужной длины.
30. Бытовой холодильник.
31. Сфагнум.
32. Лесной перегной.
Приложение 2
Рис. 1. Схема воротничка и матерчатого цилиндра.
Рис. 2. Схема емкостей для содержания клещей.
Условные обозначения:
1 - стеклянная крышка; 2 -
камера; 3 - слой перегноя со сфагнумом, 4 - 5 см;
4 - слой перегноя, 2 - 3 см; 5 - слой песка, 1,0 - 1,5 см; 6 - ватно-марлевая
пробка;
7 - фильтровальный диск; 8 - слой ваты, 1 - 2 мм; 9 - слой прокаленного песка,
до 1 мм;
10 - ватный тампон, 1,5 - 2,0 см; 11 - вода; 12 - резиновая пробка.