Государственное санитарно-эпидемиологическое нормирование
Российской Федерации
4.2. МЕТОДЫ КОНТРОЛЯ. БИОЛОГИЧЕСКИЕ И
МИКРОБИОЛОГИЧЕСКИЕ ФАКТОРЫ
Порядок
организации и проведения
лабораторной диагностики бруцеллеза
для лабораторий территориального,
регионального и федерального уровней
Методические
указания
МУК 4.2.3010-12
Москва 2013
1. Разработаны Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека (Е.Б. Ежлова, Н.Д. Пакскина); Федеральным казенным учреждением здравоохранения «Ставропольский научно-исследовательский противочумный институт» Роспотребнадзора (А.Н. Куличенко, Г.И. Лямкин, О.В. Малецкая, Т.В. Таран, С.И. Головнева, А.В. Ермаков, Г.А.-Х. Муртазалиева, Л.В. Ляпустина, Е.А. Манин, С.В. Вилинская): Федеральным казённым учреждением здравоохранения «Российский научно-исследовательский противочумный институт «Микроб» (И.Н. Шарова, Н.А. Осина, С.А. Щербакова, А.В. Топорков, В.В. Кутырев); Федеральным казённым учреждением здравоохранения «Иркутский ордена Трудового Красного Знамени научно-исследовательский противочумный институт Сибири и Дальнего Востока» (С.В. Балахонов, М.В. Чеснокова, А.И. Калиновский, Л.М. Михайлов, Н.Л. Баранникова); Федеральным казенным учреждением здравоохранения «Ростовский-на-Дону научно-исследовательский противочумный институт» Роспотребнадзора (Н.Н. Оноприенко, М.В. Цимбалистова, Н.В. Павлович): Федеральным казенным учреждением здравоохранения «Волгоградский научно-исследовательский противочумный институт» Роспотребнадзора (А.В. Липницкий, В.А. Антонов, В.П. Смелянский, О.В. Зинченко. В.В. Алексеев): ФБУН «Государственный научный центр прикладной микробиологии и биотехнологии» (И.А. Дятлов, Е.А. Тюрин, Л.В. Чекан); Федеральным казенным учреждением здравоохранения «Противочумный центр» Роспотребнадзора (С.М. Иванова, В.Е. Безсмертный); Федеральным бюджетным учреждением здравоохранения «Федеральный центр гигиены и эпидемиологии» Роспотребнадзора (В.В. Мордвинова, А.И. Верещагин).
2. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации Г.Г. Онищенко 29.03.2012 и введены в действие с момента утверждения.
3. Введены впервые.
СОДЕРЖАНИЕ
|
УТВЕРЖДАЮ Руководитель Федеральной службы Г.Г. Онищенко 29 марта 2012 г. Дата введения: 29 марта 2012 г. |
4.2. МЕТОДЫ КОНТРОЛЯ. БИОЛОГИЧЕСКИЕ И
МИКРОБИОЛОГИЧЕСКИЕ ФАКТОРЫ
Порядок организации и проведения
лабораторной диагностики бруцеллеза
для лабораторий территориального,
регионального и федерального уровней
Методические
указания
МУК 4.2.3010-12
1. Область применения
1.1. Настоящие методические указания определяют порядок организации и проведения лабораторной диагностики бруцеллеза для лабораторий территориального, регионального и федерального уровней, формы и методы их взаимодействия, номенклатуру и объем исследования, требования к лабораториям, специалистам и персоналу, участвующим в выполнении исследований, материально-техническому обеспечению исследований, к биологической безопасности проведения работ.
1.2. Настоящие методические указания предназначены для специалистов органов и учреждений, осуществляющих государственный санитарно-эпидемиологический надзор в Российской Федерации, специалистов противочумных учреждений, органов исполнительной власти субъектов Российской Федерации в области охраны здоровья граждан и медицинских организаций независимо от их организационно-правовой формы и формы собственности.
2. Нормативные ссылки
2.1. Федеральный закон от 30 марта 1999 г. № 52-ФЗ «О санитарно-эпидемиологическом благополучии населения».
2.2. Постановление Правительства Российской Федерации от 29 октября 2007 г. № 720 «О внесении изменений в пункт 5 Положения о лицензировании деятельности, связанной с использованием возбудителей инфекционных заболеваний, утвержденного постановлением Правительства Российской Федерации от 22 января 2007 г. № 31».
2.3. Постановление Главного государственного санитарного врача Российской Федерации от 24 февраля 2009 г. № 11 «О представлении внеочередных донесений о чрезвычайных ситуациях в области общественного здравоохранения санитарно-эпидемиологического характера».
2.4. Приказ Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека от 17 марта 2008 г. № 88 «О мерах по совершенствованию мониторинга за возбудителями инфекционных и паразитарных болезней».
2.5. Приказ Министерства здравоохранения и социального развития Российской Федерации от 7 июля 2009 г. № 415н «Об утверждении квалификационных требований к специалистам с высшим и послевузовским медицинским и фармацевтическим образованием в сфере здравоохранения».
2.6. СП 1.2.036-95 «Порядок учета, хранения, передачи и транспортирования микроорганизмов I - IV групп патогенности».
2.7. СанПиН 3.5.2528-09 «Гигиенические требования к размещению, устройству, оборудованию и эксплуатации больниц, родильных домов и других лечебных стационаров» Доп. 2 к СанПиН 2.1.3.1375-03.
2.8. СП 1.3.1285-03 «Безопасность работы с микроорганизмами I - II групп патогенности (опасности)».
2.9. СП 3.4.2318-08 «Санитарная охрана территории Российской Федерации».
2.10. Санитарно-эпидемиологические правила «Безопасность работы с микроорганизмами III - IV групп патогенности (опасности) и возбудителями паразитарных болезней». СП 1.3.2322-08.
2.11. СП 1.3.2518-09 «Безопасность работы с микроорганизмами III - IV групп патогенности (опасности) и возбудителями паразитарных болезней». Доп. и изм. 1 к СП 1.3.2322-08.
2.12. СанПиН 2.1.7.2790-10 «Санитарно-эпидемиологические требования к обращению с медицинскими отходами».
2.13. СП 3.1.7. 2613-10 «Профилактика бруцеллеза».
2.14. СП 1.3.2628-10 «Требования к организации работ с аэрозолями микроорганизмов I - II групп патогенности (опасности)». Изм. и доп. 1 к СП 1.3.1285-03.
2.15. МУ 3.1.7.1189-03 «Профилактика и лабораторная диагностика бруцеллеза людей».
2.16. МУ 4.2.2039-05 «Методы контроля. Биологические и микробиологические факторы. Техника сбора и транспортирования биоматериалов в микробиологические лаборатории».
2.17. МУ 3.3.2.2124-06 «Контроль диагностических питательных сред по биологическим показателям для возбудителей чумы, холеры, сибирской язвы, туляремии, бруцеллеза, легионеллеза».
2.18. МУК 4.2.2316-08 «Методы контроля бактериологических питательных сред».
2.19. МУ 1.3.2569-09 «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I - IV групп патогенности».
2.20. МУК 4.2.2495-09 «Определение чувствительности возбудителей опасных бактериальных инфекций (чумы, сибирской язвы, холеры, туляремии, бруцеллеза, сапа и мелиоидоза) к антибактериальным препаратам».
2.21. ГОСТ 9792-73 «Колбасные изделия и продукты из свинины, баранины, говядины и мяса других видов убойных животных и птиц. Правила приемки и методы отбора проб».
2.22. ГОСТ 21237-75 «Мясо. Методы бактериологического анализа».
2.23. ГОСТ 53430-2009 «Молоко и молочные продукты. Методы микробиологического анализа».
2.24. ГОСТ 26809-86 «Молоко и молочные продукты. Общие методы анализа».
2.25. ГОСТ Р ИСО 51448-99 (ИСО 3100-2-88) «Мясо и мясные продукты. Методы подготовки проб для микробиологических исследований».
2.26. ГОСТ Р ИСО 7218-2008 «Микробиология пищевых продуктов и кормов для животных. Общие требования и рекомендации по микробиологическим исследованиям».
2.27. ГОСТ Р 51447-09 (ИСО 3100-1-91) «Мясо и мясные продукты. Методы отбора проб».
2.28. Лабораторная диагностика опасных инфекционных болезней. Практическое руководство /Под ред. Г.Г. Онищенко, В.В. Кутырева.
2.29. Специфическая индикация патогенных биологических агентов. Практическое руководство /Под ред. Г.Г. Онищенко. М.: ЗАО «МП Гигиена».
3. Перечень сокращений
Г - гуанин
ГИСК - государственный институт стандартизации и контроля
ДНК - дезоксирибонуклеиновая кислота
ДТР - диагностический титр разведения
ИФА - иммуноферментный анализ
ЛПС - липополисахарид
МО - медицинская организация
м.к. - микробная клетка
МДа - мегадальтон
ME - международные единицы
мкм - микрометр
МПК - минимальная подавляющая концентрация
МУ - методические указания
МУК - методические указания по контролю
МФА - метод флуоресцентного анализа
ООН - особо опасные инфекции
ПБА - патогенный биологический агент
ПЦР - полимеразная цепная реакция
РА - реакция агглютинации
РИФ - реакция иммунофлуоресцении
РНАт - реакция нейтрализации антител
РНГА - реакция непрямой гемагглютинации
РК - реакция Кумбса
РХ - реакция Хеддльсона
РА - реакция агглютинации Райта
СанПиН - санитарно-эпидемиологические правила и нормативы
СП - санитарные правила
Тб - Тбилиси
т.п.н. - тысяч пар нуклеотидов
ФАО - FAO - Food and Agriculture Organization of the United Nations
Ц - цитозин
ЦНС - центральная нервная система
MLVA - мультилокусный анализ вариабельного числа тандемных повторов (VNTR)
4. Общие положения
4.1. Характеристика болезни и возбудителя бруцеллеза
Бруцеллез (Brucellosis) - острая или хроническая бактериальная инфекционно-аллергическая болезнь, общая для человека и животных, которая характеризуется интоксикацией и преимущественным поражением опорно-двигательного аппарата, нервной, сердечно-сосудистой, мочеполовой систем и других органов; затяжным течением, приводящим, как правило, к инвалидизации. Возбудитель бруцеллеза относится к роду Brucella, который входит в группу грамотрицательных, аэробных/микроаэрофильных палочек и кокков согласно схеме идентификации бактерий Берджи, принадлежит к семейству Brucellaceae порядка Rhizobiales класса Alphaproteobacteria. Бруцеллы являются факультативными внутриклеточными патогенами, вызывающими заболевание у большого числа животных и человека. Род Brucella состоит из 10 самостоятельных видов, различающихся по биохимическим, метаболическим, антигенным и вирулентным характеристикам: Brucella melitensis (3 биовара: преимущественно поражает коз и овец, возможна миграция на крупный рогатый скот и свиней), В. abortus (7 биоваров; вызывает аборты и орхиты у крупного рогатого скота), В. suis (5 биоваров; поражает свиней, зайцев, северных оленей, грызунов), В. neolomae (выделяется от пустынной кустарниковой крысы), В. ovis (вызывает эпидидимиты и орхиты у баранов, В. canis (поражает собак). Вновь зарегистрированные бруцеллы: В. ceti выделяются от китообразных, В. pinnipedialis - от ластоногих, В. microti - от серой полевки, В. inopinata - источник не установлен. Заболевания людей преимущественно вызывают В. melitensis, В. abortus и В. suis биовары 1 - 4, реже - В. canis.
Бруцеллез у людей протекает в виде системного поражения с вовлечением в процесс многих органов и систем и широким спектром симптомов. Болезнь начинается, как правило, с острой лихорадки с неспецифическими гриппоподобными проявлениями, склонна к хронизации и появлению осложнений в виде артритов, спондилитов, эндокардитов, менингитов, нейропатии, васкулитов, нефритов, лимфоаденопатии.
В соответствии с Международной статистической классификацией болезней и проблем, связанных со здоровьем (Десятый пересмотр. - Женева, 2003 г. МКБ-10) различают следующие формы бруцеллеза (А23):
- А23.0 Бруцеллез, вызванный Brucella melitensis;
- А23.1 Бруцеллез, вызванный Brucella abortus;
- А23.2 Бруцеллез, вызванный Brucella suis;
- А23.3 Бруцеллез, вызванный Brucella canis;
- А23.8 Другие формы бруцеллеза;
- А23.9 Бруцеллез неуточненный.
Большинство случаев заражения людей бруцеллезом происходит при непосредственном контакте с инфицированными животными, или при употреблении в пищу молочных продуктов, контаминированных бруцеллами. Бруцеллы обладают высокой инвазивностью и могут проникать через неповрежденные слизистые покровы, относятся к внутриклеточным паразитам, размножаются в полиморфно-ядерных лимфоцитах и макрофагах, но могут также находиться вне клетки.
Больной бруцеллезом человек, как источник инфекции, опасности практически не представляет, однако, отмечались редкие случаи инфицирования при пересадке костного мозга, переливании крови и половым путем.
Бруцеллы всех видов мало отличимы друг от друга по морфологическим признакам. Это микроорганизмы шаровидной, овоидной или палочковидной формы, расположены одиночно, парами, короткими цепочками, небольшими скоплениями. Спор не образуют, неподвижны. Окрашиваются всеми анилиновыми красителями, грамотрицательны.
Геном В. melitensis, В. abortus, В. oris, В. neotomae и В. suis биовара 1 представлен двумя кольцевыми молекулами ДНК размером 2100 и 1500 т.п.н. Оба репликона определяют метаболические и репликативные функции и, следовательно, являются хромосомами, а не плазмидами. В. suis биоваров 2 и 4 имеет две хромосомы размером 1850 и 1350 т.п.н., а В. suis биовара 3 - одну хромосому размером 3100 т.п.н. С хромосомой интегрированы фрагменты фаговой ДНК и мобильные генетические элементы - транспозоны. Молекулярная масса ДНК возбудителя бруцеллеза составляет 2,37×103 МДа с содержанием пар ГЦ 58 - 59 %. Плазмид у бруцелл не обнаружено.
Наиболее изучены геномы В. melitensis, В. abortus и В. suis, которые очень близки по структуре, организации и нуклеотидным последовательностям (гомология составляет более 99 %).
Основные факторы патогенности бруцелл: эндотоксин; фермент агрессии гиалуронидаза, низкомолекулярные протеины, ингибирующие фагосомо-лизосомальное слияние.
Бруцеллы нуждаются в сложных обогащенных питательных средах, характеризуются замедленным ростом, особенно в первых генерациях (5 - 10, а иногда 20 - 30 сут.). Стимулирует рост добавление нативной сыворотки крови, крови или 1 - 5 %-го глицерина. Оптимальные условия роста - рН 6,8 - 7,2, температура - 35 - 37 °С. Аэробы. В. ovis и первые генерации отдельных биоваров В. abortus при культивировании испытывают потребность в углекислоте (10 - 20 %).
Биохимическая активность бруцелл сравнительно невысока. Они расщепляют D-рибозу, аланин, глутамин, аспарагин; некоторые штаммы гидролизуют аминокислоты с образованием аммиака. Продуцируют уреазу (уровень ее продукции значительно колеблется в зависимости от вида возбудителя), липазу и амилазу (активность которых у возбудителя вида В. suis в 4 - 5 раз выше, чем у В. abortus и В. melitensis), каталазу, гиалуронидазу. Бруцеллы обладают адениндезаминазной активностью, которая в наибольшей степени выражена у представителей вида В. suis.
Для дифференциации бруцелл используют способность некоторых биоваров вырабатывать сероводород, а также чувствительность к бактериостатическому действию красителей (основного фуксина и тионина). Антигенная структура сложная и близкая для разных видов бруцелл. Два главных поверхностных антигена А и М имеют количественные видовые различия, их соотношение для В. melitensis составляет 1:20, для В. abortus, В. suis - 2:1.
Возбудитель бруцеллеза обладает общей для неспорообразующих бактерий устойчивостью к воздействию факторов окружающей среды, способен длительное время сохраняться в различных субстратах. Так, в молоке по данным разных авторов, бруцеллы способны сохраняться от 45 до 327 сут.; в масле, сливках, домашнем сыре - до 3 недель, в сливочном масле - более 4 недель, в простокваше, сметане - 8 - 15 сут., в брынзе - до 60 сут., в кумысе, шубате (сброженное верблюжье молоко) - до 3 сут.; в мясе - до 12 сут., а в замороженном виде - до 5 мес; во внутренних органах, костях, мышцах и лимфатических узлах инфицированных туш - в течение 1 мес. и более, в овечьей шерсти и смушках - от 1,5 до 4 мес. В естественных условиях во влажной почве и в навозе бруцеллы могут переживать свыше 2 мес.
Бруцеллы чувствительны к ультрафиолетовому излучению, действию прямых солнечных лучей и высоких температур: при температуре 100 °С погибают мгновенно, при 80 - 85 °С - через 5 мин, при 60 °С - через 30 мин. Сухой жар (90 - 95 °С) убивает бруцелл в течение часа. В то же время они довольно устойчивы к воздействию низких температур - сохраняют жизнеспособность при температуре минус 5 - 8 °С в течение 35 сут., а при минус 20 °С - в течение 20 сут.
Выраженной бактерицидной активностью по отношению к бруцеллам в течение 1 - 5 мин обладают растворы: сулемы (0,1 %-й); креолина (0,5 %-й); фенола (3 - 5 %-й); хлорамина (0,01 - 0,05 %-й); серной, соляной и азотной кислот (0,5 %-й); уксусной кислоты и формалина (0,2 %-й). Однако бруцеллы остаются невосприимчивыми к действию 5 %-го раствора борной кислоты в течение 60 мин; 1 - 2,5 %-х растворов карболовой кислоты в течение суток, свежегашеной извести в течение 2 ч.
Наибольшую антибактериальную активность по отношению к бруцеллам проявляют препараты тетрациклинового ряда, особенно доксициклин; рифампицин, хлорамфеникол; фторированные хинолоны - флероксацин, пефлоксацин, офлоксацин, ципрофлоксацин, ломефлоксацин, а также гентамицин, сизомицин, мономицин и другие аминогликозиды; беталактамный карбапенемный антибиотик меропенем; макролид азалидного ряда - азитромицин.
4.2. Лабораторная диагностика бруцеллеза
Лабораторная диагностика бруцеллеза включает проведение:
· диагностических исследований клинического материала для установления диагноза у лиц с подозрением на заболевание бруцеллезом. Клинический материал: кровь, сыворотка крови, спинномозговая жидкость, синовиальная жидкость (при артритах), моча, желчь, гной (при абсцессах), пунктаты костного мозга и лимфатических узлов;
· по эпидпоказаниям лабораторных исследований проб сырья животного происхождения (шерсть, кожа), продовольственного сырья (мясо и мясные продукты, молоко и молочные продукты) и объектов окружающей среды (почва, трава, фураж, подстилка, вода, смывы и т.д.).
Забор материала и лабораторное исследование материала от больных животных производят ветеринарные службы.
Для лабораторной диагностики заболевания у людей, выделения возбудителя, выявления ДНК бруцелл, антигенов возбудителя и антител к ним используют молекулярно-генетический метод (ПЦР), иммуносерологические методы (реакции агглютинации Хеддльсона, Райта, Кумбса, ИФА, РНГА), бактериоскопические методы (световая и люминесцентная микроскопия), бактериологические методы (выделение чистой культуры, её идентификация и межвидовая дифференциация штаммов), биологический метод (заражение биопробных животных), аллергологический метод (внутрикожная проба Бюрне, пробирочная реакция лизиса лейкоцитов).
Для лабораторной диагностики бруцеллеза, выявления ДНК и антигенов возбудителя в пробах продовольственного сырья, сырья животного происхождения, объектов окружающей среды используют молекулярно-генетический метод (ПЦР), иммуносерологические методы (ИФА, РНАт), бактериоскопические методы (световая и люминесцентная микроскопия), бактериологические методы (выделение чистой культуры, её идентификация и дифференциация штаммов), биологический метод (заражение биопробных животных).
Лабораторные исследования на бруцеллез проводят:
· на территориальном уровне - лаборатории медицинских организаций, филиалов ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации, ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации;
· на региональном уровне - Региональные центры по мониторингу за возбудителями инфекционных и паразитарных болезней II - IV групп патогенности в федеральных округах; Региональные центры по мониторингу за возбудителями инфекционных болезней I - II групп патогенности и Центры индикации и диагностики возбудителей опасных инфекционных болезней (противочумные учреждения, ГНЦ Роспотребнадзора);
· на федеральном уровне - Референс-центр по мониторингу за возбудителем бруцеллеза, Национальный центр верификации диагностической деятельности, осуществляющий функции государственной коллекции возбудителей особо опасных бактериальных болезней I - II групп патогенности Роспотребнадзора.
5. Порядок организации и проведения лабораторной диагностики бруцеллеза для лабораторий территориального уровня
5.1. Порядок организации и проведения лабораторной диагностики бруцеллеза для лабораторий медицинских организаций
5.1.1. Требования к лабораториям медицинских организаций, осуществляющим исследования на бруцеллез
Наличие разрешительных и регламентирующих работу документов
Лаборатории МО, осуществляющие исследования на бруцеллез, должны соответствовать установленным требованиям.
Учет, хранение, передача, транспортирование биологического материала, подозрительного на наличие возбудителя бруцеллеза, должны осуществляться в соответствии с действующими санитарными правилами.
Утилизация ПБА должна осуществляться в соответствии с действующими СанПиН по обращению с медицинскими отходами.
Проведение исследований на всех этапах: отбор проб, их хранение, транспортирование и передача, серологические исследования, взаимодействие с учреждениями Роспотребнадзора должны соответствовать требованиям настоящих МУК.
Требования к обеспечению безопасности работы персонала
Лаборатории медицинских организаций должны иметь пакет рабочих экземпляров нормативно-методической документации и инструкций, определяющих режим безопасной работы сотрудников с учетом характера работ, особенностей технологии, свойств микроорганизмов. Инструкции должны быть согласованы с комиссией по контролю соблюдения требований биологической безопасности, специалистами по охране труда, противопожарным мероприятиям и утверждены руководителем учреждения. Результаты проверок знаний правил техники безопасности персонала при проведении работ фиксируются в специальном журнале.
Все сотрудники обязаны выполнять требования по обеспечению безопасности работы с материалом, подозрительным или зараженным возбудителями инфекционных болезней III - IV групп патогенности (опасности), в соответствии с действующими нормативными документами.
Требования к специалистам и персоналу, участвующим в выполнении исследований на бруцеллез
Исследования на бруцеллез могут выполнять специалисты не моложе 18 лет с высшим и средним медицинским, биологическим образованием, окончившие соответствующие курсы профессиональной переподготовки с освоением методов безопасной работы с возбудителями инфекционных болезней III - IV групп патогенности (опасности), не имеющие противопоказаний к лечению специфическими препаратами и имеющие допуск к работе с ПБА III - IV групп на основании приказа руководителя учреждения. Специалисты, проводящие исследования на бруцеллез, должны иметь необходимые профессиональные навыки в соответствии с номенклатурой проводимых исследований (прилож. 1).
Специалисты, осуществляющие деятельность, связанную с использованием возбудителей инфекционных болезней, должны повышать квалификацию не реже одного раза в пять лет, и иметь сертификат специалиста (прилож. 2).
Порядок организации внутреннего контроля лабораторных исследований
Контроль качества работы в лабораториях МО реализуется через следующие контрольные процедуры:
· контроль качества отбора материала на исследование;
· контроль качества транспортирования материала;
· контроль качества оформления сопроводительной документации;
· контроль стерильности лабораторной посуды, дистиллированной воды;
· контроль качества диагностических препаратов и тест-систем, дезинфицирующих средств;
· контроль работы паровых и суховоздушных стерилизаторов;
· контроль работы бактерицидных облучателей;
· контроль температурного режима работы холодильников;
· контроль температурного режима работы термостатов;
· контроль качества приготовления рабочих растворов дезинфицирующих средств;
· проверку санитарного состояния помещений, включая условия уборки, контроль качества дезинфекции, контроль смывов с поверхностей и оборудования.
Результаты контроля фиксируют в специальных журналах.
Правила ведения документации
Ведение лабораторной документации, включая регистрационные и рабочие журналы, осуществляют ежедневно в соответствии с требованиями действующих методических документов.
Требования к материальным ресурсам, необходимым для выполнения диагностических исследований на бруцеллез
Для отбора материала и проведения диагностических исследований на бруцеллез в бактериологических лабораториях должны быть в наличии:
· диагностические препараты, тест-системы, транспортные питательные среды, зарегистрированные в установленном порядке (прилож. 3, 4, 5);
· химические реактивы (прилож. 7);
· приборы, оборудование, расходные материалы (прилож. 8, 9);
· комплект медицинский (укладка универсальная для забора материала от людей и из объектов окружающей среды для исследования на особо опасные инфекционные болезни).
Для проведения работ с микроорганизмами III - IV групп патогенности персонал лабораторий МО должен быть обеспечен спецодеждой и средствами индивидуальной защиты (в том числе для отбора проб клинического материала и проведения иммуносерологических реакций).
5.1.2. Номенклатура и объем исследований
МО осуществляют забор клинического материала от лиц с подозрением на бруцеллез, больных с любыми формами болезни, от лиц декретированных групп при диспансерном обследовании населения.
В лабораториях МО не проводят бактериологические диагностические исследования материала от больных с подозрением на бруцеллез.
В бактериологических лабораториях МО проводят исследования сывороток крови от больных бруцеллезом и вакцинированных против бруцеллеза лиц иммуносерологическими и аллергологическим методами:
1) выявление антител в парных сыворотках;
2) проведение реакции лизиса лейкоцитов.
Врач-инфекционист МО осуществляет оценку аллергологического статуса больных путем постановки аллергической пробы Бюрне.
5.1.3. Порядок работы при отборе материала для исследования на бруцеллез в медицинских организациях
Отбор и транспортирование проб клинического материала
Забор проб клинического материала для исследования, их упаковку и транспортирование осуществляет медицинский персонал в соответствии с требованиями действующих санитарных правил по безопасности работы с микроорганизмами I - II групп патогенности (опасности), по порядку учета, хранения, передачи и транспортирования микроорганизмов I - IV групп патогенности и методических указаний по профилактике и лабораторной диагностике бруцеллеза людей.
Клиническим материалом для отбора проб, предназначенных для дальнейшего исследования на бруцеллез, от лиц с подозрением на бруцеллез, больных людей в зависимости от клинической формы болезни являются: кровь, костный мозг, спинномозговая жидкость, пунктат из лимфоузлов, моча, желчь, суставная жидкость (при артритах), гной (при абсцессах).
Материал от больных с подозрением на бруцеллез забирают при поступлении больного до начала антибиотикотерапии.
При всех формах болезни берут кровь в объеме до 20 мл с учетом необходимости проведения бактериологических, серологических исследований и полимеразной цепной реакции (ПЦР).
Непосредственно у постели больного 10 мл крови засевают в две емкости с бифазной средой для выделения гемокультуры, или по 5 мл вносят иглой через предварительно обработанную спиртом резиновую пробку во флаконы с питательной средой жидкой для транспортирования материала и накопления бруцелл (прилож. 6), использование которой позволяет совместить этапы транспортирования материала в лабораторию и подращивания бруцелл.
Кровь для иммуносерологических исследований у больного берут натощак из локтевой вены в количестве 5 - 10 мл, соблюдая правила асептики, шприцем или с использованием вакуумной системы типа «Vakuette®» с активатором сыворотки. Шприцем кровь переносят в стерильную пробирку. Для получения сыворотки и предотвращения гемолиза пробирку с кровью оставляют при комнатной температуре в скошенном положении до образования сгустка. Полученную сыворотку отбирают в пластиковую пробирку, герметично закрывают и направляют в лабораторию для исследования на наличие специфических антител к возбудителю бруцеллеза.
Костный мозг получают путем пункции грудины шприцем с короткой и несколько затупленной иглой. Полученный костный мозг (в количестве нескольких капель) засевают в пробирку на питательные среды (см. посевы крови).
Спинно-мозговую жидкость отбирают после пункции поясничной, субокципитальной области или мозговых желудочков в количестве 0,1 - 0,3 мл и засевают на питательные среды (см. посевы крови).
Пробу мокроты, полученную в результате глубокого кашля, собирают в специальный стерильный одноразовый контейнер с завинчивающейся крышкой.
При исследовании мочи собирают её среднюю порцию (10 - 20 мл) в специальный одноразовый контейнер с завинчивающейся крышкой.
Пробы желчи (среднюю порцию) собирают при зондировании в процедурном кабинете. Над пламенем спиртовки открывают пробирку для сбора материала, полученную желчь (10 - 12 мл) помещают в одноразовую стерильную пробирку с завинчивающейся пробкой. При использовании стерильной стеклянной пробирки, закрытой газопроницаемой пробкой, после наполнения емкости обжигают горлышко и пробку в пламени спиртовки, закрывают пробирку. При использовании пробирки с газопроницаемой пробкой пробу доставляют в лабораторию в строго вертикальном положении, чтобы не замочить пробку желчью.
При обследовании больных, прошедших курс лечения антибиотиками, через 1 мес. и спустя 4 - 6 мес. после окончания курса антибиотикотерапии, а также больных хронической формой бруцеллеза в период обострения перед началом лечения рекомендуется проводить посевы крови, пунктатов костного мозга и лимфатических узлов на специальную питательную среду для выделения L-форм бруцелл (прилож. 6).
Материалом для исследования методом ПЦР являются: кровь, сыворотка крови, пунктат из лимфатических узлов, синовиальная жидкость. Забор, транспортирование и хранение биологического материала для проведения ПЦР осуществляют в соответствии с действующими методическими указаниями по организации работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I - IV групп патогенности.
Упаковка проб. Пробы для передачи в специализированные лаборатории упаковывают с соблюдением принципа тройной упаковки. Пробу (пробы) помещают в первичный контейнер (водонепроницаемый герметичный), который упаковывают в достаточное количество адсорбирующего материала на случай повреждения первичного контейнера. Вторичная упаковка (прочная, водонепроницаемая, герметичная) закрывает и защищает первичный контейнер (первичные контейнеры), упакованный в адсорбирующий материал. Вторичную упаковку помещают в наружную упаковку для транспортирования с достаточным количеством амортизирующего материала. Наружную упаковку опечатывают, маркируют необходимое положение груза стрелками или надписью «верх, осторожно». Недопустимо помещение сопроводительных документов в тару с пробами. Материал с направлением доставляют в специализированную лабораторию специально выделенным транспортом в сопровождении медицинского работника.
5.1.4. Оформление направления на исследование
На каждую направляемую в лабораторию пробу клинического материала заполняют направление в соответствии с прилож. 10. Направляемую пробу (пробы) сопровождают письмом на имя руководителя учреждения, в котором указывают вид направляемого материала и цель его исследования, количество образцов. Письмо подписывает руководитель направившего учреждения.
5.1.5. Порядок проведения лабораторных исследований на бруцеллез в медицинских организациях
Постановку и учет результатов внутрикожной аллергической пробы Бюрне у лиц, зараженных или подозрительных на зараженность бруцеллами, осуществляет врач-инфекционист МО в соответствии с инструкцией по применению аллергена бруцеллезного жидкого для внутрикожного применения (бруцеллина).
Постановку и учет иммуносерологических реакций проводят в лаборатории МО в соответствии с методическими указаниями по профилактике и лабораторной диагностике бруцеллеза людей.
5.1.6. Оформление результатов исследования
Регистрацию результатов серологического исследования на бруцеллез в бактериологических лабораториях МО осуществляют в соответствии с учетными формами, установленными в учреждении. Выдача ответов для историй болезней - по унифицированным формам.
5.1.7. Порядок взаимодействия медицинских организаций с учреждениями Роспотребнадзора
Информацию о положительных результатах серологического исследования на бруцеллез направляют в установленном порядке в соответствии с требованиями действующей нормативной документации.
Материал для бактериологических исследований на бруцеллез направляют в лабораторию особо опасных инфекций ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации. При её отсутствии материал направляют в Региональный центр по мониторингу за возбудителями инфекционных и паразитарных болезней II - IV групп патогенности, Региональный центр по мониторингу за возбудителями инфекционных болезней I - II групп патогенности или Центр индикации и диагностики опасных инфекционных болезней.
Если лаборатория МО не выполняет серологические исследования на бруцеллез, материал, подлежащий исследованию, направляют в филиал ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации или в ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации.
Передачу и транспортирование осуществляют в соответствии с действующими санитарными правилами по порядку учета, хранения, передачи и транспортирования микроорганизмов I - IV групп патогенности (опасности).
5.2. Порядок организации и проведения лабораторной диагностики бруцеллеза для филиалов ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации
5.2.1. Требования к лабораториям филиалов ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации, осуществляющим забор материала и исследования на бруцеллез
Наличие разрешительных и регламентирующих работу документов
Лаборатории филиалов ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации должны быть аккредитованы на техническую компетентность в соответствии с действующей законодательной базой Российской Федерации.
Лаборатории филиалов ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации должны соответствовать требованиям действующих нормативных документов по безопасности работ с микроорганизмами.
Учет, хранение, передача и транспортирование материала, зараженного или подозрительного на заражение бруцеллезом, утилизация отходов должны осуществляться в соответствии с действующими нормативными документами.
Требования к обеспечению безопасности работы персонала, порядок организации внутреннего контроля лабораторных исследований, правила ведения документации и требования к материальным ресурсам, необходимым для выполнения диагностических исследований на бруцеллез, аналогичны п. 5.1.1.
Требования к специалистам и персоналу, участвующим в выполнении исследований на бруцеллез
Исследования на бруцеллез могут выполнять специалисты не моложе 18 лет с высшим и средним медицинским, биологическим образованием, окончившие курсы профессиональной переподготовки по специальности «Бактериология» с основами безопасной работы с патогенными биологическими агентами (ПБА) III - IV групп, имеющие допуск к работе с ПБА III - IV групп на основании приказа руководителя учреждения.
Специалисты, осуществляющие деятельность, связанную с использованием возбудителей инфекционных болезней, должны повышать квалификацию не реже одного раза в пять лет.
5.2.2. Номенклатура и объем исследований
Лаборатории филиалов ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации осуществляют проведение серологических исследований материала от больных с подозрением на бруцеллез и при диспансерном обследовании населения декретированных групп, если лаборатория МО не выполняет данные исследования.
Специалисты филиалов ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации по эпидпоказаниям могут привлекаться специалистами ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации для сбора проб из объектов окружающей среды, продуктов животного происхождения, продовольственного сырья.
5.2.3. Порядок лабораторной диагностики бруцеллеза в лабораториях филиалов ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации
5.2.3.1. Отбор и транспортирование проб сырья животного происхождения и объектов окружающей среды.
Отбор проб сырья животного происхождения и объектов окружающей среды проводят с целью установления источника, факторов и путей передачи инфекции, условий, способствующих заражению, а также для организации и проведения санитарных мероприятий по локализации и ликвидации очага инфекции.
Специалисты филиала ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации, привлечённые к отбору материала, осуществляют его сбор, упаковку и транспортирование с соблюдением требований безопасности работы с материалом, заражённым или подозрительным на заражённость возбудителями I - II групп патогенности (опасности).
Отбор, упаковку и транспортирование проб полевого материала и сырья животного происхождения для лабораторного исследования на бруцеллёз осуществляют в соответствии с действующими санитарными правилами, методическими указаниями по организации работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I - IV групп патогенности, а также согласно действующим нормативным документам (ГОСТ) в зависимости от вида продукции.
Рекомендуется использовать для забора материала комплект медицинский (укладку универсальную для забора материала от людей и из объектов окружающей среды для исследования на особо опасные инфекционные болезни).
5.2.3.2. Проведение серологических исследований материала от больных с подозрением на бруцеллез
Исследование проводят в соответствии с п. 5.1.5.
5.2.4. Оформление направления на исследование
На каждую отправляемую в лабораторию пробу заполняют направление в соответствии с прилож. 11. Направляемую пробу (пробы) сопровождают письмом на имя руководителя учреждения, в котором указывают вид направляемого материала и цель его исследования, количество объектов. Письмо подписывает руководитель направившего учреждения.
Для проб шерсти и кормов дополнительно указывают происхождение, объем партии, вид упаковки и количество упаковочных единиц. К сопроводительному документу прилагают опись с указанием места отбора каждой пробы.
5.2.5. Оформление результатов исследования
Регистрацию результатов серологического исследования на бруцеллез в лабораториях филиалов ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации осуществляют в соответствии с п. 5.1.6.
5.2.6. Порядок взаимодействия филиалов ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации с учреждениями Роспотребнадзора
Материал из объектов окружающей среды для бактериологического исследования направляют в соответствии с требованиями действующей нормативной документации в лабораторию особо опасных инфекций ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации. При её отсутствии материал направляют в Региональный центр по мониторингу за возбудителями инфекционных и паразитарных болезней II - IV групп патогенности. Региональный центр по мониторингу за возбудителями инфекционных болезней I - II групп патогенности или Центр индикации и диагностики опасных инфекционных болезней. Передачу и транспортирование осуществляют в соответствии с действующими санитарными правилами по порядку учета, хранения, передачи и транспортирования микроорганизмов I - IV групп патогенности (опасности).
5.3. Порядок организации и проведения лабораторной диагностики бруцеллеза для лабораторий ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации
5.3.1. Порядок организации и проведения лабораторной диагностики бруцеллеза для ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации, в структуре которых отсутствуют отделы и лаборатории особо опасных инфекций
Порядок организации и проведения лабораторной диагностики бруцеллеза для лабораторий ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации, в структуре которых отсутствуют отделы или лаборатории особо опасных инфекций, соответствует порядку лабораторной диагностики бруцеллеза для лабораторий филиалов ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации (раздел 5.2).
5.3.2. Порядок организации и проведения лабораторной диагностики бруцеллеза для лабораторий особо опасных инфекций ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации
5.3.2.1. Требования к лабораториям особо опасных инфекций ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации, осуществляющим диагностические исследования на бруцеллез.
Наличие разрешительных и регламентирующих работу документов
Лаборатории ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации должны быть аккредитованы на техническую компетентность в соответствии с действующей законодательной базой Российской Федерации.
Лаборатории ООИ ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации, осуществляющие исследования на бруцеллез, должны соответствовать требованиям действующих нормативных документов по безопасности работ с микроорганизмами.
Требования к обеспечению безопасности работы персонала, правила учета, хранения, передачи и транспортирования выделенных подозрительных культур возбудителя бруцеллеза, деконтаминации и утилизации отходов, ведения документации аналогичны п. 5.2.1.
Требования к специалистам и персоналу, участвующим в выполнении исследований на бруцеллез
Исследования на бруцеллез могут выполнять специалисты не моложе 18 лет с высшим и средним медицинским или биологическим образованием, окончившие соответствующие курсы профессиональной переподготовки по специальности «Бактериология» с основами безопасной работы с патогенными биологическими агентами (ПБА) I - II групп, не имеющие противопоказаний к вакцинации против бруцеллеза, допущенные к работе с ПБА II - IV групп приказом руководителя учреждения. Необходимый уровень подготовки специалистов с высшим медицинским (биологическим) образованием и средним медицинским образованием представлен в прилож. 1.
Инженерно-технический персонал, дезинфекторы и препараторы проходят специальную подготовку по месту работы в соответствии с должностными обязанностями.
Специалисты, осуществляющие деятельность, связанную с использованием возбудителя бруцеллеза, должны повышать квалификацию не реже одного раза в пять лет (прилож. 2).
Порядок организации внутреннего контроля лабораторных исследований
Контроль качества диагностических исследований на бруцеллез в лабораториях ООИ ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации включает:
· контроль качества питательных сред, диагностических препаратов и тест-систем, эталонных штаммов, дисков с антибактериальными препаратами, дезинфицирующих средств, химических реактивов;
· проведение своевременной поверки средств измерений, аттестации испытательного оборудования;
· контроль стерильности лабораторной посуды, дистиллированной воды, растворов;
· контроль качества стерилизации паровых и суховоздушных стерилизаторов;
· контроль температурного режима холодильников;
· контроль температурного режима термостатов;
· контроль работы бактерицидных облучателей;
· контроль качества приготовления рабочих растворов дезинфицирующих средств;
· проверку состояния воздуха производственных помещений и боксов, температурного режима, влажности, давления;
· проверку санитарного состояния помещений, включая условия уборки, контроль качества дезинфекции, контроль смывов с поверхностей и оборудования.
Результаты контроля фиксируют в специальных журналах.
Требования к материальным ресурсам, необходимым для выполнения диагностических исследований на бруцеллез
Для проведения диагностических исследований на бруцеллез в бактериологических лабораториях должны быть в наличии:
· питательные среды, зарегистрированные в установленном порядке (прилож. 5, 6);
· диагностические препараты, антибактериальные препараты, зарегистрированные в установленном порядке (прилож. 3, 4, 12);
· химические реактивы (прилож. 7);
· приборы, оборудование (прилож. 8);
· расходные материалы (прилож. 9);
· комплект медицинский (укладка универсальная для забора материала от людей и из объектов окружающей среды для исследования на особо опасные инфекционные болезни);
· рабочая и защитная одежда, тип защитной одежды зависит от характера выполняемой работы.
5.3.2.2. Номенклатура и объем исследований.
Лаборатории ООИ ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации проводят:
· исследование материала от больных с подозрением на бруцеллёз;
· забор и исследование по эпидпоказаниям материала из объектов окружающей среды (почва, трава, фураж, подстилка, вода и т.д.), продовольственного сырья и продуктов животного происхождения.
Исследование материала от людей, из объектов окружающей среды, продовольственного сырья, продуктов животного происхождения проводят в зависимости от вида материала иммуносерологическими, молекулярно-генетическими (ПЦР), бактериоскопическими, бактериологическими (выделение чистой культуры и ее идентификация до вида), биологическими методами согласно действующим методическим указаниям по профилактике и лабораторной диагностике бруцеллеза людей и п. 5.3.2.3.
5.3.2.3. Порядок диагностических исследований на бруцеллез в лабораториях особо опасных инфекций ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации.
Исследование клинического материала на бруцеллез включает:
· иммуносерологическую диагностику;
· специфическую индикацию возбудителя или его маркёров (ДНК возбудителя инфекции, его антигенов) в исследуемом материале;
· выделение и идентификацию чистой культуры возбудителя бруцеллёза.
Порядок исследования клинического материал включает:
I этап
· прием, сортировка, регистрация и кодирование проб;
· первичная обработка проб и подготовка их к исследованию;
· ПЦР с пробами из нативного материала;
· постановка РНАт, ИФА для выявления специфических антигенов;
· постановка реакций агглютинации Хеддльсона и Райта, реакции Кумбса, РНГА, ИФА для выявления специфических антител в крови (сыворотки крови) больного;
· пересев клинического материала с питательной среды жидкой для транспортирования материала и накопления бруцелл на плотные и жидкие питательные среды (прилож. 5, 6);
· инкубация бифазной среды с посевом клинического материала при 37 °С до 20 - 30 сут.;
· заражение биопробных животных (морские свинки, белые мыши) подкожно в паховую область или внутрибрюшинно - при исследовании крови, спинномозговой жидкости, костного мозга.
II этап
8 мин от начала исследования - учет результатов реакции Хеддльсона.
2 - 6 ч от начала исследования - учет результатов ИФА, РНГА, РНАт.
8 - 10 ч от начала исследования - учет результатов ПЦР.
18 - 20 ч от начала исследования - учет результатов реакции агглютинации Райта.
48 ч от начала исследования:
· учет результатов реакции Кумбса;
· выдача предварительного положительного ответа на основании положительного результата ПЦР, положительных иммуносерологических реакций (РА, РК, РХ, РНГА, ИФА, РНАт).
III этап
3 - 21 сут. от начала исследования:
● учёт результатов роста на бифазной среде, плотных и жидких питательных средах;
● при наличии роста культуры (или единичных колоний) на питательных средах производят отбор колоний, сходных по морфологии с колониями возбудителя бруцеллеза;
● приготовление и микроскопия мазков в окраске по Граму из подозрительных колоний;
● отсев отобранных изолированных колоний на плотные питательные среды для получения чистой культуры;
![]() с материалом из подозрительных
колоний;
с материалом из подозрительных
колоний;
· постановка реакции слайд-агглютинации отобранных изолированных колоний с сывороткой бруцеллезной диагностической поливалентной для РА;
· подтверждение предварительного ответа на основании наличия характерного роста на плотных питательных средах, наличия в мазках из колоний мелких грамотрицательных кокковидных палочек, положительной реакции слайд-агглютинации, положительных результатов ПЦР и МФА с материалом из подозрительных колоний.
IV этап
5 - 30 сут. от начала исследования:
· пересев чистых культур на скошенный агар для хранения и последующей работы с ними:
· определение степени диссоциации выделенных культур;
· постановка с культурами возбудителя бруцеллеза, находящимися в стабильной S-форме, тестов межвидовой дифференциации:
o отношение к избыточному содержанию углекислоты в воздухе;
o способность к образованию сероводорода;
o редуцирующая активность в отношении красителей (тионин, основной фуксин);
o агглютинация моноспецифическими бруцеллезными сыворотками (anti-abortus, anti-melitensis);
o чувствительность к бруцеллезному бактериофагу Тб;
· определение чувствительности к антибактериальным препаратам диско-диффузионным методом;
· вскрытие биопробных животных, посев органов и крови на плотные питательные среды:
o белых мышей через 20 - 25 сут., посев на питательные среды патологического материала: лимфатические узлы (паховый, аксиллярный, парааортальный, подчелюстной), кусочки органов (селезенки и печени);
o морских свинок через 30 - 35 сут., посев на питательные среды патологического материала: лимфатические узлы (регионарные в месте введения исследуемого материала, паховый, подчелюстной, шейный, парааортальный), кусочки органов (селезенка, печень, костный мозг), кровь;
· приготовление мазков-отпечатков из органов биопробных животных, постановка МФА;
· постановка ПЦР (суспензия из гомогената органов, лимфатических узлов, костный мозг, сыворотка крови);
· постановка слайд-агглютинации и реакций агглютинации Хеддльсона и Райта;
· учет результатов МФА, ПЦР, РА и слайд-агглютинации.
V этап
10 - 40 сут. от начала исследования:
· учет результатов дифференциации культур для определения вида и биовара возбудителя бруцеллеза;
· учет посевов материала от биопробных животных;
· выдача окончательного положительного ответа по результатам бактериологического исследования на основании выделения чистой культуры бруцелл из посевов нативного материала или от биопробных животных, или по результатам иммуносерологического и молекулярно-генетического исследований на основании положительных результатов иммуносерологических и индикационных тестов.
36 - 60 сут. от начала исследования:
· завершение исследования и выдача окончательного отрицательного ответа проводятся на основании отсутствия специфического роста на питательных средах, отрицательных результатов ПЦР и иммуносерологических реакций на всех этапах исследования, отсутствия специфического роста в посевах от биопробных животных.
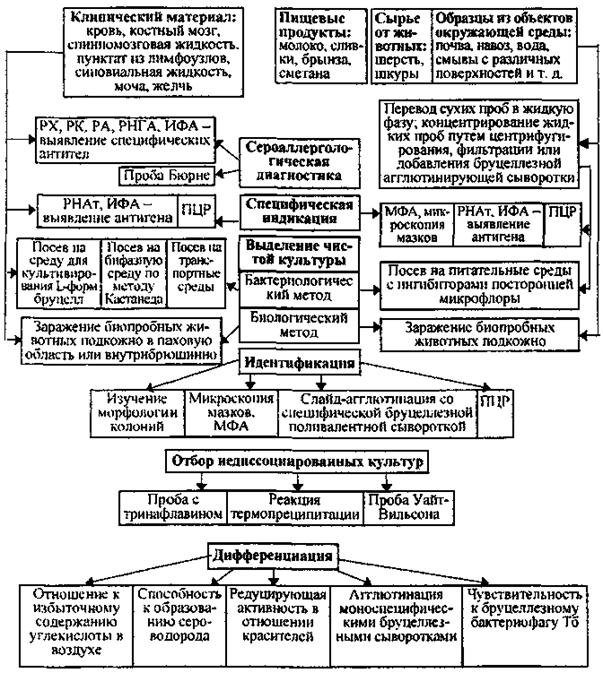
Исследование материала (по эпидпоказаниям) из объектов окружающей среды, продовольственного сырья, продуктов животного происхождения проводят в соответствии со схемой (рис. 1), которая отличается от аналогичной схемы исследования клинического материала наличием дополнительных этапов:
1) исследование нативного материала бактериоскопическим методом (световая и люминесцентная микроскопия);
Рис. 1. Схема лабораторной диагностики бруцеллеза
2) при бактериологическом методе исследования необходимо выполнить:
· перевод сухих проб в жидкую фазу (почва, пищевые продукты): суспендирование в 0,9 %-м растворе натрия хлорида или бульоне;
· концентрирование возбудителя в исследуемом материале путем центрифугирования проб при 3000 об./мин в течение 2 ч, фильтрации или добавления специфической бруцеллезной агглютинирующей сыворотки в соотношении 1:100;
· посев на плотные питательные среды с ингибиторами посторонней микрофлоры (генцианвиолет из расчета 1:200000, полимиксин - 3 мкг/мл и амфоглюкамин - 3 мкг/мл), не препятствующими росту бруцелл;
3) при биологическом методе исследования материала, контаминированного посторонней микрофлорой, заражение биопробных животных производят подкожно.
5.3.2.4. Регистрация и оформление результатов исследования
Регистрацию результатов анализа в лаборатории ООИ ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации производят в установленном порядке. Результаты исследования оформляют на бланке учреждения.
5.3.2.5. Порядок взаимодействия лабораторий особо опасных инфекций ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации с учреждениями Роспотребнадзора.
Информацию о выделенных и идентифицированных штаммах возбудителя бруцеллеза передают в Референс-центр по мониторингу за возбудителем бруцеллеза.
Штаммы возбудителя бруцеллеза, выделенные от людей, из объектов окружающей среды и идентифицированные в лаборатории ООИ ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации, для подтверждения видовой принадлежности передают в установленном порядке в Региональный центр по мониторингу за возбудителями инфекционных и паразитарных болезней II - IV групп патогенности, Региональный центр по мониторингу за возбудителями инфекционных болезней I - II групп патогенности или Центр индикации и диагностики возбудителей опасных инфекционных болезней. Для дальнейшего изучения и установления биоварной принадлежности штаммы по договоренности передают в Референс-центр по мониторингу за возбудителем бруцеллеза.
Передачу и транспортирование осуществляют в соответствии с действующими санитарными правилами «Порядок учета, хранения, передачи и транспортирования микроорганизмов I - IV групп патогенности». Прилагаются паспорт на штамм в одном экземпляре, сопроводительное письмо, акт упаковки и акт передачи.
6. Порядок организации и проведения лабораторной диагностики бруцеллеза для лабораторий регионального уровня
6.1. Порядок организации и проведения лабораторной диагностики бруцеллеза для лабораторий Региональных центров по мониторингу за возбудителями инфекционных и паразитарных болезней II - IV групп патогенности, курирующих субъекты Российской Федерации
Порядок организации и проведения лабораторной диагностики бруцеллеза для лабораторий Региональных центров по мониторингу за возбудителями инфекционных и паразитарных болезней II - IV групп патогенности, курирующих субъекты Российской Федерации, соответствует п. 5.3.2.
6.2. Порядок организации и проведения лабораторной диагностики бруцеллеза для лабораторий Региональных центров по мониторингу за возбудителями инфекционных болезней I - II групп патогенности и Центров индикации и диагностики возбудителей опасных инфекционных болезней
6.2.1. Требования к лабораториям Региональных центров по мониторингу за возбудителями инфекционных болезней I - II групп патогенности и Центров индикации и диагностики возбудителей опасных инфекционных болезней
Наличие разрешительных и регламентирующих работу документов, требования к специалистам и персоналу, участвующим в выполнении исследований на бруцеллез, требования к обеспечению безопасности работы персонала, порядок организации внутреннего контроля лабораторных исследований, правила ведения документации и требования к материальным ресурсам, необходимым для выполнения диагностических исследований на бруцеллез, аналогичны п. 5.3.2.1.
6.2.2. Номенклатура и объем исследований
Лаборатории Региональных центров по мониторингу за возбудителями инфекционных болезней I - II групп патогенности и Центров индикации и диагностики возбудителей опасных инфекционных болезней проводят:
· забор и исследование материала из объектов окружающей среды (почва, трава, фураж, подстилка, вода и т.д.), продовольственного сырья и продуктов животного происхождения по эпидпоказаниям;
· исследование материала от больных с подозрением на бруцеллез по эпидпоказаниям;
· идентификацию и межвидовую дифференциацию штаммов возбудителя бруцеллеза основными методами согласно действующим методическим указаниям по профилактике и лабораторной диагностике бруцеллеза людей.
6.2.3. Порядок диагностических исследований на бруцеллез в лабораториях Региональных центров по мониторингу за возбудителями инфекционных болезней I - II групп патогенности и Центров индикации и диагностики возбудителей опасных инфекционных болезней
Порядок исследования клинического материала, проб из объектов окружающей среды, а также штаммов, поступивших из лабораторий ООИ ФБУЗ «Центр гигиены и эпидемиологии» в субъекте Российской Федерации, соответствует п. 5.3.2.3.
6.2.4. Регистрация и оформление результатов исследования
Регистрацию результатов анализа в лаборатории Региональных центров по мониторингу за возбудителями инфекционных болезней I - II групп патогенности и Центров индикации и диагностики возбудителей опасных инфекционных болезней производят по учетным формам рабочей документации. Результаты исследования выдают на соответствующем бланке учреждения.
6.2.5. Порядок взаимодействия лабораторий Региональных центров по мониторингу за возбудителями инфекционных болезней I - II групп патогенности и Центров индикации и диагностики возбудителей опасных инфекционных болезней с учреждениями Роспотребнадзора
Информацию о выделенных и идентифицированных штаммах возбудителя бруцеллеза передают в Референс-центр по мониторингу за возбудителем бруцеллеза.
Штаммы возбудителя бруцеллеза, выделенные от людей, из объектов окружающей среды и идентифицированные в Региональных центрах по мониторингу за возбудителями инфекционных болезней I - II групп патогенности или Центрах индикации и диагностики опасных инфекционных болезней, направляют в Референс-центр по мониторингу за возбудителем бруцеллеза.
Передачу и транспортирование осуществляют в соответствии с действующими санитарными правилами «Порядок учета, хранения, передачи и транспортирования микроорганизмов I - IV групп патогенности». Прилагаются паспорт на штамм в одном экземпляре, сопроводительное письмо, акт упаковки и акт передачи живых культур.
7. Порядок организации и проведения лабораторной диагностики бруцеллеза для лабораторий федерального уровня
7.1. Порядок организации и проведения лабораторной диагностики бруцеллеза для Референс-центра по мониторингу за возбудителем бруцеллеза
7.1.1. Требования к лабораториям Референс-центра по мониторингу за возбудителем бруцеллеза
Наличие разрешительных и регламентирующих работу документов, требования к специалистам и персоналу, участвующим в выполнении исследований на бруцеллез, требования к обеспечению безопасности работы персонала, порядок организации внутреннего контроля лабораторных исследований, правила ведения документации и требования к материальным ресурсам, необходимым для выполнения диагностических исследований на бруцеллез, аналогичны п. 5.3.2.1.
7.1.2. Номенклатура и объем исследований
Лаборатории Референс-центра по мониторингу за возбудителем бруцеллеза проводят:
· полную идентификацию и изучение биологических, молекулярно-генетических, биохимических свойств недиссоциированных (S-форм) штаммов возбудителя бруцеллеза, в том числе с атипичными свойствами;
· генетическое титрование и секвенирование ДНК штаммов возбудителя бруцеллеза;
· исследование клинического, биологического материала, проб пищевых продуктов и образцов из окружающей среды по эпидемиологическим показаниям с учетом сложившейся эпизоотолого-эпидемиологической обстановки.
7.1.3. Организация и обеспечение диагностической деятельности при мониторинге за возбудителем бруцеллеза
Материалом для исследования служат штаммы возбудителя бруцеллеза, в том числе штаммы с атипичными свойствами, выделенные в лабораториях территориального и регионального уровней или в лаборатории Референс-центра.
При исследовании штаммов возбудителя бруцеллеза, в том числе с атипичными свойствами, используют весь комплекс современных высокотехнологичных методов бактериологического, иммуносерологического и молекулярно-генетического анализа, включая применение экспериментальных методов и серий препаратов.
Порядок исследования клинического материала, проб из объектов окружающей среды на бруцеллез соответствует п. 5.3.2.3.
Дополнительно проводят: изучение окислительно-метаболической активности, определение МПК антибиотиков, генотипирование, секвенирование ДНК выделенных штаммов.
Идентификацию и дифференциацию штаммов возбудителя бруцеллеза осуществляют по полной схеме:
· определение степени диссоциации культуры в пробе с трипафлавином реакции термопреципитации и Уайту-Вильсону;
· изучение морфологии колоний и характера роста на плотных питательных средах и характера роста в жидких питательных средах;
· изучение морфологии и тинкториальных свойств микробных клеток;
· проба с бруцеллезной поливалентной сывороткой (слайд-агглютинация, пробирочная агглютинация);
· отношение к избыточному содержанию углекислоты в воздухе;
· способность к образованию сероводорода;
· редуцирующая активность в отношении красителей (тионин, основной фуксин);
· агглютинация моноспецифическими бруцеллезными сыворотками (anti-abortus, anti-melitensis);
· чувствительность к бруцеллезному бактериофагу (Тб) и другим бруцеллезным бактериофагам;
· определение уреазной активности бруцелл;
· определение чувствительности к антибактериальным препаратам;
· определение генотипа выделенных штаммов методом MLVA;
· секвенирование фрагментов ДНК выделенных штаммов.
7.1.4. Порядок взаимодействия Референс-центра по мониторингу за возбудителем бруцеллеза с учреждениями Роспотребнадзора
Информацию о выделенных и/или идентифицированных штаммах возбудителя бруцеллеза (паспорта штаммов) направляют в Национальный центр верификации диагностической деятельности, осуществляющий функцию Государственной коллекции возбудителей особо опасных бактериальных инфекций I - II групп патогенности Роспотребнадзора.
Заключение о результатах идентификации присланного на исследование штамма направляют в учреждение, из которого штамм получен.
Штаммы возбудителя бруцеллеза, идентифицированные в лаборатории Референс-центра по мониторингу за возбудителем бруцеллеза, по запросу передают в Национальный центр верификации диагностической деятельности, осуществляющий функцию Государственной коллекции возбудителей особо опасных бактериальных инфекций I - II групп патогенности Роспотребнадзора.
Передачу и транспортирование осуществляют в соответствии с действующими санитарными правилами по порядку учета, хранения, передачи и транспортирования микроорганизмов I - IV групп патогенности. Прилагаются паспорт на штамм в одном экземпляре, сопроводительное письмо, акт упаковки и акт передачи.
7.2. Порядок организации и проведения лабораторной диагностики бруцеллеза для Национального центра верификации диагностической деятельности, осуществляющего функции государственной коллекции возбудителей особо опасных бактериальных инфекций I - II групп патогенности, Роспотребнадзора
7.2.1. Требования к лабораториям Национального центра верификации диагностической деятельности, осуществляющего функции государственной коллекции возбудителей особо опасных бактериальных инфекций I - II групп патогенности Роспотребнадзора
Наличие разрешительных и регламентирующих работу документов, требования к специалистам и персоналу, участвующим в выполнении исследований на бруцеллез, требования к обеспечению безопасности работы персонала, порядок организации внутреннего контроля лабораторных исследований, правила ведения документации и требования к материальным ресурсам, необходимым для выполнения диагностических исследований на бруцеллез аналогичны п. 5.3.2.1.
7.2.2. Номенклатура и объем исследований
Бактериологические лаборатории Национального центра верификации диагностической деятельности осуществляют:
· верификацию результатов диагностики бруцеллеза и идентификации штаммов, полученных из Региональных центров по мониторингу за возбудителями инфекционных болезней I - II групп патогенности. Центров индикации и диагностики опасных инфекционных болезней, Референс-центра по мониторингу за бруцеллезом;
· диагностические исследования материала от больных бруцеллезом по эпидпоказаниям;
· хранение коллекционных штаммов, охраноспособное и авторское депонирование.
7.2.3. Организация и обеспечение диагностической деятельности
Порядок исследования клинического материала, проб из объектов окружающей среды на бруцеллез соответствует п. 5.3.2.3 и 7.1.3.
7.2.4. Порядок взаимодействия лабораторий Национального центра верификации диагностической деятельности, осуществляющего функции государственной коллекции возбудителей особо опасных бактериальных инфекций I - II групп патогенности Роспотребнадзора с учреждениями Роспотребнадзора
Национальный центр верификации диагностической деятельности, осуществляющий функции государственной коллекции возбудителей особо опасных бактериальных инфекций I - II групп патогенности Роспотребнадзора направляет в Региональные центры по мониторингу за возбудителями инфекционных болезней I - II групп патогенности, Центры индикации и диагностики возбудителей опасных инфекционных болезней, Референс-центр по мониторингу за возбудителем бруцеллеза результаты проведенных исследований.
Приложение 1
1. Требования к знаниям и умениям специалистов медицинских организаций, выполняющих диагностические исследования на бруцеллез.
1) Врачи-бактериологи должны знать:
· основные положения эпидемиологического надзора за бруцеллезом, в том числе в части, касающейся исследования больных бруцеллезом людей;
· нормативные документы, регламентирующие проведение исследований на бруцеллез;
· требования биологической безопасности при работе с материалом, подозрительным на зараженность возбудителями III - IV групп патогенности, а также требования биологической безопасности при работе с материалом, подозрительным на зараженность возбудителем бруцеллеза (II группа патогенности);
· этапы подготовительной работы (подготовка питательных сред, диагностических препаратов, реактивов);
· требования к доставке клинического материала, его регистрации, хранению и уничтожению;
· этапы лабораторного исследования на бруцеллез;
· методы ускоренной диагностики бруцеллеза;
· сроки выдачи предварительного положительного результата исследования;
· правила и сроки передачи подозрительного клинического материала.
2) Врачи-бактериологи должны уметь:
· проводить комплексную сероаллергологическую диагностику бруцеллеза у людей, направленную на выявление антител в крови (пластинчатая реакция агглютинации Хеддльсона, объемная реакция агглютинации Райта, РНГА) или общую сенсибилизацию организма (реакция лизиса лейкоцитов);
· оценивать результаты вышеперечисленных реакций и вести соответствующую документацию.
3) Лаборанты, медицинские лабораторные техники и медицинские технологи должны знать:
· правила работы с материалом, подозрительным на зараженность возбудителями III - IV групп патогенности, а также с материалом, подозрительным на зараженность возбудителем бруцеллеза (II группа патогенности);
· этапы подготовительной работы (подготовку посуды, питательных сред, диагностических препаратов, реактивов);
· методы обеззараживания и подготовки материала для исследования;
· методы ускоренной диагностики бруцеллеза.
4) Лаборанты, медицинские лабораторные техники и медицинские технологи должны уметь:
· подготовить реактивы и диагностические препараты для серологических исследований;
· обеззараживать клинический материал и готовить его разведения для серологического исследования;
· ставить реакцию лизиса лейкоцитов;
· готовить отработанный материал для автоклавирования.
2. Требования к знаниям и умениям специалистов бактериологических лабораторий ФБУЗ «ЦГиЭ» и их филиалов, выполняющих диагностическое исследование на бруцеллез.
1) Врачи-бактериологи должны знать:
· основные положения эпидемиологического надзора за бруцеллезом, в том числе в части, касающейся сроков, объемов и контингентов, подлежащих обследованию на бруцеллез, а также сроков, объемов и видов исследуемых проб из продуктов и объектов окружающей среды;
· нормативные документы, регламентирующие проведение исследований на бруцеллез;
· требования биологической безопасности при работе с материалом, подозрительным на зараженность возбудителями III - IV групп патогенности, а также требования биологической безопасности при работе с материалом, подозрительным на зараженность возбудителем бруцеллеза (II группа патогенности);
· этапы подготовительной работы (подготовка питательных сред, диагностических препаратов, реактивов);
· требования к доставке материала для исследования на бруцеллез, его регистрации, хранению и уничтожению;
· этапы лабораторного исследования на бруцеллез;
· методы ускоренной диагностики бруцеллеза;
· сроки выдачи предварительного положительного результата исследования;
· правила и сроки передачи подозрительного на бруцеллез материала.
2) Врачи-бактериологи должны уметь:
· проводить комплексную сероаллергологическую диагностику бруцеллеза у людей, направленную на выявление антител в крови (пластинчатая реакция агглютинации Хеддльсона, объемная реакция агглютинации Райта, антиглобулиновая проба Кумбса, НМФА, РНГА, ИФА) или общую сенсибилизацию организма (реакция лизиса лейкоцитов);
· оценивать результаты вышеперечисленных реакций и вести соответствующую документацию.
3) Лаборанты, медицинские лабораторные техники и медицинские технологи должны знать:
· правила работы с материалом, подозрительным на зараженность возбудителями III - IV групп патогенности, а также с материалом, подозрительным на зараженность возбудителем бруцеллеза (II группа патогенности);
· этапы подготовительной работы (подготовку посуды, питательных сред, диагностических препаратов, реактивов);
· методы обеззараживания и подготовки материала для исследования;
· методы ускоренной диагностики бруцеллеза.
4) Лаборанты, медицинские лабораторные техники и медицинские технологи должны уметь:
· подготавливать реактивы и диагностические препараты для серологических исследований;
· обеззараживать клинический или иной материал и готовить его разведения для серологического исследования;
· ставить реакцию лизиса лейкоцитов;
· готовить отработанный материал для автоклавирования.
3. Требования к знаниям и умениям специалистов лабораторий ООИ ФБУЗ «ЦГиЭ», выполняющих бактериологическое исследование на бруцеллез.
1) Врачи-бактериологи должны знать:
· основные положения эпидемиологического надзора за бруцеллезом;
· нормативные документы, регламентирующие проведение исследований на бруцеллез;
· требования биологической безопасности при работе с материалом, подозрительным на зараженность возбудителями II - IV групп патогенности, а также требования биологической безопасности при работе с материалом, подозрительным на зараженность возбудителем бруцеллеза;
· этапы подготовительной работы (подготовка питательных сред, диагностических препаратов, реактивов);
· требования к доставке материала для исследования на бруцеллез, его регистрации, хранению и уничтожению;
· этапы лабораторного исследования на бруцеллез;
· методы ускоренной диагностики бруцеллеза;
· сроки выдачи предварительного положительного результата исследования;
· методы специфической индикации бруцелл;
· методы определения степени диссоциации;
· методы идентификации выделенных культур;
· культуральные, морфологические, иммуносерологические и биохимические свойства возбудителя бруцеллеза;
· методы внутриродового и внутривидового типирования (дифференциации) бруцеллезного микроба;
· методы идентификации L-форм бруцелл;
· правила и сроки передачи выделенных (подозрительных) культур;
· методы контроля качества питательных сред и ингибиторов посторонней микрофлоры;
· методы определения антибиотикочувствительности бруцелл.
2) Врачи-бактериологи должны уметь:
· проводить комплексную сероаллергологическую диагностику бруцеллеза у людей, направленную на выявление антител в крови (пластинчатая реакция агглютинации Хаддлсона, объемная реакция агглютинации Райта, антиглобулиновая проба Кумбса, НМФА, РНГА, ИФА) или общую сенсибилизацию организма (реакция лизиса лейкоцитов);
· осуществлять индикацию бруцелл в патологическом (клиническом) материале, материале из объектов окружающей среды и пищевых продуктов (микроскопия мазков, окрашенных по Грамму или Козловскому, МФА, ИФА, РНАт, ПЦР);
· осуществлять выделение подозрительных культур (посев на твердые и жидкие питательные среды, постановка биологической пробы);
· идентифицировать выделенные культуры возбудителя бруцеллеза (морфология колоний, микроскопия культуральных мазков, окрашенных по Грамму или Козловскому, МФА, проба с бруцеллезной поливалентной сывороткой, ПЦР);
· определять степень диссоциации культур возбудителя бруцеллеза (проба с трипафлавином, реакция термопреципитации, проба Уайт-Вильсона);
· осуществлять внутриродовое и внутривидовое типирование бруцеллезного микроба (отношение к избытку СО2, способность к образованию сероводорода, редуцирующая активность в отношении красителей, агглютинация моноспецифическими бруцеллезными сыворотками.
· чувствительность к бруцеллезным диагностическим бактериофагам, адениндезаминазная активность);
· определять антибиотикочувствительность выделенных культур;
· оценивать результаты вышеперечисленных исследований и вести соответствующую документацию.
3) Лаборанты, медицинские лабораторные техники и медицинские технологи должны знать:
· правила работы с материалом, подозрительным на зараженность возбудителями II - IV групп патогенности, а также с материалом, подозрительным на зараженность возбудителем бруцеллеза;
· этапы подготовительной работы (подготовку посуды, питательных сред, диагностических препаратов, реактивов);
· методы ускоренной диагностики бруцеллеза;
· методы специфической индикации бруцелл;
· методы идентификации выделенных культур;
· культуральные, морфологические, иммуносерологические и биохимические свойства возбудителя бруцеллеза;
· методы внутриродового и внутривидового типирования (дифференциации) бруцеллезного микроба;
· методы контроля качества питательных сред и ингибиторов посторонней микрофлоры.
4) Лаборанты, медицинские лабораторные техники и медицинские технологи должны уметь:
· подготовить к работе необходимые питательные среды;
· осуществлять посев поступившего подозрительного на бруцеллез материала на специальные среды;
· готовить ингредиенты для окраски мазков по Грамму и Козловскому;
· готовить мазки, фиксировать их и окрашивать по Грамму и Козловскому, а также флюоресцирующими иммуноглобулинами;
· подготавливать реактивы и диагностические препараты для серологических исследований;
· обеззараживать исследуемый материал и готовить его разведения для серологических тестов;
· ставить реакцию лизиса лейкоцитов;
· выполнять дифференциальные тесты с выделенными культурами (образование сероводорода, редуцирующая активность в отношении красителей, чувствительность к фагам и др.);
· проводить определение качества питательных сред;
· готовить отработанный материал для автоклавирования.
4. Требования к знаниям и умениям специалистов Региональных центров по мониторингу за возбудителями инфекционных болезней II - IV групп патогенности, Региональных центров по мониторингу за возбудителями инфекционных болезней I - II групп патогенности, Центров индикации и диагностики возбудителей опасных инфекционных болезней. Центра Минздрава России по бруцеллезу, Референс-центра по мониторингу за возбудителем бруцеллеза и Национального центра верификации диагностической деятельности, выполняющих бактериологическое исследование на бруцеллез.
1) Врачи-бактериологи должны знать:
· основные положения эпидемиологического надзора за бруцеллезом;
· вопросы организации лабораторных исследований на бруцеллез;
· нормативные документы, регламентирующие проведение исследований на бруцеллез;
· требования биологической безопасности при работе с материалом, подозрительным на зараженность возбудителями I - II групп патогенности;
· требования к доставке материала, его регистрации, хранению и уничтожению;
· этапы лабораторного исследования на бруцеллез;
· сроки выдачи ответов, правила и сроки передачи и хранения выделенных культур;
· этапы подготовительной работы (подготовка питательных сред, диагностических препаратов, реактивов);
· критерии оценки качества питательных сред, используемых для диагностики бруцеллеза;
· сероаллергологическую диагностику бруцеллеза;
· методы индикации и идентификации культур возбудителя бруцеллеза;
· культуральные, морфологические, иммуносерологические, биохимические и генетические свойства возбудителя бруцеллеза;
· методы определения степени диссоциации;
· методы внутриродового и внутривидового типирования (дифференциации) бруцеллезного микроба;
· методы генетического типирования штаммов бруцеллеза.
2) Врачи-бактериологи должны уметь:
· провести полное исследование поступившего материала по схеме лабораторной диагностики бруцеллеза;
· идентифицировать выделенные культуры возбудителя бруцеллеза;
· определять степень диссоциации культур возбудителя бруцеллеза (проба с трипафлавином, реакция термопреципитации, проба Уайт-Вильсона);
· осуществлять внутриродовое и внутривидовое типирование бруцеллезного микроба;
· определить эпидемическую значимость культур;
· осуществлять генетическое типирование штаммов бруцеллеза;
· определять антибиотикочувствительность выделенных культур;
· вести соответствующую документацию.
3) Лаборанты, медицинские лабораторные техники и медицинские технологи должны знать:
· правила работы с материалом, подозрительным на зараженность возбудителями I - II групп патогенности;
· этапы подготовительной работы (подготовку посуды, питательных сред, диагностических препаратов, реактивов);
· методы ускоренной диагностики бруцеллеза;
· методы специфической индикации бруцелл;
· методы идентификации выделенных культур;
· культуральные, морфологические, иммуносерологические и биохимические свойства возбудителя бруцеллеза;
· методы внутриродового и внутривидового типирования (дифференциации) бруцеллезного микроба;
· методы контроля качества питательных сред и ингибиторов посторонней микрофлоры.
4) Лаборанты, медицинские лабораторные техники и медицинские технологи должны уметь:
· подготовить к работе необходимые питательные среды;
· осуществлять посев поступившего подозрительного на бруцеллез материала на специальные среды;
· готовить ингредиенты для окраски мазков по Грамму и Козловскому;
· готовить мазки, фиксировать их и окрашивать по Грамму и Козловскому, а также флюоресцирующими иммуноглобулинами;
· подготавливать реактивы и диагностические препараты для серологических исследований;
· обеззараживать исследуемый материал и готовить его разведения для серологических тестов;
· выполнять дифференциальные тесты с выделенными культурами (образование сероводорода, редуцирующая активность в отношении красителей, чувствительность к фагам и др.);
· ставить реакцию лизиса лейкоцитов;
· проводить определение качества питательных сред;
· готовить отработанный материал для автоклавирования.
Приложение 2
|
Уровни |
№ п/п |
Бактериологические лаборатории |
Подготовка по ООИ в противочумных учреждениях (не менее 500 ч) |
Повышение квалификации по ООИ (72 - 500 ч) |
Другие виды подготовки (семинары по лабораторной диагностике бруцеллеза) |
Вакцинация против бруцеллеза |
||||
|
врачи |
лаборанты |
врачи |
лаборанты |
врачи |
лаборанты |
врачи |
лаборанты |
|||
|
Территориальный |
1 |
ЛПУ |
- |
- |
± |
± |
+ |
+ |
- |
- |
|
2 |
Филиалы ФБУЗ ЦГиЭ |
- |
- |
± |
± |
+ |
+ |
- |
- |
|
|
3 |
ФБУЗ ЦГиЭ (без лабораторий ООИ) |
- |
- |
± |
± |
+ |
+ |
- |
- |
|
|
4 |
ФБУЗ ЦГиЭ (с лабораторией ООИ) |
+ |
+ |
+ |
+ |
± |
± |
+ |
+ |
|
|
Региональный |
5 |
Региональные центры по мониторингу II - IV групп патогенности |
+ |
+ |
+ |
+ |
± |
± |
+ |
+ |
|
6 |
Региональные центры по мониторингу I - II групп патогенности и Центры индикации и диагностики |
+ |
+ |
+ |
+ |
± |
± |
+ |
+ |
|
|
Федеральный |
7 |
Референс-центр по мониторингу за бруцеллезом |
+ |
+ |
+ |
+ |
± |
± |
+ |
+ |
|
8 |
Национальный Центр верификации |
+ |
+ |
+ |
+ |
± |
± |
+ |
+ |
|
|
Условные обозначения: « + » - обязательный уровень подготовки; « - » - не требуется подготовка; « ± » - подготовка рекомендуется |
||||||||||