МИНИСТЕРСТВО ПРИРОДНЫХ РЕСУРСОВ И ЭКОЛОГИИ
РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральная служба по гидрометеорологии и мониторингу
окружающей среды (Росгидромет)
|
РУКОВОДЯЩИЙ ДОКУМЕНТ |
РД |
МАССОВАЯ КОНЦЕНТРАЦИЯ ФЕНМЕДИФАМА В ВОДАХ
Методика измерений газохроматографическим методом
Ростов-на-Дону
2012
Предисловие
1 РАЗРАБОТАН федеральным государственным бюджетным учреждением «Гидрохимический институт» (ФГБУ «ГХИ»)
2 РАЗРАБОТЧИК Л.В. Боева, канд. хим. наук
3 СОГЛАСОВАН с НПО «Тайфун» 09.02.2012
и УМЗА Росгидромета 02.04.2012
4 УТВЕРЖДЕН Заместителем Руководителя Росгидромета 03.02.2012
5 АТТЕСТОВАН ГУ ГХИ, свидетельство об аттестации методики измерений № 484.01.00175-2011 от 27.06.2011
6 ЗАРЕГИСТРИРОВАН ЦМТР ФГБУ НПО «Тайфун» за номером РД 52.24.484-2012 от 20.04.2012
7 ВЗАМЕН РД 52.24.484-95 «Методические указания. Методика выполнения измерений массовой концентрации фенмедифама в поверхностных водах суши газохроматографическим методом»
СОДЕРЖАНИЕ
Введение
Гербицид фенмедифам (бетанал, буретан, бурефен, кемифам, пистол) широко применяется в агрохимической практике для борьбы с сорными растениями, что обусловливает поступление этого гербицида в водные объекты с ливневым стоком с сельхозугодий и через атмосферу.
Химическое название фенмедифама - 3-[(метоксикарбонил)амино]-фенил-(3-метилфенил)карбамат, структурная формула
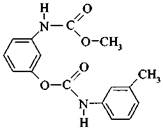
Из-за значительных объемов применения фенмедифам включен в приоритетный перечень пестицидов, подлежащих контролю в поверхностных водах.
Предельно допустимая концентрация (ПДК) фенмедифама для водных объектов хозяйственно-питьевого и культурно-бытового назначения - 2 мг/дм3, в воде водоемов (ГН 1.2.2701-10) - 0,05 мг/дм3; для водных объектах рыбохозяйстве иного назначения ПДК равна 0,0001 мг/дм3.
РУКОВОДЯЩИЙ ДОКУМЕНТ
МАССОВАЯ КОНЦЕНТРАЦИЯ ФЕНМЕДИФАМА В ВОДАХ
Методика измерений газохроматографическим методом
Дата введения - 2012-06-01
1 Область применения
1.1 Настоящий руководящий документ устанавливает методику измерений (далее - методика) массовой концентрации фенмедифама в пробах поверхностных вод суши в диапазоне от 10 до 300 мкг/дм3 включительно газохроматографическим методом.
1.2 Допускается выполнение измерений в пробах с массовой концентрацией фенмедифама, превышающей верхний предел указанного в 1.1 диапазона, при разбавлении экстракта в соответствии с 10.5.
1.3 Настоящий руководящий документ предназначен для применения в лабораториях, осуществляющих анализ природных и очищенных сточных вод.
2 Нормативные ссылки
В настоящем руководящем документе использованы ссылки на следующие нормативные документы:
ГОСТ 12.1.005-88 ССБТ. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 ССБТ. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 17.1.5.04-81 Охрана природы. Гидросфера. Приборы и устройства для отбора, первичной обработки и хранения проб природных вод. Общие технические условия
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ Р 51592-2000 Вода. Общие требования к отбору проб
ГН 1.2.2701-10 «Гигиенические нормативы содержания пестицидов в объектах окружающей среды»
МИ 2881-2004 Рекомендация. ГСИ. Методики количественного химического анализа. Процедуры проверки приемлемости результатов анализа
Примечание - Ссылки на остальные нормативные документы приведены в разделе 4.
3 Требования к показателям точности измерений
3.1 При соблюдении всех регламентируемых методикой условий выполнения измерений характеристики погрешности результата измерения с вероятностью 0,95 не должны превышать значений, приведенных в таблице 1.
Таблица 1 - Диапазон измерений, значения характеристик погрешности и ее составляющих при принятой вероятности Р = 0,95
|
Диапазон измерений массовых концентраций фенмедифама X, мкг/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости) σr, мкг/дм3 |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) σR, мкг/дм3 |
Показатель правильности (границы систематической погрешности) ± Δс, мкг/дм3 |
Показатель точности (границы погрешности) ± Δ, мкг/дм3 |
|
От 10 до 300 включ. |
0,4 + 0,08 ∙ X |
0,5 + 0,10 ∙ X |
0,4 + 0,07 ∙ Х |
1,0 + 0,20 ∙ Х |
При выполнении измерений массовой концентрации фенмедифама свыше 300 мкг/дм3 при соответствующем разбавлении экстракта, погрешность измерения не превышает значений, рассчитанных по приведенной в таблице 1 зависимости. Предел обнаружения фенмедифама составляет 4 мкг/дм3.
3.2 Значения показателя точности методики используют при:
- оформлении результатов измерений, выдаваемых лабораторией;
- оценке деятельности лабораторий на качество проведения измерений;
- оценке возможности использования результатов измерений при реализации методики в конкретной лаборатории.
4 Требования к средствам измерений, вспомогательным устройствам, реактивам, материалам
4.1 Средства измерений, вспомогательные устройства
4.1.1 Хроматограф газовый Кристалл 2000 М, Хроматэк-Кристалл 5000.2, Цвет-550, Цвет-800 или другой с термоионным или термоаэрозольным детектором.
4.1.2 Весы высокого (II) класса точности по ГОСТ Р 53228-2008, максимальная нагрузка не более 200 г, дискретность отсчета не более 0,0002 г.
4.1.3 Весы среднего (III) класса точности по ГОСТ 53228-2008, максимальная нагрузка не более 500 г, дискретность отсчета 0,001 г.
4.1.4 Термометр любого типа по ГОСТ 29224-91 с диапазоном измерения от 0 °С до 100 °С и ценой деления 1 °С.
4.1.5 Микрошприцы МШ-10М по ТУ 2-833-106-90-2 шт.
4.1.6 Государственный стандартный образец (ГСО) состава пестицида фенмедифама ГСО 7512-98, массовая доля основного вещества не менее 99 %.
4.1.7 Колбы мерные 2-го класса точности исполнения 2 по ГОСТ 1770-74 вместимостью: 25 см3 - 1 шт., 50 см3 - 1 шт.
4.1.8 Колбы мерные 2-го класса точности исполнения 2 или пробирки градуированные исполнения 2 с ценой деления 0,1 см3 по ГОСТ 1770-74 с притертыми стеклянными пробками вместимостью 10 см3 - 6 шт.
4.1.9 Пробирки градуированные исполнения 2 с ценой деления 0,1 см3 по ГОСТ 1770-74 с притертыми стеклянными пробками вместимостью 5 см3 - 5 шт.
4.1.10 Пипетки градуированные 2-го класса точности исполнения 1, 2 по ГОСТ 29227-91 вместимостью: 1 см3 - 4 шт., 2 см3 - 2 шт., 5 см3 - 1 шт.
4.1.11 Пипетка с одной отметкой 2-го класса точности исполнения 2 по ГОСТ 29169-91 вместимостью 5 см3 - 1 шт.
4.1.12 Цилиндры мерные исполнения 1, 3 по ГОСТ 1770-74 вместимостью: 25 см3 - 2 шт., 50 см3 - 2 шт., 500 см3 - 2 шт.
4.1.13 Колбы Кн исполнения 1, ТХС, по ГОСТ 25336-82 с притертыми стеклянными пробками вместимостью: 100 см3 - 10 шт., 1000 см3 - 1 шт.
4.1.14 Воронки делительные типа ВД исполнения 1, 3 по ГОСТ 25336-82 вместимостью 1000 см3 - 4 шт.
4.1.15 Воронки лабораторные, тип В, по ГОСТ 25336-82 диаметром 36 мм - 1 шт., 56 мм - 6 шт., 75 мм - 1 шт.
4.1.16 Стаканы, тип В, исполнения 1 по ГОСТ 25336-82, вместимостью: 50 см3 - 4 шт.; 600 или 1000 см3 - 5 шт.
4.1.17 Колонка газохроматографическая стеклянная с внутренним диаметром 3 мм и длиной 1 м.
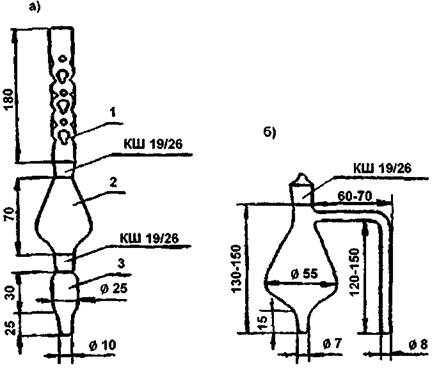
4.1.18 Устройство для концентрирования экстрактов (аппарат Кудерна-Даниша, см. рисунок 1а) - 6 шт., или колбы с Г-образным отводом вместимостью 100 см3 (см. рисунок 1б) - 6 шт., или испаритель ротационный ИР-1М по ТУ 25-11-917 - 1 шт.
а) аппарат Кудерна-Даниша (1 - дефлегматор, 2 - средняя часть аппарата, 3 - пробирка для сбора концентрата); б) колба с Г-образным отводом
Рисунок 1 - Устройства для концентрирования экстрактов
4.1.19 Эксикатор исполнения 2, диаметром корпуса 250 мм по ГОСТ 25336-82.
4.1.20 Склянка для промывания газов типа СПТ по ГОСТ 26336-82.
4.1.21 Установка из стекла группы ТС для перегонки растворителей (круглодонная колба типа К-1 с взаимозаменяемым конусом 29/32, вместимостью 1000 см3, дефлегматор длиной не менее 350 мм с взаимозаменяемыми конусами 19/26 и 29/32, насадка типа Н1 с взаимозаменяемыми конусами 19/26-14/23-14/23, холодильник типа ХПТ-1 длиной не менее 400 мм, алонж типа АИ с взаимозаменяемым конусом муфты 14/23) по ГОСТ 25336-82; термометр лабораторный стеклянный ТЛ-50 с взаимозаменяемым конусом КШ 14/23, длиной нижней части термометра 60 мм и диапазоном измерения температур от 0 °С до 100 °С, цена деления шкалы - 0,5 °С по ТУ 25-2021.007-88).
4.1.22 Стаканчики для взвешивания (бюксы) по ГОСТ 25336-82: СВ-14/8 - 1 шт., СН 85/15 - 2 шт.
4.1.23 Чашки выпарные № 4 или 5 по ГОСТ 9147-80 - 2 шт.
4.1.24 Пипетки Пастера по ТУ 9464-001-52876351-2000 - 2 шт.
4.1.25 Палочки стеклянные по ГОСТ 27460-87 диаметром 4 или 5 мм - 4 шт.
4.1.26 Ложки фарфоровые по ГОСТ 9147-80 № 1 и 2.
4.1.27 Посуда стеклянная для отбора проб и хранения растворов и реактивов вместимостью 25, 50, 500, 1000 см3.
4.1.28 Генератор водорода любого типа, вырабатывающий водород марки «А» по ГОСТ 3022-80.
4.1.29 Воздушный компрессор любого типа для питания детектора газового хроматографа или воздух газообразный по ГОСТ 9.010-80.
4.1.30 Микрокомпрессор аквариумный любого типа.
4.1.31 Насос вакуумный любого типа.
4.1.32 Муфельная печь с регулируемым нагревом любого типа.
4.1.33 Шкаф сушильный общелабораторного назначения.
4.1.34 Баня водяная любого типа.
4.1.35 Электроплитка по ГОСТ 14919-83.
Примечание - Допускается использование других типов средств измерений, посуды и вспомогательного оборудования, в том числе импортных, с характеристиками не хуже, чем у приведенных в 4.1.
4.2 Реактивы и материалы
4.2.1 Хроматон N-AW-DMCS (N-AW-HMDS или N-Super) или Хромосорб W-HP (фракция 0,125 - 0,16 мм или 0,16 - 0,20 мм) с 5 % нанесенной не подвижной фазы EGSP-Z или OV-210.
4.2.2 н-Гексан (далее - гексан) по ТУ 2631-003-05807999-98, х.ч.
4.2.3 Ацетон особой чистоты ОСЧ 9-5 по ТУ 2633-039-44493179-00.
4.2.4 Этиловый эфир уксусной кислоты (этилацетат) по ГОСТ 22300-76, ч.
4.2.5 Калий углекислый по ГОСТ 4332-76, ч.д.а.
4.2.6 Натрий сернокислый, безводный (сульфат натрия) по ГОСТ 4166-76, ч.д.а.
4.2.7 Кислота соляная по ГОСТ 3118-77, х.ч.
4.2.8 Универсальная индикаторная бумага рН 1-12 по ТУ 6-09-1181-76.
4.2.9 Азот нулевой, марка «А» по ТУ 6-21-39-96 или азот газообразный ос.ч. (1 сорт) по ГОСТ 9293-74.
4.2.10 Уголь активный БАУ-А по ГОСТ 6217-74.
4.2.11 Вода дистиллированная по ГОСТ 6709-72.
4.2.12 Стеклоткань или стекловата по ГОСТ 10146-74.
4.2.13 Вата медицинская по ГОСТ 5556-81.
4.2.14 Трубка из силиконовой резины с внутренним диаметром 5 или 6 мм.
Примечание - Допускается использование реактивов, изготовленных по другой нормативной и технической документации, в том числе импортных, с квалификацией не ниже указанной в 4.2.
5 Метод измерений
Выполнение измерений газохроматографическим методом основано на извлечении фенмедифама из предварительно очищенной гексаном пробы воды экстракцией этилацетатом и количественном его определении с азотселективным (термоионным или термоаэрозольным) детектором.
Идентификацию фенмедифама осуществляют по времени его удерживания; расчёт концентрации проводят по соотношению высот или площадей хроматографических пиков на хроматограммах градуировочных образцов и экстрактов пробы воды
6 Требования безопасности, охраны окружающей среды
6.1 При выполнении измерений массовой концентрации фенмедифама в пробах природных и очищенных сточных вод соблюдают требования безопасности, установленные в национальных стандартах и соответствующих нормативных документах.
6.2 По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся ко 2-му, 3-му, 4-му классам опасности по ГОСТ 12.1.007.
6.3 Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных ПДК в соответствии с ГОСТ 12.1.005.
6.4 Выполнение измерений следует проводить при наличии вытяжной вентиляции. Оператор, выполняющий измерения, должен быть проинструктирован о специфических мерах предосторожности при работе с фенмедифамом.
6.5 Оператор, выполняющий измерения на хроматографе должен знать правила безопасности при работе с электрооборудованием и сжатыми газами.
6.6 Градуировочные растворы и сливы органических растворителей собирают в герметично закрывающуюся посуду и утилизируют согласно установленным правилам.
7 Требования к квалификации операторов
К выполнению измерений и обработке их результатов допускаются лица с высшим профессиональным образованием или со средним профессиональным образованием и стажем работы в лаборатории не менее 3 лет, владеющие техникой газохроматографического анализа и освоившие методику.
8 Требования к условиям измерений
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
- температура окружающего воздуха (20 ± 5) °С;
- атмосферное давление от 84,0 до 106,7 кПа (от 630 до 800 мм рт.ст.);
- влажность воздуха не более 80 % при 25 °С;
- напряжение в сети (220 ± 10) В;
- частота переменного тока в сети питания (50 ± 1) Гц.
9 Подготовка к выполнению измерений, в том числе отбор проб
9.1 Отбор и хранение проб
Отбор проб для выполнения измерений массовой концентрации фенмедифама производится в соответствии с ГОСТ 17.1.5.05 и ГОСТ Р 51592. Оборудование для отбора проб должно соответствовать ГОСТ 17.1.5.04 и ГОСТ Р 51592. Из батометра пробу без фильтрования переносят в стеклянные бутыли вместимостью 0,5 - 1,0 дм3 и закрывают притёртыми стеклянными или обёрнутыми тефлоновой пленкой или алюминиевой фольгой корковыми или полиэтиленовыми пробками. Применение полиэтиленовой посуды и резиновых пробок не допускается.
Пробы воды, предназначенные для определения в них фенмедифама можно хранить не более 5 сут. при температуре от 5 °С до 7 °С. Перед проведением анализа пробы в этом случае подогревают до комнатной температуры.
Осушенные безводным сульфатом натрия этилацетатные экстракты в стеклянной посуде с притертыми пробками могут храниться при температуре от 5 °С до 7 °С не более 10 сут.
9.2 Приготовление растворов и реактивов
9.2.1 Сульфат натрия безводный
Перед использованием сульфат натрия прокаливают в муфельной печи при температуре 400 °С в течение 8 ч. Прокаленный сульфат натрия хранят в колбе с притертой пробкой в эксикаторе.
9.2.2 Соляная кислота, водный раствор 1:1
Для приготовления раствора смешивают равные объемы концентрированной соляной кислоты и дистиллированной воды.
9.2.3 Этилацетат, очищенный
Этилацетат перед использованием сушат в течение нескольких дней над карбонатом калия (поташом), затем фильтруют через слой медицинской ваты в колбу для перегонки и перегоняют, отбирая фракцию, кипящую в диапазоне температур от 76,5 °С до 77,5 °С. Хранят в плотно закрытой склянке.
9.3 Приготовление фильтра для очистки воздуха
Используемый для упаривания экстрактов воздух необходимо очищать, пропуская через фильтр с активным углем. В качестве фильтра применяют склянку для очистки газов типа СПТ. Входной и выходной отростки склянки заполняют медицинской ватой и наполняют склянку активным углем. При этом выходную часть склянки наполняют активным углем так, чтобы его уровень не доходил до выходного отростка примерно на 3 - 4 см. После этого входной отросток склянки соединяют с аквариумным микрокомпрессором, а на выходной отросток надевают трубку из силиконовой резины. В другой конец трубки вставляют стеклянную пипетку Пастера. Струя очищенного воздуха, поступающего из пипетки при включении микрокомпрессора, используется для упаривания экстрактов.
9.4 Подготовка набивной колонки
Стеклянную газохроматографическую колонку внутренним диаметром 3 мм и длиной 1 м промывают последовательно ацетоном и гексаном, сушат при температуре от 110 °С до 120 °С в сушильном шкафу и заполняют носителем с неподвижной фазой EGSP-Z или OV-210.
Для заполнения газохроматографической колонки один ее конец, который в дальнейшем будет подсоединяться к детектору, закрывают тампоном из промытого ацетоном и гексаном стекловолокна и присоединяют к вакуумному насосу через мелкую капроновую сетку. Затем включают насос и заполняют колонку носителем с фазой, добавляя последний небольшими порциями и постукивая колонку палочкой с резиновым концом при постоянно работающем насосе, следя за тем, чтобы носитель заполнял колонку равномерно, без разрывов.
Заполненную колонку закрывают тампоном из стекловолокна и помещают в термостат колонок хроматографа, подсоединив к испарителю, но не подсоединяя к детектору. Кондиционирование колонки целесообразно проводить следующим образом. Установив расход азота через колонку от 35 до 45 см3/мин, выдерживают колонку при температуре от 60 °С до 70 °С в течение 30 мин. Затем поднимают температуру термостата колонок со скоростью 2 - 3 град/мин до 230 °С в случае использования неподвижной фазы EGSP-Z или до 260 °С в случае использования неподвижной фазы OV-210 и при этой температуре кондиционируют колонку в течение 8 ч.
9.5 Подготовка хроматографа
Подготовку хроматографа проводят в соответствии с руководством по его эксплуатации. После кондиционирования колонки её подсоединяют к детектору, устанавливают расход газа-носителя (азота) через колонку от 30 до 40 см3/мин и проверяют герметичность соединений.
Устанавливают необходимый режим работы хроматографа. После выхода прибора на рабочий режим вводят несколько раз по 5 мм3 градуировочного образца фенмедифама № 3 или № 4 и проверяют эффективность работы колонки.
Примечание: вместо набивной колонки может быть использована капиллярная кварцевая колонка DB-210 или аналогичная другой марки длиной 25 - 30 м, диаметром 0,32 мм с толщиной фазы 0,25 - 0,50 мкм. Кондиционирование капиллярной колонки осуществляется в соответствии с её паспортом.
Условия хроматографирования следует устанавливать свои для каждого конкретного хроматографа и колонки, исходя из приведенных ниже рекомендаций:
- температура испарителя...................................................... от 220 °С до 230 °С;
- температура колонки........................................................... от 200 °С до 220 °С (при необходимости может использоваться программирование температуры в диапазоне от 100 °С до 220 °С);
- температура детектора и солевого источника, а также расход азота на поддув детектора и соотношение расходов водорода и воздуха - в соответствии с руководством по эксплуатации используемого детектора;
- расход азота через набивную колонку............................... от 30 до 40 см3/мин;
- рабочий предел измерений на усилителе в зависимости от определяемых концентраций;
- скорость диаграммной ленты (при использовании самописца)................. 240 мм/ч.
9.6 Приготовление градуировочных растворов фенмедифама
9.6.1 Градуировочные растворы готовят из ГСО, содержащего чистый реактив с массовой долей фенмедифама не менее 99 %. Для приготовления градуировочного раствора № 1 на лабораторных весах высокого класса точности взвешивают (0,0250 ± 0,0005) г фенмедифама. Навеску количественно переносят в мерную колбу с притертой пробкой вместимостью 25 см3, растворяют примерно в 20 см3 ацетона. Спустя 2 ч после растворения навески доводят объём раствора до метки на колбе ацетоном и перемешивают. Полученному раствору приписывают концентрацию фенмедифама 1000 мкг/см3.
Раствор хранят в герметично закрытой склянке в холодильнике не более 6 мес.
9.6.2 Для приготовления градуировочного раствора № 2 отбирают пипеткой с одной отметкой 5,0 см3 градуировочного раствора № 1, помещают его в мерную колбу вместимостью 50 см3, доводят объём раствора в колбе до метки ацетоном и перемешивают. Полученному раствору приписывают концентрацию фенмедифама 100 мкг/см3.
Раствор хранят в плотно закрытой склянке в холодильнике не более 3 мес.
9.6.3 Границы погрешности приготовления градуировочных растворов фенмедифама не превышают ± 2 %.
9.7 Приготовление градуировочных образцов
Градуировочные образцы фенмедифама готовят в мерных колбах с притертыми пробками вместимостью 10 см3, отмеривая градуированными пипетками вместимостью 1 и 2 см3 указанные в таблице 2 объёмы градуировочных растворов соответствующих концентраций и помещая их в колбу. Объём раствора в мерной колбе доводят до метки ацетоном. Приписываемое градуировочному образцу значение массовой концентрации фенмедифама также приведено в таблице 2. Градуировочные образцы хранят в холодильнике в плотно закрытых склянках не более 1 мес.
Примечание - при отсутствии мерных колб вместимостью 10 см3 допускается использовать для приготовления градуировочных образцов градуированные пробирки вместимостью 10 см3.
Таблица 2 - Схема приготовления градуировочных образцов
|
Номер градуировочного образца |
Концентрация градуировочного раствора, используемого для приготовления градуировочного образца, мкг/см3 |
Объем градуировочного раствора, вносимый в мерную колбу, см3 |
Массовая концентрация фенмедифама в градуировочном образце, мкг/см3 |
|
1 |
100 |
0,5 |
5,0 |
|
2 |
100 |
1,0 |
10 |
|
3 |
100 |
2,0 |
20 |
|
4 |
1000 |
0,5 |
50 |
|
5 |
1000 |
1,0 |
100 |
|
6 |
1000 |
1,5 |
150 |
10 Порядок выполнения измерений
10.1 Выполнение холостого опыта
Холостой опыт проводят перед анализом проб воды с целью проверки чистоты применяемых реактивов, материалов и посуды.
Для выполнения холостого опыта берут 500 см3 дистиллированной воды и анализируют её согласно 10.2 - 10.5.
Если на хроматограмме холостого опыта имеется пик со временем удерживания фенмедифама, то устанавливают, какой из реактивов или материалов загрязнен и проводят его очистку или заменяют этим же реактивом или материалом, но из другой партии.
10.2 Предварительная очистка проб воды гексаном
Отмеривают мерным цилиндром 500 см3 нефильтрованной пробы природной воды, помещают её в делительную воронку и подкисляют раствором соляной кислоты (см. 9.2.2) до рН 3 по универсальной индикаторной бумаге. Затем в делительную воронку вносят 15 см3 гексана и встряхивают её в течение 3 мин.
После экстракции содержимому воронки дают расслоиться в течение 15 - 30 мин. Водную фазу переносят в стакан вместимостью 600 или 1000 см3, а гексановый экстракт отбрасывают. В очищенную гексаном пробу воды в стакане добавляют порциями в 3 - 4 приема 50 г безводного сульфата натрия и перемешивают до его полного растворения. Делительную воронку ополаскивают дважды по 10 см3 ацетоном и, после растворения сульфата натрия, возвращают пробу воды в делительную воронку.
10.3 Извлечение из воды фенмедифама
В делительную воронку вносят 50 см3 этилацетата и интенсивно экстрагируют пробу в течение 5 мин. Дают смеси в делительной воронке расслоиться в течение 15 - 30 мин.
Затем водную фазу переносят в стакан, а этилацетатный экстракт - в колбу с притёртой пробкой вместимостью 100 см3 (объём получаемого при этом экстракта составляет от 25 до 30 см3). Пробу воды вновь возвращают в делительную воронку и экстрагируют ещё раз 15 см3 этилацетата. После расслоения фаз пробу воды отбрасывают, а этилацетатный экстракт объединяют с первым экстрактом.
В колбу с объединенным этилацетатным экстрактом при непрерывном помешивании добавляют безводный сульфат натрия в количестве от 2 до 5 г (в зависимости от степени эмульгированности экстракта) и затем фильтруют экстракт через слой безводного сульфата натрия (примерно, 2 - 3 г), помещенного в воронку на подложку из обезжиренной ваты и предварительно смоченного этилацетатом до появления первой капли. Вату для обезжиривания промывают гексаном, а затем высушивают и хранят в плотно закрытом бюксе.
Делительную воронку ополаскивают внутри 5 см3 этилацетата, переносят эту порцию этилацетата из делительной воронки в колбу, в которой был объединённый экстракт, обмывают ею стенки колбы и находящийся в колбе сульфат натрия и также фильтруют через слой сульфата натрия в воронке. Колбу и находящийся в ней сульфат натрия ещё раз ополаскивают 5 см3 этилацетата, который затем фильтруют через ту же воронку с сульфатом натрия.
Весь фильтрат (экстракт и промывные порции этилацетата) собирают в аппарат Кудерна-Даниша для упаривания, либо в колбу с притертой пробкой вместимостью 100 см3, если его необходимо оставить на хранение. Хранят экстракт в холодильнике при температуре от 5 °С до 7 °С не более 10 дней. После хранения содержимое колбы переносят в аппарат Кудерна-Даниша, обмывают колбу 5 см3 этилацетата, промывную порцию этилацетата также переносят в аппарат Кудерна-Даниша.
10.4 Концентрирование экстракта
К аппарату Кудерна-Даниша, содержащему полученный по 10.3 экстракт, подсоединяют дефлегматор и помещают аппарат на водяную баню при температуре 96 - 98 °С так, чтобы уровень воды в бане доходил до середины шлифа пробирки для концентрата. Необходимо следить, чтобы дефлегматор не охлаждался и кипение не прекращалось (при необходимости - защитить среднюю часть аппарата асбестовым экраном).
Экстракт упаривают в этих условиях до объема, примерно, 0,5 см3. Удаление растворителя длится от 30 до 40 мин. Затем аппарат извлекают из водяной бани и охлаждают на воздухе. Дефлегматор и среднюю часть аппарата обмывают 3 см3 этилацетата и отсоединяют пробирку с концентратом. После отсоединения пробирки её содержимое упаривают досуха струей азота или очищенного воздуха.
Сухой остаток растворяют в ацетоне, приливая последний в пробирку аппарата Кудерна-Даниша по её стенкам, обмывая их. Объем ацетонового раствора сухого остатка доводят до 1,0 см3 добавлением по каплям ацетона или подпариванием струей азота или воздуха.
Вместо аппарата Кудерна-Даниша концентрирование экстрактов можно проводить в колбах с Г-образным отводом на водяной бане с температурой около 80 °С под струей воздуха или азота или с помощью ротационного испарителя (температура бани около 50 °С).
10.5 Хроматографирование
В испаритель хроматографа вводят 5 мм3 градуировочного образца фенмедифама № 3, 4 или 5 и записывают хроматограмму. Устанавливают время удерживания фенмедифама по результатам трех хроматографирований. Этот параметр следует проверять ежедневно перед началом измерений после выхода хроматографа на рабочий режим. Время удерживания фенмедифама в зависимости от условий хроматографирования составляет от 7 до 9 мин.
Затем в испаритель хроматографа три раза вводят аликвоту (5 мм3) ацетонового раствора пробы (см. 10.4). Фенмедифам идентифицируют, сравнивая время его удерживания на хроматограмме градуировочного образца и пробы. Объемы вводимых в хроматограф аликвот градуировочного образца и пробы должны быть одинаковы.
Для выполнения количественных расчетов массовой концентрации фенмедифама в качестве градуировочного образца следует из приведенных в таблице 2 выбирать такой градуировочный образец, высота пика фенмедифама на хроматограмме которого наиболее близка к высоте его пика на хроматограмме пробы.
Если концентрация фенмедифама в ацетоновом концентрате пробы превышает его концентрацию в образце № 6, то отбирают пипеткой или микрошприцем аликвоту концентрата, помещают ее в пробирку вместимостью 5 см3, добавляют ацетон до объема 1,0 или 2,0 см3, перемешивают и повторяют измерение. Аликвоту пробы для разбавления следует выбирать так, чтобы концентрация фенмедифама в разбавленном растворе была выше концентрации в образце № 4, но ниже концентрации в образце № 6.
10.6 Определение коэффициента учета потерь фенмедифама
В процессе анализа проб воды происходит некоторая потеря фенмедифама. Во избежание получения заниженных результатов, в формулу, по которой рассчитывают массовую концентрацию фенмедифама, введен коэффициент b, учитывающий эти потери. Величина потерь, главным образом зависит от вида устройств, применяемых для концентрирования экстрактов, и типа анализируемой воды.
Для определения коэффициента b в две делительные воронки вносят по 500 см3 природной воды определенного типа. В одну из проб пипеткой вносят 1,0 см3 раствора градуировочного образца № 2 или № 3 и содержимое делительной воронки перемешивают. Затем обе пробы анализируют согласно 10.2 - 10.6, применяя то устройство для концентрирования экстрактов, которое обычно применяется в данной лаборатории.
Пробы воды, как с добавками, так и без добавок, анализируют в 3-х повторностях. Рассчитывают коэффициент b по формуле
![]() (1)
(1)
где Сд - массовая концентрация добавки фенмедифама к пробе воды, мкг/дм3;
X' - массовая концентрация фенмедифама в пробе воды с добавкой (среднее арифметическое из трех измерений), мкг/дм3;
X - массовая концентрация фенмедифама в пробе воды без добавки (среднее арифметическое из трех измерений), мкг/дм3.
Массовую концентрацию фенмедифама в пробах воды с добавками и без добавок Х' и X, соответственно, находят по формуле (2) при b = 1.
Определение коэффициента учета потерь проводят для каждого типа воды, анализируемой в лаборатории.
Ориентировочная величина коэффициента b, полученная при метрологической аттестации методики, составляет 1,15.
10.7 Мешающие влияния и их устранение
Предварительная обработка проб воды гексаном и применение полярных неподвижных фаз EGSP-Z и OV-210 при хроматографировании проб позволяет осуществлять достаточно надёжное отделение хроматографического пика фенмедифама от хроматографических пиков переходящих в гексан компонентов природных вод и ряда пестицидов, в том числе пропазина, атразина, симазина, прометрина, диметоата.
11 Обработка результатов измерений
Массовую концентрацию фенмедифама в анализируемой пробе воды X, мкг/дм3, рассчитывают по формулам
или ![]() (3)
(3)
где Сст - массовая концентрация фенмедифама в градуировочном образце, мкг/см3;
Sx(hx) - площадь (высота) пика фенмедифама на хроматограмме пробы,
V1 - объём ацетонового раствора сухого остатка пробы, см3;
Sст(hст) - площадь (высота) пика фенмедифама на хроматограмме градуировочного образца;
V2 - объём пробы воды, взятый для анализа, дм3;
b - коэффициент, учитывающий потери фенмедифама в процессе анализа;
η - степень разбавления экстракта (если разбавление не проводилось, η = 1).
12 Оформление результатов измерений
12.1 Результат измерения в документах, предусматривающих его использование, представляют в виде
Х ± ∆, мкг/дм3 (Р = 0,95), (4)
где ± Δ - границы характеристики погрешности результата измерения для данной массовой концентрации фенмедифама, мкг/дм3 (см. таблицу 1).
Численные значения результата измерения должны оканчиваться цифрой того же разряда, что и значения характеристики погрешности; последние не должны содержать более двух значащих цифр.
12.2 Допустимо представлять результат в виде
X ± Δл (Р = 0,95) при условии Δл < Δ, (5)
где ± Δл - границы характеристик погрешности результатов измерений, установленные при реализации методики в лаборатории и обеспечиваемые контролем стабильности результатов измерений.
12.3 Результаты измерений оформляют протоколом или записью в журнале по формам, приведенным в Руководстве по качеству лаборатории.
13 Контроль качества результатов измерений при реализации методики в лаборатории
13.1 Общие положения
13.1.1 Контроль качества результатов измерений при реализации методики в лаборатории предусматривает:
- оперативный контроль исполнителем процедуры выполнения измерений (на основе оценки погрешности при реализации отдельно взятой контрольной процедуры);
- контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности).
13.1.2 Периодичность оперативного контроля и процедуры контроля стабильности результатов выполнения измерений регламентируют в Руководстве по качеству лаборатории.
13.2 Алгоритм оперативного контроля процедуры выполнения измерений с использованием метода добавок
13.2.1 Оперативный контроль исполнителем процедуры выполнения измерений проводят путем сравнения результатов отдельно взятой контрольной процедуры Кк с нормативом контроля К. Для выполнения контроля измеряют концентрацию фенмедифама в рабочей пробе без добавки и в пробе с известной добавкой. Добавка к пробе должна составлять не более 100 % от концентрации фенмедифама в пробе. При отсутствии фенмедифама в пробе добавка должна быть равна удвоенной минимально определяемой концентрации. Пробу с добавкой анализируют одновременно с рабочими пробами.
13.2.2 Результат контрольной процедуры Кк, мкг/дм3, рассчитывают по формуле
Кк = |Х' - Х - Сд|, (6)
13.2.3 Норматив контроля погрешности К, мкг/дм3 рассчитывают по формуле
![]() (7)
(7)
где Δлх' - значения характеристики погрешности результатов измерений, установленные при реализации методики в лаборатории, соответствующие массовой концентрации фенмедифама в пробе с добавкой, мкг/дм3;
Δлх - значения характеристики погрешности результатов измерений, установленные при реализации методики в лаборатории, соответствующие массовой концентрации фенмедифама в рабочей пробе, мкг/дм3.
Примечание - Допустимо для расчета норматива контроля использовать значения характеристик погрешности, полученные расчетным путем по формулам Δлх' = 0,84 ∙ Δх' и Δлх = 0,84 ∙ Δх.
13.2.4 Если результат контрольной процедуры удовлетворяет условию
Кк ≤ К, (8)
процедуру анализа признают удовлетворительной.
При невыполнении условия (8) контрольную процедуру повторяют. При повторном невыполнении условия (8) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
14 Проверка приемлемости результатов, полученных в условиях воспроизводимости
14.1 Расхождение между результатами измерений, полученными в двух лабораториях, не должно превышать предела воспроизводимости R. При выполнении этого условия приемлемы оба результата измерений и в качестве окончательного может быть использовано их общее среднее значение. Значение предела воспроизводимости рассчитывают по формуле
R = 2,77 ∙ σR. (9)
14.2 При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов измерений согласно разделу 5 ГОСТ Р ИСО 5725-6 или МИ 2881.
14.3 Проверка приемлемости проводится при необходимости сравнения результатов измерений, полученных двумя лабораториями.
Лист регистрации изменений
|
Номер изменения |
Номер страницы |
Номер документа (ОРН) |
Подпись |
Дата внесения изменения |
Дата введения изменения |
|||
|
измененной |
замененной |
новой |
аннулированной |
|||||