РД 52.24.367-95
РУКОВОДЯЩИЙ ДОКУМЕНТ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ. МЕТОДИКА ВЫПОЛНЕНИЯ
ИЗМЕРЕНИЙ МАССОВОЙ КОНЦЕНТРАЦИИ НИТРАТОВ В
ПОВЕРХНОСТНЫХ ВОДАХ СУШИ
ПОТЕНЦИОМЕТРИЧЕСКИМ МЕТОДОМ С
ИОНСЕЛЕКТИВНЫМ ЭЛЕКТРОДОМ
Ростов-на-Дону
1995
Предисловие
1. РАЗРАБОТАН Гидрохимическим институтом, Малым научно-производственным предприятием «Акватест»
2. РАЗРАБОТЧИКИ Л.Ф. Быстрова
3. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Начальником ГУЭМЗ Росгидромета Цатуровым Ю.С. 17.04.95
4. ОДОБРЕН Секцией по методам химического и радиологического мониторинга природной среды ЦКПМ Росгидромета 11.04.95, протокол № 2
5. СВИДЕТЕЛЬСТВО ОБ АТТЕСТАЦИИ МВИ Выдано Гидрохимическим институтом в 1995 г. № 16
6. ЗАРЕГИСТРИРОВАН ЦКБ ГМП в 1995 г. № 367
7. ВЗАМЕН РД 52.24.16-85
Введение
Азот относятся к числу биогенных элементов и его соединения имеют особое значение для развития жизни в водных объектах. При отсутствии азотсодержащих соединений в воде рост и развитие водной растительности прекращается, однако избыток этих соединений также приводит к негативным последствиям, вызывая процессы эвтрофирования водного объекта и ухудшение качества воды.
Минеральные формы азота в водных объектах представлены, главным образом нитритами, нитратами, аммиаком и ионами аммония.
Источниками поступления соединений азота в природные воды являются разложение клеток отмерших организмов, прижизненные выделения гидробионтов, атмосферные осадки, фиксация из воздуха в результате жизнедеятельности азотфиксирующих бактерий. Значительное количество азота может попадать в водные объекты с бытовыми, сельскохозяйственными и промышленными сточными водами.
Понижение содержания соединений азота в водоемах связано, в основном, с потреблением их водными растениями. Некоторую роль в этом процессе играет денитрификация, т.е. перевод связанного азота в свободное состояние.
Нитраты являются конечным продуктом минерализации органических азотсодержащих веществ, их содержание в воде, как правило, значительно превышает содержание аммонийного и нитритного азота. В незагрязненных водных объектах концентрация нитратного азота обычно не превышает десятков микрограммов в кубическом дециметре. Для нитратов характерно уменьшение содержания в вегетационный период за счет потребления водными растениями и увеличение осенью при отмирании водных организмов и минерализации органических веществ. Максимальное содержание нитратов наблюдается в зимний период.
Содержание нитратов в подземных водах обычно значительно выше, чем в поверхностных.
Предельно допустимая концентрация нитратного азота в природных водах составляет 9,1 мг/дм3 для водных объектов рыбохозяйственного назначения и 10 мг/дм3 - хозяйственно-питьевого и культурно-бытового назначения.
РД 52.24.367-95
РУКОВОДЯЩИЙ ДОКУМЕНТ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ. МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ МАССОВОЙ КОНЦЕНТРАЦИИ НИТРАТОВ В ПОВЕРХНОСТНЫХ ВОДАХ СУШИ ПОТЕНЦИОМЕТРИЧЕСКИМ МЕТОДОМ С ИОНСЕЛЕКТИВНЫМ ЭЛЕКТРОДОМ
Дата введения 01.07.95 г.
1. Назначение и область применения методики
Настоящий руководящий документ устанавливает потенциометрическую методику выполнения измерений массовой концентрации нитратов в пробах поверхностных вод суши в диапазоне 0,6 - 6200 мг/дм3 с ионоселективным электродом.
2. Нормы погрешности и значения характеристик погрешности измерения
В соответствии с ГОСТ 27384 погрешность выполнения измерений массовой концентрации нитратов в природных водах не должна превышать ± 25 % в диапазоне от 0,01 до 0,1 мг/дм3, ± 20 % в диапазоне от 0,1 до 3,0 мг/дм3 и 15 % свыше 3,0 мг/дм3.
Установленные для настоящей методики значения характеристик погрешности и ее составляющих приведены в таблице 1.
Таблица 1 - Значения характеристик погрешности и ее составляющих (P = 0,95)
|
Характеристики составляющих погрешности, % |
Характеристика погрешности, % |
||
|
случайной,
|
систематической, Dc |
||
|
0,6 - 62 |
8 |
14 |
28 |
|
св. 62 - 6200 |
10 |
7 |
20 |
3. Метод измерения
В основу определения положено измерение потенциала электрода, селективного к нитрат-ионам. По величине электродного потенциала из градуировочной зависимости находят концентрацию в пробе нитрат-ионов.
Возможное мешающее влияние хлорид-, иодид- и бромид ионов устраняют введением в анализируемую пробу раствора сульфата серебра и фосфатного буферного раствора.
4. Средства измерений, вспомогательные устройства, реактивы, материалы
4.1. Средства измерений, вспомогательные устройства
4.1.1. Иономер любого типа, работающий в режиме милливольтметра, снабженный магнитной мешалкой
4.1.2. Электрод измерительный ЭМ-020604 КСРШ.418422.015 по КОРШ. 418422.015 ТУ или другой с аналогичными характеристиками.
4.1.3. Электрод вспомогательный хлорсеребряный ЭВЛ-1МЗ по ТУ 25.05.2181 или другого типа с аналогичными характеристиками.
4.1.4. Весы аналитические 2 класса точности по ГОСТ 244.
4.1.5. Весы технические лабораторные любого типа 4 класса точности с пределом взвешивания 200 г.
4.1.6. Шкаф сушильный общелабораторного назначения по ГОСТ 13474.
4.1.7. Колбы мерные не ниже 2 класса точности по ГОСТ 1770 вместимостью:
100 см3 - 1
250 см3 - 1
1000 см3 - 1
4.1.8. Пипетка градуированная не ниже 2 класса точности по ГОСТ 29227 вместимостью:
2 см3 - 2
10 см3 - 1
4.1.9. Цилиндры мерные по ГОСТ 1770 вместимостью:
25 см3 - 2
4.1.10. Стаканы химические по ГОСТ 25336 вместимостью:
50 см3 - 8
500 см3 - 1
4.1.11. Стаканчики для взвешивания (бюксы) по ГОСТ 25336 - 2
Допускается использование других типов средств измерений, посуды и вспомогательного оборудования, в том числе импортных, с характеристиками не хуже, чем у приведенных в 4.1.
4.2.1. Стандартный образец нитрат-ионов или нитрат калия KNO3 ГОСТ 4144, х.ч.
4.2.2. Сульфат серебра Ag2SO4 по ТУ 6-09-3703, х.ч.
4.2.3. Хлорид калия KCl по ГОСТ 4234, х.ч.
4.2.4. Гидроксид калия KOH по ГОСТ 4203, х.ч.
4.2.5. Ортофосфорная кислота H3PO4 по ГОСТ 6552, х.ч.
4.2.6. Вода дистиллированная, по ГОСТ 6709.
4.2.7. Фильтровальная бумага.
Допускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже указанной в 4.2.
5. Отбор и хранение проб
Отбор проб для определения нитратов производится в соответствии с ГОСТ 17.1.5.05. Пробы помещают в стеклянную или полиэтиленовую посуду с плотно закрывающейся пробкой. Нитраты являются биохимически нестойким компонентом, поэтому анализ должен быть проведен в день отбора пробы. При охлаждении до 3 - 5 °C допускается хранение проб в течение 3 сут. Более длительное хранение возможно при замораживании пробы.
6. Подготовка к выполнению измерений
6.1. Приготовление растворов и реактивов
6.1.1. Фосфатный буферный раствор (pH 2,2)
К 300 см3 дистиллированной воды приливают при перемешивании 68 см3 H3PO4. В небольшом количестве дистиллированной воды растворяют 28 г KOH. Оба раствора смешивают в химическом стакане, переносят в мерную колбу вместимостью 1000 см3 и доводят дистиллированной водой до метки на колбе.
6.1.2. Раствор сульфата серебра 10-2 моль/дм3
3,117 г Ag2SO4 растворяют в дистиллированной воде в мерной колбе вместимостью 1000 см3 и доводят дистиллированной водой до метки на колбе. Хранят в темной склянке не более 3 мес.
6.1.3. Насыщенный раствор хлорида калия
60 г KCl растворяют в 200 см3 дистиллированной воды при температуре 50 - 60 °C. После охлаждения используют раствор над осадком для заполнения вспомогательного электрода.
6.2. Приготовление градуировочных растворов
Градуировочные растворы, аттестованные по процедуре приготовления готовят из стандартного образца нитрат-ионов или нитрата калия.
Приготовление градуировочных растворов из стандартного образца или нитрата калия осуществляют в соответствии с 6.2.1 - 6.2.7.
Для градуировочных растворов с концентрацией 1,00 · 10-1 - 1,00 · 010-4; 2,00 · 10-5; 1,00 · 010-5 моль/дм3 погрешности, обусловленные процедурой приготовления, не превышают 1 %, для градуировочного раствора с концентрацией 6,00 · 10-5 - 2 % относительно приписанного значения концентрации нитрат-ионов.
6.2.1. Раствор нитрата калия 1,00 · 010-1 моль/дм3
Раствор готовят из стандартного образца нитратных ионов в соответствии с инструкцией по его применению, или 2,527 г KNO3, предварительно высушенного при 110 °C до постоянной массы, растворяют в дистиллированной воде в мерной колбе вместимостью 250 см3 и доводят объем дистиллированной водой до метки на колбе.
6.2.2. Раствор нитрата калия 1,00 · 10-2 моль/дм3 (2,0 pNO3)
Отбирают 10 см3 раствора KNO3 1,00 · 10-1 моль/дм3 в мерную колбу вместимостью 100 см3 и доводят дистиллированной водой до метки на колбе.
6.2.3. Раствор нитрата калия 1,00 · 10-3 моль/дм3 (3,0 pNO3)
Отбирают 10 см3 раствора KNO3 1,00 · 10-2 моль/дм3 в мерную колбу вместимостью 100 см3 и доводят дистиллированной водой до метки на колбе.
6.2.4. Раствор нитрата калия 1,00 · 10-4 моль/дм3 (4,0 pNO3)
Отбирают 10 см3 раствора KNO3 1,00 · 10-3 моль/дм3 в мерную колбу вместимостью 100 см3 и доводят дистиллированной водой до метки на колбе.
6.2.5. Раствор нитрата калия 6,00 · 10-5 моль/дм3 (4,2 pNO3)
Отбирают 6,0 см3 раствора KNO3 1,00 · 10-3 моль/дм3 в мерную колбу вместимостью 100 см3 и доводят дистиллированной водой до метки на колбе.
6.2.6. Раствор нитрата калия 2,00 · 10-5 моль/дм3 (4,7 pNO3)
Отбирают 2,0 см3 раствора KNO3 1,00 · 10-3 моль/дм3 в мерную колбу вместимостью 100 см3 и доводят дистиллированной водой до метки на колбе.
6.2.7. Раствор нитрата калия 1,00 · 10-5 моль/дм3 (5,0 pNO3)
Отбирают 10 см3 раствора KNO3 1,00 · 10-4 моль/дм3 в мерную колбу вместимостью 100 см3 и доводят дистиллированной водой до метки на колбе.
Градуировочные растворы нитрата калия 1,00 · 10-1 - 1,00 · 10-2 моль/дм3 хранят не более 1 мес., 1,00 · 10-3 - 1,00 · 10-5 моль/дм3 готовят непосредственно перед использованием.
6.3. Подготовка прибора, измерительного и вспомогательного электродов к работе
Подготовку иономера, измерительного и вспомогательного электродов к работе осуществляют в соответствии с инструкциями по их эксплуатации.
6.4. Установление градуировочной зависимости
В стаканы вместимостью 50 см3 вносят по 20 см3 раствора нитрата калия с концентрацией 1,00 · 10-5; 2,00 · 10-5; 6,00 · 10-5; 1,00 · 10-4; 1,00 · 10-3 моль/дм3 и добавляют по 2 см3 раствора сульфата серебра и по 2 см3 фосфатного буферного раствора. Стаканы устанавливают на магнитную мешалку, погружают в раствор электроды и проводят измерение потенциала в градуировочных растворах от меньшей концентрации нитратных ионов (1,00 · 10-5 моль/дм3) к большей (1,00 · 10-3 моль/дм3). Глубина погружения электродов и скорость перемешивания должны быть одинаковыми во всех измерениях. Показания прибора записывают после установления постоянного значения потенциала. Время его установления зависит от концентрации нитрат-ионов в градуировочных растворах и составляет от нескольких секунд до минут.
Для каждой концентрации градуировочного раствора проводят по три параллельных измерения потенциала и за результат принимают среднее арифметическое. Градуировочную зависимость устанавливают в координатах: значения pNO3 градуировочных растворов (pNO3 = -lg[NO3-], где [NO3-] - концентрация нитрат-ионов, моль/дм3) - соответствующие им значения потенциала, мВ.
Градуировочную зависимость устанавливают перед каждой серией определений, а также при замене измерительного или вспомогательного электродов.
Если инструкцией по эксплуатации прибора предусмотрен иной способ установления градуировочной зависимости (градуировки), то ее устанавливают в соответствии с инструкцией к данному прибору.
7. Выполнение измерений
20 см3 анализируемой пробы вносят в стакан вместимостью 50 см3, приливают 2 см3 раствора сульфата серебра и 2 см3 фосфатного буферного раствора. Стакан устанавливают на магнитную мешалку, погружают в раствор электроды, ожидают установления равновесного значения потенциала и записывают показания прибора.
После окончания измерения потенциала электроды отмывают дистиллированной водой. Отмывка электродов происходит достаточно быстро при трехкратной замене дистиллированной воды.
Температура анализируемой пробы должна быть одинакова с температурой растворов при установлении градуировочной зависимости.
8. Вычисление результатов измерений
Значение pNO3 в анализируемых пробах находят по градуировочной зависимости. Массовую концентрацию нитратов Cx, мг/дм3, рассчитывают по следующим соотношениям:
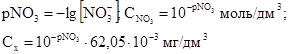 (1)
(1)
или находят из таблицы 2 для значений pNO3 в диапазоне 4 - 5. Для перевода в pNO3 мг/дм3 в диапазоне 3 - 4 увеличивают табличные значения в 10 раз. Например, pNO3, равный 4,41, соответствует 2,41 мг/дм3, pNO3, равный 3,41 - 24,1 мг/дм3.
Результат измерения в документах, предусматривающих его использование, представляют в виде:
![]() (2)
(2)
где D - характеристика погрешности измерения для данной массовой концентрации нитратов (таблица 1).
Численные значения результата измерения должны оканчиваться цифрой того же разряда, что и значения характеристики погрешности.
Таблица 2 - Пересчет значений pNO3 в концентрацию нитратных ионов
|
pNO3 |
С, г/дм3 |
pNO3 |
С, г/дм3 |
pNO3 |
С, г/дм3 |
pNO3 |
С, г/дм3 |
|
4,00 |
6,20 |
4,26 |
3,40 |
4,52 |
1,87 |
4,78 |
1,02 |
|
4,01 |
6,05 |
4,27 |
3,32 |
4,53 |
1,82 |
4,79 |
1,00 |
|
4,02 |
5,92 |
4,28 |
3,25 |
4,54 |
1,78 |
4,80 |
0,98 |
|
4,03 |
5,78 |
4,29 |
3,17 |
4,55 |
1,74 |
4,81 |
0,96 |
|
4,04 |
5,65 |
4,30 |
3,10 |
4,56 |
1,70 |
4,82 |
0,93 |
|
4,05 |
5,52 |
4,31 |
3,03 |
4,57 |
1,66 |
4,83 |
0,91 |
|
4,06 |
5,39 |
4,32 |
2,96 |
4,58 |
1,63 |
4,84 |
0,89 |
|
4,07 |
5,27 |
4,33 |
2,89 |
4,59 |
1,59 |
4,85 |
0,87 |
|
4,08 |
5,15 |
4,34 |
2,83 |
4,60 |
1,55 |
4,86 |
0,85 |
|
4,09 |
5,03 |
4,35 |
2,76 |
4,61 |
1,52 |
4,87 |
0,83 |
|
4,10 |
4,92 |
4,36 |
2,70 |
4,62 |
1,48 |
4,88 |
0,81 |
|
4,11 |
4,81 |
4,37 |
2,64 |
4,63 |
1,45 |
4,89 |
0,79 |
|
4,12 |
4,70 |
4,38 |
2,58 |
4,64 |
1,42 |
4,90 |
0,78 |
|
4,13 |
4,59 |
4,39 |
2,52 |
4,65 |
1,38 |
4,91 |
0,76 |
|
4,14 |
4,49 |
4,40 |
2,46 |
4,66 |
1,35 |
4,92 |
0,74 |
|
4,15, |
4,38 |
4,41 |
2,41 |
4,67 |
1,32 |
4,93 |
0,72 |
|
4,16 |
4,28 |
4,42 |
2,35 |
4,68 |
1,29 |
4,94 |
0,71 |
|
4,17 |
4,19 |
4,43 |
2,30 |
4,69 |
1,23 |
4,95 |
0,69 |
|
4,18 |
4,09 |
4,44 |
2,25 |
4,70 |
1,20 |
4,96 |
0,67 |
|
4,19 |
4,00 |
4,45 |
2,19 |
4,71 |
1,18 |
4,97 |
0,66 |
|
4,20 |
3,91 |
4,46 |
2,14 |
4,72 |
1,15 |
4,98 |
0,64 |
|
4,21 |
3,82 |
4,47 |
2,10 |
4,73 |
1,12 |
4,99 |
0,63 |
|
4,22 |
3,73 |
4,48 |
2,05 |
4,74 |
1,10 |
5,00 |
0,62 |
|
4,23 |
3,65 |
4,49 |
2,00 |
4,75 |
1,07 |
||
|
4,24 |
3,56 |
4,50 |
1,96 |
4,76 |
1,05 |
||
|
4,25 |
3,48 |
4,51 |
1,91 |
4,77 |
1,03 |
9. Контроль погрешности измерений
Оперативный контроль погрешности проводят с использованием метода добавок совместно с методом разбавления пробы. Периодичность контроля - не менее одной контрольной на 15 - 20 рабочих проб за период, в течение которого условия проведения анализа неизменны.
Измеряют концентрацию нитрат-ионов в исходной пробе (Cx), в пробе, разбавленной в n раз (n = 1,5 ÷ 2,5) (Cр) и в пробе, разбавленной в n раз с введенной добавкой (Срд). Величина добавки (Cд) должна соответствовать содержанию нитрат-ионов в исходной пробе. Если нитраты в исходной пробе не обнаружены, величина добавки должна быть равна минимально определяемой концентрации.
Результат контроля признают удовлетворительным, если:
|Cрд - Cр - Сд| + |n · Cр - Cx| £ Кп (3)
Норматив контроля погрешности (Кп) рассчитывают по формуле:
![]() (P = 0,95), (4)
(P = 0,95), (4)
где Dc и
![]() -
характеристики систематической и случайной составляющих погрешности измерения
концентрации нитратов в исходной пробе.
-
характеристики систематической и случайной составляющих погрешности измерения
концентрации нитратов в исходной пробе.
Если в исходной пробе нитраты не обнаружены, то погрешность рассчитывают для концентрации добавки.
При превышении норматива повторяют измерение с использованием другой пробы. При повторном превышении норматива выясняют причины, приводящие к неудовлетворительным результатам, и устраняют их.
10. Требования безопасности
10.1. При выполнении измерений массовой концентрации нитратов в пробах природных и очищенных сточных вод соблюдают требования безопасности, установленные в «Правилах по технике безопасности при производстве наблюдений и работ на сети Госкомгидромета», Л., Гидрометеоиздат, 1983, или в «Типовой инструкции по технике безопасности для гидрохимических лабораторий служб Роскомвода», M., 1995.
10.2. По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся к 2, 3 классам опасности по ГОСТ 12.1.007.
10.3. Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005.
11. Требования к квалификации операторов
К выполнению измерений допускаются лица со средним профессиональным образованием или без профессионального образования, но имеющие стаж работы в лаборатории не менее года и освоившие методику анализа.
12. Затраты времени на проведение анализа
На приготовление растворов и реактивов в расчете на 100 определений требуется 3,0 чел.-ч.
На выполнение измерений и вычисление результата анализа единичной пробы - 0,1 чел.-ч.
На выполнение измерений и вычисление результатов анализа серии из 10 проб - 1 чел.-ч.
Затраты времени на подготовку посуды включены в затраты времени на проведение анализа.
ФЕДЕРАЛЬНАЯ СЛУЖБА ПО ГИДРОМЕТЕОРОЛОГИИ И МОНИТОРИНГУ ОКРУЖАЮЩЕЙ СРЕДЫ
ГИДРОХИМИЧЕСКИЙ ИНСТИТУТ
СВИДЕТЕЛЬСТВО № 16
об аттестации МВИ
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ массовой концентрации нитратов в поверхностных водах суши потенциометрическим методом с ионселективным электродом.
ОСНОВАНА на измерении потенциала электрода, селективного к нитрат-ионам. По величине электродного потенциала из градуировочной зависимости находят концентрацию в пробе нитрат-ионов.
РАЗРАБОТАНА Гидрохимическим институтом, МНПП «Акватест».
РЕГЛАМЕНТИРОВАНА в РД 52.24.367-95.
АТТЕСТОВАНА в соответствии с ГОСТ Р 8.563 (ГОСТ 8.010).
АТТЕСТАЦИЯ проведена Гидрохимическим институтом на основании результатов экспериментальных исследований в 1985 г., и метрологической экспертизы материалов в 1995 г.
В результате аттестации МВИ установлено:
1. МВИ соответствует предъявляемым к ней метрологическим требованиям и обладает следующими основными метрологическими характеристиками:
Значения характеристик погрешности и ее составляющих (P = 0,95)
|
Диапазон измеряемых концентраций нитратов, С, мг/дм3 |
Характеристики составляющих погрешности, % |
Характеристика погрешности, % |
|
|
случайной,
|
систематической Dc |
||
|
0,6 - 62 |
8 |
14 |
28 |
|
св. 62 - 6200 |
10 |
7 |
20 |
2. Оперативный контроль погрешности измерений проводят в соответствии с разделом 9 РД 52.24.367-95.
Дата выдачи свидетельства март 1995 г.
Главный метролог ГУ ГХИ A.A. Назарова
СОДЕРЖАНИЕ