Государственное
санитарно-эпидемиологическое нормирование
Российской Федерации
4.1. Методы контроля. Химические факторы
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ 3-МОНОХЛОРПРОПАНДИОЛА,
2-МОНОХЛОРПРОПАНДИОЛА И ГЛИЦИДОЛА В ПИЩЕВЫХ
РАСТИТЕЛЬНЫХ МАСЛАХ И ЖИВОТНЫХ ЖИРАХ
Методические указания
МУК 4.1.3547-19
Москва, 2019
1. Разработаны: ФГБУН «ФИЦ питания и биотехнологии» (В.В. Бессонов, А.Д. Малинкин, М.А. Макаренко).
2. Утверждены руководителем Федеральной службы по надзору в сфере защите прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А.Ю. Поповой «24» мая 2019 г.
3. Введены впервые.
СОДЕРЖАНИЕ
|
УТВЕРЖДАЮ Руководитель Федеральной службы ____________________ А.Ю. Попова «24» мая 2019 г. |
4.1. Методы контроля. Химические факторы
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ 3-МОНОХЛОРПРОПАНДИОЛА,
2-МОНОХЛОРПРОПАНДИОЛА И ГЛИЦИДОЛА В ПИЩЕВЫХ
РАСТИТЕЛЬНЫХ МАСЛАХ И ЖИВОТНЫХ ЖИРАХ
Методические указания
МУК 4.1.3547-19
I. Общие положения
1.1. Рациональное название: 3-монохлорпропан-1,2-диол. CAS №: 96-24-2
Синонимы: 3-МХПД, 3-хлорпропан-1,2-диол

Рис. 1. Структурная формула 3-МХПД.
3-МХПД образуется в пищевых продуктах при определенных условиях в присутствии хлорид-ионов.
Физические свойства: 3-МХПД представляет собой вязкую бесцветную жидкость с температурой кипения 213 °С. Растворим в воде, спирте, эфире. Токсичность: LD50 у крыс составляет 152 мг/кг.
1.2. Рациональное название: 2-монохлорпропан-1,3-диол. CAS №: 497-04-1
Синонимы: 2-МХПД, 2-хлорпропан-1,3-диол
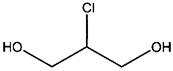
Рис. 2. Структурная формула 2-МХПД.
Физические свойства: 2-МХПД представляет собой вязкую бесцветную жидкость. Растворим в воде, спирте, эфире.
1.3. Рациональное название: 2,3-эпокси-1-пропанол. CAS №: 556-52-5
Синонимы: глицидол, эпоксипропиловый спирт.
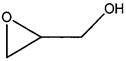
Рис. 3. Структурная формула глицидола.
Глицидол образуется главным образом при гидролизе глицидиловых эфиров, которые в свою очередь образуются из диацилглицеридов при высоких температурах (более 240 °С).
Физические свойства: глицидол представляет собой вязкую бесцветную жидкость без запаха с температурой кипения 167 °С. Растворим в воде, спирте, эфире. Токсичность: LD50 у крыс составляет 420 мг/кг.
II. Область применения
2.1. Методические указания предназначены для определения содержания 2-монохлорпропандиола, 3-монохлорпропандиола и глицидола в диапазоне концентраций от 0,3 до 30,0 мг/кг в пищевых растительных маслах и животных жирах.
2.2. Методические указания предназначены для специалистов органов и организаций, осуществляющих федеральный государственный санитарно-эпидемиологический надзор, проводящих санитарно-эпидемиологические экспертизы, исследования и иные виды оценок, а также для аккредитованных лабораторий, проводящих отбор проб и исследования пищевых продуктов.
III. Требования к показателям точности измерений
3.1. При соблюдении всех регламентированных условий и проведении анализа в точном соответствии с данной методикой значения погрешности (и ее составляющих) результатов измерений не превышают значений, приведенных в таблице 1.
Таблица 1
Значения характеристики погрешности, нормативов
оперативного контроля
точности, повторяемости, воспроизводимости
|
Анализируемый объект |
Диапазон определяемых концентраций, мг/кг |
Показатель точности (границы относительной погрешности Р = 0,95), ±δ, % |
Показатель повторяемости (среднеквадратичное отклонение повторяемости), σr, % |
Показатель воспроизводимости (средне квадратичное отклонение воспроизводимости), σR, % |
Предел повторяемости (значение допустимого расхождения между двумя результатами параллельных определений), r, % |
Предел воспроизводимости (значение допустимого расхождения между двумя результатами измерений, полученных в разных лабораториях), R, %, (Р = 0,95) |
Средняя полнота извлечения вещества, % |
|
3-МХПД |
|||||||
|
пищевые растительные масла и животные жиры |
0,3 - 30,0 |
50 |
9,4 |
10,7 |
26 |
30 |
113,6 |
|
2-МХПД |
|||||||
|
пищевые растительные масла и животные жиры |
0,3 - 30,0 |
35 |
9,2 |
8,3 |
26 |
23 |
107,9 |
|
Глицидол |
|||||||
|
пищевые растительные масла и животные жиры |
0,3 - 30,0 |
69 |
9,2 |
16,5 |
26 |
46 |
87,5 |
IV. Средства измерений, вспомогательные устройства,
материалы, реактивы
4.1. Средства измерений:
газовый хроматограф, оснащенный тройным квадрупольным масс-селективным детектором;
хроматографическая колонка с фазой (5 %-фенил)-метилполисилоксан, 30×0,25 мм×0,25 мкм, с малым уносом подвижной фазы (для ГХ-МС);
весы неавтоматического действия по ГОСТ Р 53228 специального класса точности с пределом допускаемой абсолютной погрешности ±0,0001 г.;
дозаторы вместимостью 0,2; 1 и 5 см3 (с переменным объемом);
колбы мерные наливные 2-25-2, 2-50-2 и 2-100-2 по ГОСТ 1770-74;
цилиндр мерный 1-100-2 по ГОСТ 1770-74;
цилиндр мерный объемом 25 см3 по ГОСТ 1770-74.
Вспомогательные устройства:
устройство для упаривания серии проб (центрифужный концентратор, прибор для упаривания в токе азота или аналогичные устройства);
орбитальный шейкер;
ультразвуковая ванна;
центрифуга для микропробирок.
Материалы:
пробирки центрифужные с завинчивающейся крышкой объемом 15 см3;
микроцентрифужные пробирки с защелкивающейся крышкой объемом 2 см3;
виалы стеклянные объемом 2 см3;
вставки в виалы объемом 200 мм3;
бумага индикаторная, ТУ 6-09-1181-89.
Реактивы:
3-монохлорпропан-1,2-диол (3-МХПД) (CAS № 96-24-2, содержание основного вещества не менее 98 %);
3-монобромпропан-1,2-диол (3-МБПД) (CAS № 4704-77-2, содержание основного вещества не менее 97 %;
3-монохлорпропан-1,2-диол-1,1,2,3,3-d5 (3-МХПД-D5) (CAS № 342611-01-2, содержание основного вещества не менее 97 %, изотопная чистота не менее 97,7 %);
3-монобромпропан-1,2-диол-1,1,2,3,3-d5 (3-МБПД-D5) (СAS № 1246820-48-3, содержание основного вещества не менее 97 %, изотопная чистота не менее 98,4 %);
Кислота фенилборная (ФБК) (CAS № 98-80-6, содержание основного вещества не менее 95 %);
1,2-дипальмитоил-3-монохлорпропандиол-1,1,2,3,3-d5 (1,2-дипальмитат-3-МХПД-d5) (CAS № 1185057-55-9, содержание основного вещества не менее 98 %, изотопная чистота не менее 98 %);
1,3-дипальмитоил-2-монохлорпропандиол-1,1,2,3,3-d5 (1,3-бипальмитат-2-МХПД-65) (CAS № 1426395-62-1, содержание основного вещества не менее 98 %, изотопная чистота не менее 97,4 %);
1,2-дипальмитоил-3-монохлорпропандиол (1,2-дипальмитат-3-МХПД) (СAS № 51930-97-3, содержание основного вещества не менее 98 %);
1,3-дипальмитоил-2-монохлорпропандиол (1,3-дипальмитат-2-МХПД) (СAS № 169471-41-4, содержание основного вещества не менее 98 %);
метанол (для ВЭЖХ);
толуол (для ВЭЖХ);
изооктан (для ВЭЖХ);
натрия гидроксид, х.ч., ГОСТ 4328-77;
эфир диэтиловый, х.ч., ТУ 2600-001-45682126-13;
этилацетат, х.ч., ГОСТ 22300-76;
натрий бромистый, х.ч., ТУ 6-09-5331-87
гексан, х.ч., СТП ТУ СОМР 2-008-06;
кислота ортофосфорная, х.ч., ГОСТ 6552-80;
вода для лабораторного анализа по ГОСТ Р 52501, первой степени чистоты;
универсальная индикаторная бумага;
гелий со степенью чистоты не менее 99,9999 %, ТУ 0271-001-45905715-02.
4.2. Допускается использование средств измерений, вспомогательных устройств, материалов и реактивов с аналогичными или лучшими характеристиками.
V. Принцип метода
5.1. Методика основана на одновременном определении свободных и связанных форм 3-МХПД, 2-МХПД и глицидола в виде фенилборных дериватов свободных 3-МХПД, 2-МХПД и 3-МБПД соответственно после реакции с фенилборной кислотой в пищевых растительных маслах и животных жирах методом газожидкостной хроматографии (ГЖХ) с использованием тройного квадрупольного масс-селективного детектора.
Примечание 1. В процессе длительной щелочной переэтерификации происходит высвобождение МХПД и глицидола из их этерифицированных с жирными кислотами форм. При этом использование низких температур предотвращает нежелательное образование глицидола из свободного 3-МХПД. Добавление подкисленного раствора бромида натрия останавливает реакцию высвобождения и способствует образованию стабильной формы МБПД (3-МБПД >> 2-МБПД) из свободного нестабильного глицидола.
Примечание 2. На всех этапах щелочной переэтерификации следует избегать нагревания проб. Рекомендуется проверять кислотность водной фазы после добавления к пробе раствора бромида натрия.
VI. Отбор проб
6.1. При отборе проб растительных масел и животных жиров следует руководствоваться действующей нормативно-технической документацией по отбору проб для определения токсичных элементов в указанных образцах.
VII. Приготовление стандартных растворов1
________
1 Для приготовления растворов, указанных в главе VII настоящих МУК, допускается использование растворов с аналогичными или лучшими характеристиками. При этом приготовление каждого раствора следует скорректировать в соответствии с требуемой конечной концентрацией аналита.
Приготовление раствора внутреннего стандарта 3-МХПД-d5
с концентрацией 10 мкг/см3
7.1. В виалу с 10 мг 3-МХПД-d5 (количество, указанное поставщиком) вносят около 1 см3 метанола, виалу закрывают крышкой, перемешивают на орбительном шейкере до растворения аналита и переносят в колбу на 50 см3. Затем виалу промывают метанолом 3 - 4 раза, который также переносят в колбу на 50 см3, добавляют около 25 см3 метанола, перемешивают, доводят до метки и снова перемешивают. 2,5 см3 полученного раствора переносят в мерную колбу на 50 см3, доводят до метки метанолом, перемешивают. Приготовленный раствор хранят в морозильной камере при температуре от -22 °С до -25 °С в течение 2-х месяцев.
Приготовление
раствора внутреннего стандарта
3-МБПД-d5 с концентрацией 10 мкг/см3
7.2. В виалу с 1 мг 3-МБПД-d5 (количество, указанное поставщиком) вносят около 1 см3 метанола, виалу закрывают крышкой, перемешивают на орбительном шейкере до растворения аналита и переносят в колбу на 50 см3. Затем виалу промывают метанолом 3 - 4 раза, который также переносят в колбу на 50 см3, добавляют около 25 см3 метанола, перемешивают, доводят до метки и снова перемешивают. 25 см3 полученного раствора переносят в мерную колбу на 50 см3, доводят до метки метанолом, перемешивают. Приготовленный раствор хранят в морозильной камере при температуре от -22 °С до -25 °С в течение 2-х месяцев.
Приготовление
совместного раствора внутреннего стандарта
1,2-дипальмитоил-3-МХПД-d5 и
1,3-дипальмитоил-2-МХПД-d5
с концентрациями 25,6 мкг/см3 каждого
7.3. В каждую виалу с 2,5 мг 1,2-дипальмитоил-3-МХПД-d5 и 2,5 мг 1,3-дипальмитоил-2-МХПД-d5 (количество, указанное поставщиком) вносят около 1 см3 толуола, виалы закрывают крышкой, перемешивают на орбительном шейкере до растворения аналитов и переносят в отдельные колбы на 25 см3. Затем виалы промывают толуолом 3 - 4 раза, который также переносят в соответствующие колбы на 25 см3, перемешивают, доводят до метки и снова перемешивают 6,40 см3 полученного раствора 1,2-дипальмитат-3-МХПД-d5 и 6,40 см3 раствора 1,3-дипальмитат-2-МХПД-d5 переносят в мерную колбу на 25 см3, доводят до метки толуолом, перемешивают. Приготовленный раствор хранят в морозильной камере при температуре от -22 °С до -25 °С в течение 2-х месяцев.
Приготовление
совместного раствора 3-МХПД
и глицидола для градуировки
7.4. Навески по 10 мг 3-МХПД и глицидола (погрешность взвешивания ±0,5 мг) переносят в мерную колбу на 100 см3, добавляют около 25 см3 метанола, перемешивают до растворения, доводят до метки метанолом (основной стандартный раствор с концентрациями 100 мкг/см3).
Путем последовательных разведений готовят рабочие стандартные растворы 3-МХПД и глицидола с концентрациями 0,05 мкг/см3, 0,2 мкг/см3, 0,50 мкг/см3, 2,00 мкг/см3 и 5,00 мкг/см3 в течение 2-х месяцев.
Приготовление
совместного раствора 1,2-дипальмитоил-3-МХПД
и 1,3-дипальмитоил-2-МХПД для градуировки
7.5. В мерную колбу на 100 см3 отвешивают 10 мг 1,3-дипальмитоил-2-МХПД, добавляют около 25 см3 толуола, перемешивают, доводят до метки и снова перемешивают.
В виалу с 10 мг 1,2-дипальмитоил-3-МХПД (количество, указанное поставщиком) вносят около 1 см3 толуола, виалу закрывают крышкой, перемешивают на орбительном шейкере до растворения аналита и переносят в другую колбу на 100 см3. Затем виалу промывают толуолом 3 - 4 раза, который также переносят в указанную колбу, добавляют около 25 см3 толуола, перемешивают, доводят до метки и снова перемешивают.
В мерную колбу на 25 см3 отбирают по 6,65 см3 каждого приготовленного раствора, доводят до метки толуолом (основной стандартный раствор 1,2-дипальмитоил-3-МХПД и 1,3-дипальмитоил-2-МХПД с концентрациями по 26,6 мкг/см3 каждого, что эквивалентно 5 мкг/см3 свободных 3-МХПД и 2-МХПД соответственно).
Путем последовательных разведений готовят рабочие стандартные растворы 1,2-дипальмитоил-3-МХПД и 1,3-дипальмитоил-2-МХПД с концентрациями, эквивалентными концентрациям свободных 3-МХПД и 2-МХПД 0,05 мкг/см3, 0,2 мкг/см3, 0,50 мкг/см3, 2,00 мкг/см3 и 5,00 мкг/см3. Растворы хранят при температуре от -22 °С до -25 °С в течение 2-х месяцев.
VIII. Приготовление необходимых растворов реактивов
Приготовление раствора гидроксида или метоксида натрия
8.1. Навеску 250 мг (погрешность взвешивания ±0,5 мг) гидроксида (мектоксида) натрия помещают в мерную колбу на 100 см3, добавляют около 50 см3 метанола, перемешивают, доводят до метки и снова перемешивают (возможно неполное растворение реактива). Раствор хранят при температуре от -22 °С до -25 °С в течение 2-х месяцев.
Приготовление раствора бромида натрия 55 %
8.2. Навеску 55 г бромида натрия (погрешность взвешивания ±0,5 г) помещают в мерную колбу на 100 см3, добавляют около 85 см3 воды деионизированной, перемешивают до полного растворения, доводят водой деионизированной до метки, перемешивают. К приготовленному раствору добавляют к нему 0,33 см3 ортофосфорной кислоты (600 мм3 этого раствора должно нейтрализовать 500 мм3 раствора гидроксида или метоксида натрия и изменять pH среды до 1 - 3). Раствор хранят при температуре от -22 °С до -25 °С в течение 2-х месяцев.
Приготовление смеси диэтилового эфира и этилацетата 40:60 (об.)
8.3. Дозируют 40 см3 диэтилового эфира в мерный цилиндр на 100 см3, доводят объем до 100 см3 этилацетатом. Смесь готовят непосредственно перед использованием.
Приготовление насыщенного раствора фенилборной кислоты
8.4. Навеску 1 г фенилборной кислоты помещают в мерную колбу на 50 см3, добавляют 0,1 см3 воды деионизированной и доводят до метки диэтиловым эфиром. Для дериватизазции используют только чистую надосадочную жидкость. Раствор хранят при температуре от -22 С до -25 С в течение 2-х месяцев.
IX. Подготовка проб совместных растворов для градуировки
Подготовка проб совместного раствора 3-МХПД и глицидола
9.1. Подготовка проб совместного раствора 3-МХПД и глицидола осуществляется в следующем порядке:
9.1.1. В центрифужные пробирки на 15 см3 дозируют по 600 мм3 рабочих стандартных растворов, приготовленных по п. 7.4, добавляют по 50 мм3 растворов 3-МХПД-d5 по п. 7.1 и 3-МБПД-d5 по п. 7.2.
9.1.2. Добавляют 600 мм3 подкисленного р-ра бромида натрия по п. 8.2.
9.1.3. Добавляют 1 см3 смеси диэтилового эфира: этилацетата по п. 8.3 для экстракции аналита. Верхний слой отбирают в другую центрифужную пробирку на 15 см3. Экстракцию повторяют.
9.1.4. Объединенный экстракт упаривают без нагревания.
9.1.5. Добавляют 1 см3 раствора ФБК по п. 8.4, мешают и дают отстояться 15 минут.
9.1.6. Раствор упаривают до полного высыхания и добавляют 1 см3 изооктана.
9.1.7. Пробы озвучивают до разбиения белесого осадка, переносят в микроцентрифужные пробирки на 2 мл и центрифугируют при не менее 13000 об/мин (не менее 15700 g) течение 5 минут.
9.1.8. Около 800 мм3 чистой надосадочной жидкости переносят в виалу на 2 см3.
9.1.9. 1 мм3 полученной пробы вводят в хроматограф.
Подготовка проб совместного раствора 1,2-дипальмитоил-3-МХПД и 1,3-дипальмитоил-2-МХПД
9.2. Подготовка проб совместного раствора 1,2-дипальмитоил-3-МХПД и 1,3-дипальмитоил-2-МХПД осуществляется в следующем порядке:
9.2.1. В центрифужные пробирки на 15 см3 дозируют по 600 мм3 рабочих стандартных растворов, приготовленных по п. 7.5 и добавляют 100 мм3 совместного раствора 1,2-дипальмитоил-3-МХПД-d5 и 1,3-дипальмитоил-2-МХПД-d5 по п. 7.3.
9.2.2. Добавляют 600 мм3 диэтилового эфира и помещают в морозильную камеру с температурой -25 °С на 30 мин.
9.2.3. Не дожидаясь размораживания проб добавляют 500 мм3 метанольного гидроксида (метоксида) натрия по п. 8.1, закрывают крышками, мешают и помещают в морозильную камеру с температурой -25 °С на 16 часов (для предотвращения образования глицидола из МХПД в щелочной среде).
9.2.4. Не дожидаясь размораживания проб добавляют 600 мм3 подкисленного бромида натрия по п. 8.2.
9.2.5. Верхний слой упаривают без нагревания.
9.2.6. Добавляют 600 мм3 гексана, мешают, дают отстояться до расслоения (можно центрифугировать) и удаляют верхний слой. Процедуру повторяют.
9.2.7. Добавляют 900 мм3 смеси диэтилового эфира: этилацетата по п. 8.3, перемешивают и дают отстояться до расслоения. Верхний слой отбирают в новую центрифужную пробирку на 15 см3. Экстракцию повторяют еще раз.
9.2.8. Экстракты упаривают без нагревания.
9.2.9. Добавляют 1 см3 раствора ФБК по п. 8.4, мешают и дают отстояться 15 мин.
9.2.10. Раствор упаривают до полного высыхания и добавляют 1 см3 изооктана.
9.2.11. Пробы озвучивают до разбиения белесого осадка, переносят в микроцентрифужные пробирки на 2 мл и центрифугируют при не менее 13000 об/мин (не менее 15700 g).
9.2.12. Около 800 мм3 чистой надосадочной жидкости переносят в виалу и вводят в хроматограф.
Примечание: Пробы рекомендуется анализировать сразу или в день приготовления; при хранении более суток возможно выпадение кристаллического осадка фенилборной кислоты.
Подготовка пробы пищевого растительного масла
или животного жира для анализа
9.3. Подготовка пробы пищевого растительного масла или животного жира для анализа осуществляется в следующем порядке:
9.3.1. Подготовка пробы А:
9.3.1.1. Взвешивают 100 мг ± 20 мг масла в центрифужную пробирку на 15 см3.
9.3.1.2. Добавляют по 50 мм3 растворов внутренних стандартов 3-МХПД-d5 и 3-МБПД-d5, приготовленных по п. 7.1 и п. 7.2 соответственно.
9.3.1.3. Добавляют 600 мм3 диэтилового эфира (для растворения масла пробирку можно погреть) и перемешивают. Раствор помещают в морозильную камеру с температурой -25 °С на 30 мин (для предотвращения образования глицидола из МХПД в щелочной среде).
9.3.1.4. Не дожидаясь размораживания пробы добавляют 500 мм3 метанольного гидроксида (метоксида) натрия по п. 8.1, перемешивают и помещают в морозильную камеру с температурой -25 °С на 16 часов.
9.3.1.5. Не дожидаясь размораживания пробы добавляют 600 мм3 подкисленного бромида натрия по п. 8.2 для прекращения реакции.
9.3.1.6. Верхний слой упаривают без нагревания.
9.3.1.7. Добавляют 600 мм3 гексана и перемешивают. Дают отстояться до расслоения (можно центрифугировать) и удаляют верхний слой. Повторяют этот этап еще один раз.
9.3.1.8. Добавляют 900 мм3 смеси диэтилового эфира: этилацетата по п. 8.3, перемешивают и дают отстояться до расслоения. Верхний слой отбирают в другую центрифужную пробирку на 15 см3. Экстракцию повторяют еще раз.
9.3.1.9. Экстракты упаривают без нагревания.
9.3.1.10. Добавляют 1 см3 раствора ФБК по п. 8.4, мешают и дают отстояться около 15 мин.
9.3.1.11. Раствор упаривают до полного высыхания и добавляют 1 см3 изооктана.
9.3.1.12. Пробы озвучивают до разбиения белесого осадка, переносят в микроцентрифужные пробирки на 2 мл и центрифугируют при не менее 13000 об/мин (не менее 15700 g) в течение 5 минут.
9.3.1.13. Около 800 мм3 чистой надосадочной жидкости переносят в виалу и вводят в хроматограф.
9.3.2. Подготовка пробы Б:
9.3.2.1. Взвешивают около 100 мг (точность взвешивания ±20 мг) масла в центрифужную пробирку на 15 см3.
9.3.2.2. Добавляют 100 мм3 совместного раствора внутренних стандартов 1,2-дипальмитоил-3-МХПД-d5 и 1,3-дипальмитоил-2-МХПД-d5, приготовленного по п. 8.3.
9.3.2.3. Добавляют 600 мм3 диэтилового эфира (для растворения масла пробирку можно погреть) и перемешивают. Раствор помещают в морозильную камеру с температурой -25 °С на 30 мин (для предотвращения образования глицидола из МХПД в щелочной среде).
9.3.2.4. Не дожидаясь размораживания пробы добавляют 500 мм3 метанольного гидроксида (метоксида) натрия по п. 8.1, перемешивают и помещают в морозильную камеру с температурой -25 °С на 16 часов.
9.3.2.5. Не дожидаясь размораживания пробы добавляют 600 мм3 подкисленного бромида натрия по п. 8.2 для прекращения реакции.
9.3.2.6. Верхний слой упаривают без нагревания.
9.3.2.7. Добавляют 600 мм3 гексана и перемешивают. Дают отстояться до расслоения (можно центрифугировать) и удаляют верхний слой. Повторяют этот этап еще один раз.
9.3.2.8. Добавляют 900 мм3 смеси диэтилового эфира: этилацетата по п. 8.3, мешают и дают отстояться до расслоения. Верхний слой отбирают в другую центрифужную пробирку на 15 см3. Экстракцию повторяют еще раз.
9.3.2.9. Экстракты упаривают без нагревания.
9.3.2.10. Добавляют 1 см3 раствора ФБК по п. 8.4, мешают и дают отстояться около 15 мин.
9.3.2.11. Раствор упаривают на до полного высыхания и добавляют 1 см3 изооктана.
9.3.2.12. Пробы озвучивают до разбиения белесого осадка, переносят в микроцентрифужные пробирки на 2 мл и центрифугируют при не менее 13000 об/мин (не менее 15700 g) в течение 5 минут.
9.3.2.13. Около 800 мм3 чистой надосадочной жидкости переносят в виалу и вводят в хроматограф.
X. Хроматографические условия измерений
10.1. Хромато-масс-спектрометр включают и настраивают в соответствии с техническим руководством по его эксплуатации и устанавливают хроматографические параметры, представленные в таблице 2.
Таблица 2
Основные параметры работы хромато-масс-спектрометра
|
Температурная программа |
Начальная температура 60 °С, 5 °С/мин до 190 °С, 20 °С/мин до 280 °С, задержка 5 мин, по окончании 300 °С 5 мин |
|
Режим работы инжектора |
Без деления потока |
|
Температура инжектора |
250 °С |
|
Вводимый объем пробы |
1 мм3 |
|
Тип лайнера |
одинарный конический, для режима без деления потока, со стекловатой |
|
Газ-носитель |
Гелий |
|
Скорость потока газа- носителя |
1,2 см3/мин |
|
Режим потока |
Постоянный поток |
|
Температура интерфейса |
280 °С |
|
Температура источника |
230 °С |
|
Температура квадруполя |
150 °С |
Рекомендуется следующий порядок ввода пробы:
1. Не менее 5 раз промыть шприц гексаном или изооктаном;
2. 2 раза промыть шприц вводимой пробой;
3. Удалить пузырьки воздуха;
4. Ввести 1 мм3 пробы в хроматограф и начать анализ;
5. Не менее 5 раз промыть шприц гексаном или изооктаном.
Работу проводят в режиме мониторинга выбранных реакций, при этом устанавливают параметры для переходов, представленные в таблице 3. Первый ион-фрагмент соответствующего аналита используется для количественного расчета, второй является подтверждающим.
Таблица 3
Примеры параметров режима мониторинга выбранных реакций2
________
2 В зависимости от характеристик используемого оборудования указанные значения m/z ионов-фрагментов и энергии соударения могут отличаться от приведенных. Данные таблицы могут использоваться для тройного квадрупольного масс-детектора Agilent 7000С.
|
Аналит |
Ион-предшественник, m/z |
Ион-фрагмент, m/z |
Энергия соударения, еВ |
Временной сегмент |
|
3-МХПД |
196 |
147 |
10 |
1(15,0 - 18,4 мин.) |
|
196 |
91 |
25 |
||
|
3-МХПД-d5 |
201 |
150 |
10 |
|
|
201 |
93 |
25 |
||
|
2-МХПД |
196 |
104 |
25 |
2(18,4 - 19,5 мин.) |
|
196 |
91 |
15 |
||
|
2-МХПД-d5 |
201 |
107 |
10 |
|
|
201 |
104 |
20 |
||
|
3-МБПД |
242 |
147 |
10 |
3 (19,5-23,0 мин.) |
|
242 |
91 |
25 |
||
|
3-МБПД-d5 |
247 |
150 |
10 |
|
|
247 |
93 |
25 |
XI. Построение градуировочной кривой
11.1. При построении градуировочной зависимости для количественного определения 3-МХПД, 2-МХПД и глицидола анализируют рабочие стандартные градуировочные растворы различных уровней концентраций в указанных условиях, приготовленные по п. 7.4 и п. 7.5. Затем строят графики зависимости массы аналита во вводимой пробе от отношения площади хроматографического пика аналита к площади пика внутреннего стандарта для каждого фрагментного иона, используемого для количественного определения. Построение графиков может проводиться при помощи программы обработки данных ГЖХ-МС/МС или при помощи программы для работы с электронными таблицами.
Рассчитанная в ходе градуировки концентрация по фрагментарному иону, используемому для количественного определения, должна совпадать с теоретической в пределах 20 %.
Градуировочная зависимость считается приемлемой, если рассчитанное значение квадрата коэффициента корреляции для градуировочной кривой каждого фрагментного иона, используемого для количественного определения, составляет не менее 0,98.
Расчет содержания аналитов в исследуемом образце пищевого масла проводится следующим образом:
|
|
(1) |
|
|
(2) |
|
(3) |
|
|
(4) |
|
|
(5) |
где С3-МХПД(а) - содержание 3-МХПД в пробе А, мкг/г;
Сглицидола(а) - содержание глицидола в пробе А, мкг/г;
С3-МХПД(б) - содержание 3-МХПД в пробе Б, мкг/г;
С2-МХПД(б) - содержание 2-МХПД в пробе Б, мкг/г;
Сглицидола(б) - содержание глицидола в пробе Б, мкг/г;
G1 - масса 3-МХПД во вводимой в хромато-масс-спектрометр пробе А, рассчитанная по градуировке, мкг;
G2 - масса глицидола во вводимой в хромато-масс-спектрометр пробе А, рассчитанная по градуировке, мкг;
G3 - масса 3-МХПД во вводимой в хромато-масс-спектрометр пробе Б, рассчитанная по градуировке, мкг;
G4 - масса 2-МХПД во вводимой в хромато-масс-спектрометр пробе Б, рассчитанная по градуировке, мкг;
m - масса навески образца, г.
XII. Выражение результатов
12.1. Результат анализа представляет собой суммы свободных и этерифицированных форм 2-МХПД и 3-МХПД, рассчитанных по формулам 3 и 4 соответственно и выраженных через свободные формы, и сумму свободной и этерифицированных форм глицидола, рассчитанную по формуле 5 и выраженную через свободную форму.
Результат анализа представляют в виде:
|
С ± 0,01δ×С, при Р = 0,95; |
где С - результат, рассчитанный для пробы В с точностью до второго десятичного знака, мг/кг;
δ - значение относительной погрешности измерений, %.
XIII. Контроль качества результатов измерений
при реализации методики в лаборатории
13.1. Контроль качества результатов измерений в лаборатории при реализации методики осуществляют по ГОСТ Р ИСО 5725-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений», используя контроль стабильности среднеквадратического (стандартного) отклонения промежуточной прецизионности по 6.2.3 ГОСТ Р ИСО 5725-6 и показателя правильности по 6.2.4 ГОСТ Р ИСО 5725-6.
ХIV.Требования безопасности, охраны окружающей среды
14.1. При выполнении работ необходимо соблюдать следующие требования:
помещение лаборатории должно быть оборудовано общей приточно-вытяжной вентиляцией в соответствии с ГОСТ 12.4.021. Содержание вредных веществ в воздухе рабочей зоны не должно превышать гигиенических нормативов3;
требования техники безопасности при работе с химическими реактивами в соответствии с ГОСТ 12.1.007;
требования техники безопасности при работе с электроустановками в соответствии с ГОСТ Р 12.1.019.
Помещение лаборатории должно соответствовать требованиям пожарной безопасности в соответствии с ГОСТ 12.1.004 и быть оснащено средствами пожаротушения в соответствии с ГОСТ 12.4.009.
________
3 ГН 2.2.5.3532-18 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны», утвержденные постановлением Главного государственного санитарного врача Российской Федерации от 13.02.2018 № 25; ГН 2.2.5.2308-07 «Ориентировочные безопасные уровни воздействия (ОБУВ) вредных веществ в воздухе рабочей зоны», утвержденные постановлением Главного государственного санитарного врача Российской Федерации от 19.12.2007 № 89.
XV. Требования к оператору
15.1. Работу по указанной методике могут исполнять специалисты, обладающие необходимыми специальными навыками и познаниями в области хроматомасс-спектрометрии и аналитической химии.
XVI. Условия проведения измерений
16.1. При выполнении измерений соблюдают следующие условия: температуре воздуха (20 ± 5) °С, относительная влажность не более 80 % (условия измерений должны соответствовать требованиям, изложенным в паспортах или иных документах на используемое оборудование и материалы).
Нормативные и методические документы
1. Федеральный закон от 30.03.1999 № 52-ФЗ «О санитарно-эпидемиологическом благополучии населения».
2. Закон Российской Федерации от 07.02.1992 № 2300-1 «О защите прав потребителей».
3. ГН 2.2.5.3532-18 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны», утвержденные постановлением Главного государственного санитарного врача Российской Федерации от 13.02.2018 № 25.
4. ГН 2.2.5.2308-07 «Ориентировочные безопасные уровни воздействия (ОБУВ) вредных веществ в воздухе рабочей зоны», утвержденные постановлением Главного государственного санитарного врача Российской Федерации от 19.12.2007 № 89.
5. ГОСТ 12.0.004-90 Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения.
6. ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования.
7. ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности.
8. ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание.
9. ГОСТ Р 12.1.019-2009 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты.
10. ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике.