Государственное санитарно-эпидемиологическое
нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных
количеств
циазофамида в воде, почве, ботве и
клубнях картофеля, плодах томатов и
томатном соке методом высокоэффективной
жидкостной хроматографии
Методические указания
МУК 4.1.3133-13
Москва 2014
1. Разработаны сотрудниками «ГНУ Всероссийский НИИ защиты растений Россельхозакадемии» (В.И. Долженко, И.А. Цибульская, Т.Д. Черменская, А.С. Комарова); ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздрава России (М.С. Орлов).
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 29 октября 2013 г. № 3).
3. Утверждены врио руководителя Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главного государственного санитарного врача Российской Федерации А.Ю. Поповой 12 ноября 2013 г.
4. Введены впервые.
СОДЕРЖАНИЕ
|
УТВЕРЖДАЮ Врио
руководителя Федеральной службы А.Ю. Попова 12 ноября 2013 г. |
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств циазофамида
в воде, почве, ботве и клубнях картофеля, плодах
томатов и томатном соке методом высокоэффективной
жидкостной хроматографии
Методические указания
МУК 4.1.3133-13
Свидетельство о метрологической аттестации № 01.5.04.133/01.00043/2013.
Настоящие методические указания устанавливают порядок применения метода высокоэффективной жидкостной хроматографии для определения массовой концентрации циазофамида в воде в диапазоне концентраций 0,001 - 0,01 мг/дм3, в почве, клубнях картофеля, томатах и томатном соке - в диапазоне концентраций 0,01 - 0,1 мг/кг, в ботве картофеля - в диапазоне концентраций 0,05 - 0,5 мг/кг.
Методические указания носят рекомендательный характер.
Название действующего вещества по ИСО: циазофамид.
Название действующего вещества по ИЮПАК: 4-хлор-2-циано-N,N-диметил-5-р-толилимидазол-1-сульфонамид.
Структурная формула:
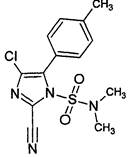
Эмпирическая формула: C13H13ClN4O2S.
Молекулярная масса: 324,78.
Химически чистое вещество представляет собой кристаллический порошок белого цвета без запаха.
Температура плавления: 153 °С.
Коэффициент распределения в системе н-октанол-вода KowlgP = 3,2 (20 °С).
Растворимость в воде (мг/дм3, 20 °С): 0,114.
Растворимость в органических растворителях (г/дм3, 20 °С): ацетон - 41,9; толуол - 5,3; гексан - 0,03; октанол - 0,25.
Краткая токсикологическая характеристика. Острая пероральная - ЛД50 > 5000 мг/кг массы тела. Острая токсичность: рыбы СК50 = 0,56 мг/л, дафнии ЭК50 = 0,19 мг/л.
Область применения. Системный фунгицид, класса цианоимидазола, применяется против фитофтороза и других заболеваний, вызываемых грибами рода Оомицетов на картофеле, томатах, огурцах; обладает высокой эффективностью против фениламидустойчивых грибов.
В России для циазофамида гигиенические нормативы не установлены.
1. Погрешность измерений
При соблюдении всех регламентированных условий проведения анализа в точном соответствии с данной методикой погрешность (и ее составляющие) результатов измерений при доверительной вероятности Р = 0,95 не превышает значений, приведенных в табл. 1, для соответствующих диапазонов концентраций.
Метрологические параметры
|
Объект анализа |
Диапазон определяемых концентраций, мг/кг (мг/дм3) |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), σr, % |
Показатель внутрилабораторной прецизионности, σRл, % |
Показатель воспроизводимости, σR, % |
Показатель точности* (границы относительной погрешности), ±δ, % |
|
Вода |
0,001 - 0,01 |
8 |
9 |
11 |
22 |
|
Почва |
0,01 - 0,1 |
9 |
11 |
12 |
24 |
|
Ботва картофеля |
0,05 - 0,5 |
9 |
11 |
12 |
24 |
|
Клубни картофеля |
0,01 - 0,1 |
7 |
9 |
12 |
23 |
|
Томаты |
0,01 - 0,1 |
9 |
11 |
12 |
24 |
|
Томатный сок |
0,01 - 0,1 |
7 |
9 |
12 |
23 |
|
*Соответствует расширенной неопределенности Uотн при коэффициенте охвата k = 2 |
|||||
Полнота извлечения циазофамида, стандартное отклонение,
доверительный интервал среднего результата для n
= 20, Р = 0,95
|
Анализируемый объект |
Предел обнаружения, мг/кг (мг/дм3) |
Диапазон определяемых концентраций, мг/кг (мг/дм3) |
Полнота извлечения, % |
Стандартное отклонение, S |
Доверительный интервал среднего результата, ± % |
|
Вода |
0,001 |
0,001 - 0,01 |
88,8 |
3,17 |
1,59 |
|
Почва |
0,01 |
0,01 - 0,1 |
92,4 |
4,18 |
2,09 |
|
Ботва картофеля |
0,05 |
0,05 - 0,5 |
82,6 |
4,30 |
2,15 |
|
Клубни картофеля |
0,01 |
0,01 - 0,1 |
82,0 |
2,39 |
1,19 |
|
Томаты |
0,01 |
0,01 - 0,1 |
89,4 |
4,09 |
2,05 |
|
Томатный сок |
0,01 |
0,01 - 0,1 |
87,4 |
1,77 |
0,89 |
2. Метод измерений
Методика основана на определении циазофамида методом высокоэффективной жидкостной хроматографии (ВЭЖХ) с использованием ультрафиолетового детектора (УФ) после его извлечения из образцов ацетонитрилом и последующей очистке на патроне для твердофазной экстракции (ТФЭ).
Идентификация циазофамида проводится по времени удерживания, количественное определение - методом абсолютной калибровки.
Избирательность метода обеспечивается сочетанием условий подготовки проб и хроматографирования.
3. Средства измерений, реактивы, вспомогательные
устройства и материалы
3.1. Средства измерений
|
Жидкостный хроматограф с быстросканирующим УФ-детектором, снабженный дегазатором, автоматическим пробоотборником и термостатом колонки |
|
|
Весы аналитические с пределом взвешивания до 210 г и пределом допустимой погрешности 0,2 мг |
|
|
Весы технические с пределом взвешивания до 400 г и допустимой погрешностью 0,1 г |
|
|
Колбы мерные на 10, 100 см3 |
|
|
Микродозаторы одноканальные переменного объема от 200 до 1000 мм3 и от 1 до 5 см3 |
|
|
Цилиндры мерные на 50 и 100 см3 |
Примечание. Допускается использование средств измерения с аналогичными или лучшими характеристиками.
3.2. Реактивы
|
Ацетонитрил, хч |
ТУ 6-09-3534-87 |
|
Вода для лабораторного анализа (бидистиллированная, деионизованная) |
|
|
н-Гексан, хч |
ТУ 6-09-3375-78 |
|
Кислота ортофосфорная, хч |
|
|
Магний серно-кислый семиводный, хч |
|
|
Натрий серно-кислый безводный, хч |
|
|
Натрий хлористый, чда |
|
|
Смесь № 1: гексан-этилацетат в соотношении 9:1 по объему |
|
|
Смесь № 2: гексан-этилацетат в соотношении 2:1 по объему |
|
|
Подвижная фаза для ВЭЖХ: смесь ацетонитрила и 0,005 М ортофосфорной кислоты в соотношении 50:50 |
|
|
Циазофамид, аналитический стандарт с содержанием основного вещества 98,2 % |
|
|
Этилацетат, хч |
ГОСТ 1138-84 |
Примечание. Допускается использование реактивов с более высокой квалификацией, не требующих дополнительной очистки растворителей.
3.3. Вспомогательные устройства и материалы
|
Аналитическая колонка для неионогенных среднеполярных соединений (100×2,1) мм, 1,7 мкм |
|
|
Аппарат для встряхивания проб |
ТУ 64-1-1081-73 |
|
Воронки лабораторные конусные |
|
|
Колбы круглодонные на шлифе вместимостью 25, 100 см3 |
|
|
Патроны для ТФЭ с гидрофильным слабокислотным сорбентом с постоянной активностью |
|
|
Пробирки полипропиленовые центрифужные с крышками объемом 50 см3 |
|
|
Ротационный вакуумный испаритель с мембранным насосом, обеспечивающим вакуум 10 мбар |
|
|
Стаканы химические вместимостью 150 см3 |
|
|
Фильтры бумажные быстрой фильтрации |
ТУ 6.091678-86 |
|
Центрифуга с максимальной рабочей частотой вращения 4000 об./мин |
|
Примечание. Допускается применение оборудования с аналогичными или лучшими техническими характеристиками.
4. Требования безопасности
4.1. При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007-76, требования по электробезопасности при работе с электроустановками по ГОСТ 12.1.019-09, а также требования, изложенные в технической документации на жидкостный хроматограф.
4.2. Помещение лаборатории должно быть оборудовано приточно-вытяжной вентиляцией, соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83. Содержание вредных веществ в воздухе не должно превышать ПДК (ОБУВ), установленных ГН 2.2.5.1313-03 и 2.2.5.2308-07.
Организация обучения работников безопасности труда - по ГОСТ 12.0.004-90.
5. Требования к квалификации операторов
Измерения в соответствии с настоящей методикой может выполнять специалист-химик, имеющий опыт работы методом высокоэффективной жидкостной хроматографии, ознакомленный с руководством по эксплуатации хроматографа, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений по п. 13.
6. Условия измерений
При выполнении измерений выполняют следующие условия:
- процессы приготовления растворов и подготовки проб к анализу проводят при температуре воздуха (20 ± 5) °С и относительной влажности не более 80 %;
- выполнение измерений на жидкостном хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к определению
7.1. Кондиционирование колонки
Перед началом анализа колонку кондиционируют в потоке подвижной фазы (0,1 - 0,2 см3/мин) до стабилизации нулевой линии.
7.2. Кондиционирование патрона для твердофазной экстракции
Патроны для ТФЭ с гидрофильным слабокислотным сорбентом с постоянной активностью промывают 2 см3 смеси № 2, затем 3 см3 смеси № 1.
7.3. Приготовление растворов
7.3.1. 0,005 М раствор ортофосфорной кислоты: (0,5 ± 0,01) г 98 %-й ортофосфорной кислоты помещают в мерную колбу объемом 1 дм3, растворяют в бидистиллированной воде и доводят объем до метки.
7.3.2. Для приготовления подвижной фазы смешивают ацетонитрил с 0,005 М раствором ортофосфорной кислоты в соотношении 50:50 по объёму, используя мерные цилиндры.
7.4. Приготовление основного и градуировочных растворов
7.4.1. Основной раствор с концентрацией 0,5 мг/см3: точную навеску циазофамида (50 ± 0,5) мг помещают в мерную колбу вместимостью 100 см , растворяют в ацетонитриле и доводят объем до метки ацетонитрилом.
7.4.2. Приготовление градуировочных растворов
Градуировочные растворы с концентрациями циазофамида 0,05, 0,1, 0,2, 0,5 и 1,0 мкг/см3 готовят методом последовательного разбавления по объему, используя раствор подвижной фазы (смесь ацетонитрила и 0,005 М ортофосфорной кислоты в соотношении 50:50).
7.4.2.1. Раствор № 1 с концентрацией 1,0 мкг/см3: в мерную колбу вместимостью 100 см3 вносят 0,2 см3 основного раствора и доводят до метки подвижной фазой.
7.4.2.2. Раствор № 2 с концентрацией 0,5 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 5,0 см3 раствора № 1 и доводят объем до метки подвижной фазой.
7.4.2.3. Раствор № 3 с концентрацией 0,2 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 2 см3 раствора № 1 и доводят объем до метки подвижной фазой.
7.4.2.4. Раствор № 4 с концентрацией 0,1 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 1 см3 раствора № 1 и доводят объем до метки подвижной фазой.
7.4.2.5. Раствор № 5 с концентрацией 0,05 мкг/см3: в мерную колбу вместимостью 10, см3 помещают 0,5 см3 раствора № 1 и доводят объем до метки подвижной фазой.
Основной раствор можно хранить в холодильнике при температуре 0 - 4 °С в течение 1 месяца, градуировочные растворы - в течение 2 дней.
При изучении полноты определения циазофамида в воде, почве, ботве и клубнях картофеля, томатах и томатном соке используют ацетонитрильные растворы вещества, приготовленные из основного раствора методом последовательного разбавления по объему ацетонитрилом.
7.5. Построение градуировочного графит
Для установления градуировочной характеристики (площадь пика концентрация циазофамида в растворе) в хроматограф вводят по 10 мм3 градуировочных растворов (не менее 3 параллельных измерений для каждой концентрации, не менее 4 точек по диапазону измеряемых концентраций). Затем измеряют площади пиков и строят график зависимости среднего значения площади пика от концентрации циазофамида в градуировочном растворе.
Методом наименьших квадратов рассчитывают градуировочный коэффициент (K) в уравнении линейной регрессии:
|
С = K⋅S, где |
S - площадь пика градуировочного раствора.
Градуировку признают удовлетворительной, если значение коэффициента линейной корреляции оказывается не ниже 0,99.
Градуировочную характеристику необходимо проверять при замене реактивов, хроматографической колонки или элементов хроматографической системы, а также при отрицательном результате контроля градуировочного коэффициента.
Градуировочную зависимость признают стабильной при выполнении следующего условия:
|
|
С - аттестованное значение массовой концентрации циазофамида в градуировочном растворе;
СK - результат контрольного измерения массовой концентрации циазофамида в градуировочном растворе;
λконтр. - норматив контроля градуировочного коэффициента, % (λконтр. = 10 % при Р = 0,95).
7.6.
Проверка хроматографического поведения циазофамида
на патроне для ТФЭ
В круглодонную колбу емкостью 10 см3 отбирают 1 см3 стандартного раствора циазофамида с концентрацией 1 мкг/см3. Отдувают растворитель током воздуха. Остаток растворяют в 1 см3 смеси № 1 и переносят на подготовленный патрон (п. 7.2). Колбу обмывают 1 см3 смеси № 1 и смыв тоже переносят на патрон. Промывают патрон 3 см3 смеси № 1, элюат отбрасывают. Затем элюируют циазофамид смесью № 2 со скоростью 1 - 2 капли в секунду. Отбирают фракции по 2 см3, упаривают досуха, растворяют в 1 см3 подвижной фазы (ацетонитрил - 0,005 М ортофосфорная кислота в соотношении 50:50) и анализируют по п. 9.4.
Фракции, содержащие циазофамид, объединяют и вновь анализируют.
Устанавливают уровень вещества в элюате, определяют полноту смывания с патрона и необходимый для очистки объем элюата.
Примечание. Проверку хроматографического поведения циазофамида на патронах следует проводить обязательно, поскольку профиль вымывания может изменяться при использовании новой партии патронов и растворителей.
8. Отбор проб и хранение
Отбор проб производится в соответствии с «Унифицированными правилами отбора проб сельскохозяйственной продукции, продуктов питания и объектов окружающей среды для определения микроколичеств пестицидов» (№ 2051-79 от 21.08.79), а также в соответствии с ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб»; ГОСТ 28168-89 «Почвы. Отбор проб». Отбор проб картофеля производится в соответствии с ГОСТ 7194-81 «Картофель свежий. Правила приемки и методы определения качества»; томатов - по ГОСТ 1725-85 «Томаты свежие».
Для длительного хранения пробы почвы подсушиваются при комнатной температуре в отсутствие прямого солнечного света. Сухие почвенные образцы могут храниться в течение года. Перед анализом сухую почву доводят до стандартной влажности, просеивают через сито с отверстиями диаметром 1 мм. Пробы овощей хранят до анализа в герметичной упаковке в морозильной камере при -18 °С. Перед анализом пробы измельчают, не размораживая.
9. Проведение определения
9.1. Экстракция циазофамида из воды
Пробу воды 100 см3 помещают в. делительную воронку вместимостью 250 см3, добавляют 30 см3 гексана и интенсивно встряхивают 2 - 3 мин. После полного разделения фаз, верхний органический слой собирают, к водному добавляют 30 см3 гексана и экстракцию повторяют. Объединенные органические фракции пропускают через воронку, содержащую безводный сульфат натрия и собирают в круглодонную колбу вместимостью 100 см3. Растворитель упаривают на ротационном вакуумном испарителе при температуре бани не выше 40 °С. Сухой остаток растворяют в 1 см3 подвижной фазы и 10 мм3 вводят в хроматограф.
9.2. Экстракция циазофамида из почвы, томатов, томатного
сока,
ботвы и клубней картофеля
Навеску измельченной культуры 10 г помещают в полипропиленовую центрифужную пробирку вместимостью 50 см3, последовательно добавляют 5 см3 воды (только для почвы), 10 см3 ацетонитрила, 8 г семиводного магния серно-кислого и 1 г хлористого натрия. Пробирку плотно закрывают и помещают в аппарат для встряхивания на 10 мин, затем центрифугируют в течение 10 мин при скорости 4000 об./мин. От верхнего ацетонитрильного слоя отбирают аликвоту 5 см3, переносят в круглодонную колбу вместимостью 25 см3. Растворитель упаривают на ротационном вакуумном испарителе при температуре бани не выше 40 °С. Сухой остаток подвергают очистке по п. 9.3.
9.3. Очистка на патроне для ТФЭ
Сухой остаток, полученный по п. 9.2, растворяют в 1 см3 смеси № 1, наносят на предварительно кондиционированный патрон (п. 7.2), колбу ополаскивают 1 см3 смеси № 1 и также наносят на патрон. Патрон промывают 3 см3 смеси № 1, элюат отбрасывают. Циазофамид элюируют 4 см3 смеси № 2, элюат собирают, упаривают досуха на ротационном вакуумном испарителе, остаток растворяют в подвижной фазе (1 см3 - почва, томаты, томатный сок, клубни картофеля; 5 см3 - ботва картофеля) и 10 мм3 вводят в хроматограф.
9.4. Условия хроматографирования
Ультраэффективный жидкостный хроматограф с быстросканирующим ультрафиолетовым детектором, снабженный дегазатором, автоматическим пробоотборником и термостатом колонки. Аналитическая колонка для неионогенных среднеполярных соединений (2,1×100) мм, 1,7 мкм. Температура колонки (30 ± 1) °С. Подвижная фаза: смесь ацетонитрила и 0,005 М ортофосфорной кислоты в соотношении 50:50. Скорость потока элюента: 0,2 см3/мин. Рабочая длина волны ультрафиолетового детектора 280 нм. Объем вводимой пробы 10 мм3.
10. Обработка результатов анализа
Количественное определение проводят методом абсолютной калибровки. Содержание циазофамида в пробе (X, мг/кг) вычисляют по формуле:
|
|
Sx - площадь пика циазофамида на хроматограмме испытуемого образца, мм2 (AU);
K - градуировочный коэффициент, найденный на стадии построения соответствующей градуировочной зависимости;
V - объём пробы, подготовленной для хроматографического анализа, см3;
Р - навеска анализируемого образца, г;
f - полнота извлечения циазофамида, приведенная в табл. 2, %.
Содержание остаточных количеств циазофамида в образце вычисляют как среднее из двух параллельных определений.
Образцы, дающие пики большие, чем стандартный раствор циазофамида с концентрацией 1,0 мкг/см3, разбавляют подвижной фазой для ВЭЖХ.
11.
Проверка приемлемости результатов
параллельных определений
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предела повторяемости:
X1, Х2 - результаты параллельных определений, мг/кг;
r - значение предела повторяемости (r = 2,8σr).
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
12. Оформление результатов
Результат анализа представляют в виде:
(![]() ± Δ) мг/кг при вероятности Р
= 0,95, где
± Δ) мг/кг при вероятности Р
= 0,95, где
![]() - среднее арифметическое результатов
определений, признанных приемлемыми, мг/кг;
- среднее арифметическое результатов
определений, признанных приемлемыми, мг/кг;
Δ - граница абсолютной погрешности, мг/кг;
|
|
|
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
В случае, если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
«содержание вещества в пробе менее нижней границы определения» (например: менее 0,01 мг/кг*, где * - 0,01 мг/кг - предел обнаружения циазофамида в томатах).
13. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений».
13.1. Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
13.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки С𝜕 должна удовлетворять условию:
|
С𝜕 = Δл, Х + Δл, Хʹ, где |
|
±Δл, Х, (±Δл, Хʹ) - характеристика погрешности (абсолютная погрешность) результатов анализа, соответствующая содержанию компонента в испытуемом образце (расчетному значению содержания компонента в образце с добавкой соответственно), мг/кг;
при этом:
|
Δл = ±0,84Δ, где |
|
Δ - граница абсолютной погрешности, мг/кг:
|
|
|
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры Kk рассчитывают по формуле:
|
Kk = Хʹ - Х - С𝜕, где |
|
Xʹ, X, С𝜕 - среднее арифметическое результатов параллельных определений (признанных приемлемыми по п. 11) содержания компонента в образце с добавкой, испытуемом образце, концентрация добавки соответственно, мг/кг.
Норматив контроля K рассчитывают по формуле:
|
|
|
Проводят сопоставление результата контроля процедуры (Kk) с нормативом контроля (K).
Если результат контроля процедуры удовлетворяет условию
|
(2) |
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры к их устранению.
13.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости.
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предел воспроизводимости
|
|
(3) |
X1, Х2 - результаты измерений в двух разных лабораториях, мг/кг;
R - предел воспроизводимости (в соответствии с диапазоном концентраций), %.
Определение остаточных количеств циазофамида в воде, почве, ботве и клубнях картофеля, плодах томатов и томатном соке методом высокоэффективной жидкостной хроматографии