Примечание: 1 - относится к сильнодействующим лекарственным средствам, применение и хранение которых должно проводиться с предосторожностью: хранение в закрытых шкафах, в сухом помещении.
2 - ГФ X - Государственная фармакопея СССР, X издание.
3 - "+" - температурный параметр, для контроля которого используют химическое соединение.
4 - используют любой из красителей, перечисленных в рецептуре 1,
5 - при использовании серы в качестве химического теста добавление красителя нецелесообразно, так как при плавлении вещества не происходит его смешение с красителем.
Химические тесты для контроля температурных параметров режимов работы воздушных стерилизаторов
|
№ п/п |
Наименование химического соединения |
Цвет, форма кристаллов, запах |
Нормативно-техническая документация |
Количество элемента, г |
Температурный параметр, подлежащий контролю, °С |
|
|
|
|
|||||
|
1. |
Левомицетин*2 |
Белый или белый со слабым желто-зеленым оттенком кристаллический порошок без запаха |
ГФ Х3, с. 371 |
100 |
+4 |
- |
|
2. |
Кислота винная |
Порошок белого цвета или прозрачные бесцветные кристаллы |
100,0 |
- |
+ |
|
|
3. |
Гидрохинон |
Бесцветные или светло-серые серебристые кристаллы |
100,0 |
- |
+ |
|
|
4. |
Тиомочевина |
Блестящие бесцветные кристаллы |
100,0 |
- |
+ |
|
Примечание:
1 - В состав химических тестов, используемых для контроля работы воздушных стерилизаторов, краситель не добавляют, т.к. указанные химические соединения изменяют свой цвет при достижении температуры плавления.
2 - Относится к сильнодействующим лекарственным средствам, применение и хранение которых должно проводиться с предосторожностью: хранение в закрытых шкафах, в сухом помещении.
3 - ГФ X - Государственная Фармакопея СССР X издание.
4 - "+" -температурный параметр, для контроля которого используют химическое соединение.
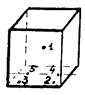
3.3.5.1. Самоконтроль работы паровых стерилизаторов (п. 2.6.1) проводят по следующей методике: упакованные химические тесты (п. 1.9) нумеруют и размещают в контрольные точки паровых стерилизаторов в соответствии с приложением 1. Работу парового стерилизатора прекращают через 7 минут стерилизационной выдержки.
Оценку показаний химических тестов проводят аналогично п. 3.3.3.
3.3.5.2. Самоконтроль работы воздушных стерилизаторов (п. 2.6.2) проводят по следующей методике: упакованные химические тесты (п. 1.9) нумеруют и размещают в контрольные точки воздушных стерилизаторов в соответствии с приложением 2. Работу воздушного стерилизатора прекращают через 30 минут стерилизационной выдержки.
Оценку показаний химических тестов проводят аналогично п. 3.3.3.
При обнаружении неудовлетворительных результатов химического контроля поступают, как указано в п. 2.8.
3.4. Термохимические индикаторы предназначены для оперативного контроля одного (температура) или совокупности нескольких параметров режимов работы паровых (температура, наличие остаточного воздуха, присутствие водяного насыщенного пара под избыточным давлением) и воздушных стерилизаторов (температура и время стерилизации).
3.4.1. Термохимический индикатор представляет собой полоску бумаги, на которую нанесена термоиндикаторная краска. Определение параметров, достигнутых в процессе стерилизации, основано на изменении цвета термоиндикаторной краски при достижении "температуры перехода", строго определенной для каждой краски.
3.4.2. Для контроля соблюдения параметров режимов работы паровых стерилизаторов могут быть использованы импортные средства контроля "Indicator Tape", "Sterikig А С", выпускаемые фирмой "Wipak Medical" (Финляндия), "Strate-line sterilization Monitor", выпускаемые фирмой "Propper Mfg. Co' Inc., L.I.C., N.Y. 1101", "Autoclave Indicator Tape", выпускаемые фирмой "3М Со" (США) и др., в соответствии с инструкцией по применению.
3.4.3. В таблице 3 приведен перечень термоиндикаторных красок, рекомендуемых для изготовления термохимических индикаторов, применяемых для контроля параметров режима работы воздушных стерилизаторов.
3.4.4. Методика подготовки термоиндикаторных красок к употреблению и меры предосторожности при работе с ними изложены в инструкции завода-изготовителя.
3.4.5. Термохимические индикаторы готовят следующим образом: термоиндикаторную краску тщательно размешивают, затем кистью тонким слоем наносят на листы белой писчей бумаги, дают высохнуть при комнатной температуре в течение 10 - 15 минут. Затем нарезают полоски размером 1×2 - 1×3 см. Термохимические индикаторы можно хранить до 1 года при комнатной температуре в местах, защищенных от света.
Термоиндикаторные
краски для контроля параметров режимов работы воздушного стерилизатора при
температуре ![]() °С, время выдержки - 60 минут
°С, время выдержки - 60 минут
|
Марка термоиндикаторной краски |
Минимально допустимая температура стерилизации, °С |
Цвет краски |
Характеристика термоиндикаторной краски |
|
|
исходный |
после воздействия |
|||
|
ТИК 29 |
170 |
светло-розовый |
темно-коричневый |
Свидетель достижения минимально допустимой температуры 170 °С |
|
ТИК 6 |
170 |
светло-зеленый |
коричневый |
Показатель длительности поддержания температуры 170 °С в течение 15 - 20 минут |
Примечание: Краски изготавливает Рижский лакокрасочный завод. Адрес завода: 226007, г. Рига, ул. Даугавпилс, 63/65.
3.4.6. Пронумерованные термохимические индикаторы размещают в контрольные точки воздушных стерилизаторов в соответствии с приложением 4 (приклеивают или прикрепляют на пакеты с контрольными тестами или на упаковку стерилизуемых изделий).
3.4.7. По окончании стерилизации термохимические индикаторы вынимают из стерилизатора и визуально определяют изменение их цвета.
3.4.7.1. При удовлетворительном результате контроля термохимические индикаторы должны изменить цвет до заданного, что свидетельствует о соблюдении параметров режима стерилизации.
3.4.7.2. При неудовлетворительном результате контроля изменение цвета термохимических индикаторов до заданного отсутствует, т.е., параметры режима стерилизации не соблюдены.
3.4.8. При обнаружении неудовлетворительных результатов термохимических индикаторов поступают, как указано в п. 2.8.
4. Бактериологический метод контроля
4.1. Бактериологический метод контроля предназначен для контроля эффективности работы стерилизаторов на основании выявления гибели спор тест-культур.
4.2. Бактериологический метод контроля работы стерилизаторов осуществляют с помощью биотестов.
4.3. Биотест представляет собой дозированное количество тест-культуры на носителе (или в нем), помещенном в упаковку. Упаковка предназначена для сохранения целостности носителя со спорами и предупреждения вторичного обсеменения после стерилизации.
4.3.1. Биотесты для контроля работы паровых стерилизаторов представляют собой флаконы из трубки стеклянной для лекарственных средств, ФИ/1-5 НС 1 ТУ 640709-10-88 (инсулиновые флаконы) или чашечки из алюминиевой фольги, содержащие высушенные споры тест-культуры Bacillus stearothermophilus BКM В-718.
4.3.2. Биотесты для контроля работы воздушных стерилизаторов представляют собой упакованные носители, перечисленные в п. 4.3.1, кроме того могут быть применены в качестве носителя диски из фильтровальной бумаги (ГОСТ 12026-76), содержащие высушенные споры тест-культуры Bacillus licheniformis штамм G.
4.4. Биотесты готовят бактериологические лаборатории дезинфекционных станций или санитарно-эпидемиологических станций в соответствии с методикой, изложенной в приложении 5.
4.5. Бактериологическая лаборатория выдает биотесты в пакетах из упаковочной бумаги (ОСТ 42-21-2-85), запечатанных в полиэтиленовые пакеты, которые служат для доставки биотестов.
4.6. Упакованные биотесты (п. 1.9) нумеруют и размещают в контрольные точки паровых (приложение 1) и воздушных (приложение 2) стерилизаторов.
4.7. По окончании стерилизации биотесты вынимают из стерилизатора, помещают в полиэтиленовый пакет и в тот же день доставляют в бактериологическую лабораторию с сопроводительным бланком.
4.8. Культивирование тест-культур после бактериологического контроля работы стерилизаторов осуществляют в соответствии с приложением 5.
4.9. При получении от бактериологической лаборатории извещения по телефону при заключении о неудовлетворительных результатах бактериологического контроля поступают, как указано в п. 2.8.
Стерилизатор разрешают использовать после устранения причин неудовлетворительной работы стерилизатора и получения удовлетворительных результатов бактериологического контроля.
5. Показатели качества работы стерилизаторов
5.1. Показателем качества работы стерилизаторов при соблюдении заданных условий их эксплуатации является соответствие отклонения температуры в различных точках камеры стерилизатора регламентированным, о чем свидетельствуют:
- показания максимальных термометров;
- изменение исходного состояния химических тестов (агрегатное состояние и цвет);
- изменение цвета термохимических индикаторов;
- отсутствие роста тест-культур в биотесте при культивировании после стерилизации.
6. Причины неудовлетворительных результатов контроля работы паровых и воздушных стерилизаторов
6.1. К причинам неудовлетворительных результатов контроля работы паровых и воздушных стерилизаторов следует отнести:
- неисправность стерилизатора (негерметичность камеры, дефекты прокладок, неисправность нагревательных элементов) или контрольно-измерительной аппаратуры (неисправность термометра, манометра);
- неполное удаление воздуха из камеры парового стерилизатора перед стерилизацией;
- избыточную, неравномерную или неправильную загрузку стерилизационной камеры;
- нарушение режима стерилизации;
- использование упаковочного материала, не предусмотренного ОСТ 42-21-2-85 -металлические пеналы (воздушная стерилизация), клеенка (паровая стерилизация);
- нарушение режима вентиляции (проникновение "загрязненного" воздуха через фильтр аппарата).
|
Начальник
Главного |
М.И. Наркевич |
Приложение 1
Расположение контрольных точек в паровых стерилизаторах
|
Емкость камеры стерилизатора, (тип аппарата, дм3) |
Число контрольных точек |
Расположение контрольных точек |
|
Описание |
||
|
до 100 |
5 |
для стерилизаторов прямоугольных; |
|
т. 1 - у загрузочной двери; |
||
|
т. 2 - у противоположной стенки (разгрузочной двери); |
||
|
свыше 100 до 750 включительно |
11 |
для стерилизаторов круглых вертикальных; |
|
т. 1 - в верхней части камеры; |
||
|
т. 2 - в нижней части камеры; |
||
|
свыше 750 |
13 |
для стерилизаторов круглых горизонтальных; |
|
т. 1 - у загрузочной двери; |
||
|
т. 2 - у противоположной стенки (разгрузочной двери); |
||
|
т. 3 - т. 13 - в центре стерилизационных коробок или внутри стерилизуемых упаковок, размещенных на разных уровнях, против часовой стрелки. |
Примечание: контрольные точки 1 и 2 находятся в стерилизационной камере вне стерилизуемых изделий.
Приложение 2
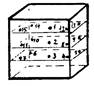
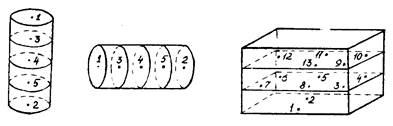
Расположение контрольных точек в воздушных стерилизаторах
|
Емкость камеры стерилизатора, тип аппарата, дм3 |
Число контрольных точек |
Расположение контрольных точек |
|
|
Описание |
Схема |
||
|
до 80 |
5 |
т. 1 - в центре камеры, т. 2, т. 3 - в нижней части камеры: справа (т. 2) и слева (т. 3) на одинаковом удалении от двери и задней стенки, т. 4, т. 5 - в нижней части камеры: справа (т. 4) и слева (т. 5) у двери |
|
|
свыше 80 однокамерные |
15 |
т. 1, т. 2, т. 3 - в центре камеры на трех уровнях сверху вниз, т. 4 - т. 15 - по углам на трех уровнях (т. 4 - т. 7 - низ, т. 8 - т. 11 - середина, т. 12 - т. 15 - верх), размещая против часовой стрелки |
|
|
свыше 80 двухкамерные |
30 |
аналогичным образом для каждой камеры |
|
Примечание: контрольные тесты помещают на расстоянии не менее 5 см от стенок стерилизационной камеры.
Приложение 3
Давление и соответствующая давлению температура
|
Давление, МПа |
(кгс/см2) |
Температура, °С |
|
0,00 |
0,0 |
99,1 |
|
0,05 |
0,5 |
110,8 |
|
0,06 |
0,6 |
112,7 |
|
0,07 |
0,7 |
114,6 |
|
0,08 |
0,8 |
116,3 |
|
0,09 |
0,9 |
118,0 |
|
0,10 |
1,0 |
119,6 |
|
0,11 |
1,1 |
121,2 |
|
0,12 |
1,2 |
122,7 |
|
0,13 |
1,3 |
124,1 |
|
0,14 |
1,4 |
125,1 |
|
0,15 |
1,5 |
126,8 |
|
0,16 |
1,6 |
128,1 |
|
0,17 |
1,7 |
129,3 |
|
0,18 |
1,8 |
130,6 |
|
0,19 |
1,9 |
131,8 |
|
0,20 |
2,0 |
132,9 |
|
0,21 |
2,1 |
134,0 |
|
0,22 |
2,2 |
135,1 |
|
0,23 |
2,3 |
136,1 |
|
0,24 |
2,4 |
137,2 |
|
0,25 |
2,5 |
138,2 |
Приложение 4
Изготовление химических тестов проводит специально подготовленный персонал.
Изготовление химического теста включает в себя следующие операции:
1. Взвешивание компонентов химического теста.
2. Приготовление состава химического теста.
3. Нарезка заготовок стеклянных трубок.
4. Запайка с одного конца стеклянных трубок.
5. Заполнение составом химического теста стеклянных трубок.
6. Запайка стеклянных трубок со второго конца.
7. Контроль линейных размеров химического теста и его герметичности.
8. Упаковка химического теста.
Взвешивание компонентов осуществляют на весах лабораторных общего назначения 4-го класса точности по ГОСТ 24104-88 с наибольшими пределами взвешивания 200 г. Допускаемая погрешность взвешивания 0,01 г. В случае наличия комкования используемые вещества предварительно размельчают и просеивают через сито с проволочной сеткой.
Процесс приготовления состава химического теста состоит в перемешивании
химического соединения с красителем (или без него) в соответствии с данными таблиц 1 и 2 раздела 3 методических указаний. Приготовление осуществляют в емкости из нержавеющей стали или покрытой эмалью, или фарфоровой ступке. Перемешивание проводят вручную в течение 10 - 30 минут (в зависимости от объема емкости) до получения однородной по окраске смеси или в смесителе, который представляет собой емкость из нержавеющей стали или покрытой эмалью, снабженную мешалкой с частотой вращения 40 - 70 об/мин. В этом случае вначале загружают половину необходимого количества соединения (например, бензойной кислоты), а затем все количество красителя (например, фуксина) и после этого вторую половину бензойной кислоты. Полученную смесь тщательно перемешивают не менее 30 минут до получения однородной по окраске смеси.
Нарезку заготовок стеклянных трубок начинают с нанесения надреза на трубке надфилем, напильником с металлической насечкой или специальным ножом из высокоуглеродистой стали или победита. Надрез производят без нажима, перпендикулярно оси трубки на 1/6 - 1/5 части длины ее окружности. Затем надрез слегка смачивают водой, трубку обертывают куском мягкой, но плотной ткани, берут двумя руками так, чтобы большие пальцы упирались в нее с противоположной надрезу стороны и стараются легким, но резким движением одновременно растянуть и согнуть трубку в месте надреза.
Полученные заготовки стеклянных трубок запаивают с одного конца в пламени газовой или жидкостной горелки.*
Заполнение составом химического теста стеклянных трубок производят методом уплотнения на 1/2 - 1/3 ее высоты. Рабочее место заполнения составом химического теста стеклянных трубок должно быть оснащено поддонами (пластмассовым или металлическим), куда попадает излишний состав теста при заполнении им стеклянных трубок. На рабочем месте заполнения стеклянных трубок составом химического теста не должно быть течи воды или парения.
Заполненные стеклянные трубки запаивают со второго конца в пламени газовой или жидкостной горелки.
После запайки проводят метрический контроль размеров стеклянной трубки с помощью штангенциркуля с ценой деления 0,1 мм или с помощью измерительной металлической линейки с ценой деления 1 мм. Для достижения стандартности тестов стенки трубок должны быть одинаковой толщины, длина трубок 45 ± 5 мм, наружный диаметр 4 ± 1 мм.
Перед упаковкой проводят сплошной контроль герметичности химических тестов, который осуществляют опусканием тестов в воду на 4 - 5 минут. Тесты с намокшим составом отбраковывают.
После проведения контроля на герметичность химические тесты в количестве 3050 штук заворачивают в оберточную или упаковочную бумагу. К каждой такой упаковке прикладывают упаковочный лист с указанием обозначения химического теста, срока годности и количества единиц в упаковке. Срок годности химического теста определяют по сроку годности химического соединения, который указан на этикетке.
Исходные химические вещества следует хранить в местах, недоступных для общего пользования, в герметичной таре, в темном сухом прохладном помещении.
Лекарственные средства списка Б должны храниться в отдельных запирающихся шкафах.
Химические тесты хранят в упаковке в сухих помещениях.
______________
* Для укупорки тестов нельзя использовать ватно-марлевые и резиновые пробки, так как они не обеспечивают герметичности теста, что приводит к растворению состава химических тестов в конденсате (контроль работы паровых стерилизаторов) и контакту стерилизуемых изделий с веществами, образующимися при нагревании состава химических тестов (контроль работы воздушных стерилизаторов).
Меры предосторожности
Рекомендованные химические соединения по предельно допустимым концентрациям в воздухе рабочей зоны относятся ко II - IV классу опасности (ГОСТ 12.1.007-76 "Вредные вещества. Классификация и общие требования безопасности").
Указанные соединения характеризуются общетоксическим и раздражающим действием на организм.
Работа с этими химическими соединениями требует изолированного помещения с эффективной общеобменной приточно-вытяжной вентиляцией, в том числе наличия местных вытяжных устройств (вытяжного шкафа).
К работе допускаются лица не моложе 18 лет, прошедшие соответствующий инструктаж по технике безопасности и мерам предосторожности при работе с химическими соединениями (ответственный за инструктаж - лицо, специально назначенное приказом администрации).
Персонал, изготавливающий химические тесты, проходит предварительный и периодический (раз в год) медицинские осмотры. Лица с повышенной чувствительностью к применяемым химическим соединениям, а также имеющие противопоказания по состоянию здоровья в соответствии с приказом МЗ СССР от 29 сентября 1989 г. № 555 "О совершенствовании системы медицинских осмотров трудящихся и водителей индивидуальных транспортных средств к работе не допускаются.
При изготовлении и запайке химических тестов необходимо не допускать рассыпания и пыления веществ. Следует избегать попадания их на кожу и слизистые оболочки. Все работы необходимо проводить в спецодежде (хлопчатобумажных халатах и резиновых перчатках). По окончании работы руки следует вымыть мылом и смазать кремом.
При отсутствии вытяжного шкафа работы следует проводить с использованием средств индивидуальной защиты органов дыхания (фильтрующий универсальный респиратор марки РУ-60 М или РПГ-67 с противогазовым патроном марки 4 "А"), защитных очков марок ПО-2, ПО-3, а также резиновых перчаток.
Первая помощь при случайном отравлении
При несоблюдении мер предосторожности у персонала могут возникнуть признаки отравления.
В этом случае пострадавшего следует вывести из рабочего помещения на свежий воздух, снять загрязненную спецодежду, обеспечить покой и согревание. При необходимости его следует направить в медпункт, для оказания врачебной помощи.
При попадании веществ на кожу их следует осторожно удалить ватным тампоном (не втирая и не размазывая), после чего место загрязнения обмыть струей воды с мылом в течение 5 - 10 минут.
При попадании любого вещества в глаза их следует немедленно обильно промыть водой в течение 5 - 10 минут и закапать 1 - 2 капли 30 % раствора альбуцида, а при болезненности - 1 - 2 капли 2 % раствора новокаина.
При раздражении дыхательных путей рекомендуется ингаляция водяным паром, 2 % раствором питьевой соды.
После этого выпить небольшими глотками теплое молоко с содой или боржоми.
При болезненном кашле следует использовать средства против кашля (таблетки от кашля, мукалтин).
При случайном проглатывании химических соединений необходимо выпить несколько стаканов воды или раствор марганцевокислого калия розового цвета (1:5000, 1:10000) и затем вызвать рвоту механическим раздражением корня языка. После рвоты рекомендуется обильное питье теплой воды или чая, применение взвеси активированного угля (2 столовые ложки на литр воды).
При сохранении признаков отравления следует обратиться за специальной медицинской помощью.
Приложение 5
1. Приготовление биотестов осуществляют в боксе, специально оборудованной комнате или шкафу с ламинарным потоком воздуха с соблюдением асептики.
2. Для проведения работы ежедневно помещения боксов и предбоксника подвергают тщательной обработке. Стены, пол, поверхности инвентаря протирают 3 % раствором перекиси водорода с 0,5 % моющего средства (Триас-А, Астра, Лотос). В случае обнаружения в воздухе грибов или споровых форм микроорганизмов влажную уборку проводят 6 % раствором перекиси водорода с 0,5 % выше перечисленных моющих средств.
Внутреннюю поверхность настольного бокса обрабатывают так же, как и помещение бокса. Через 45 - 60 минут после обработки в бокс вносят все необходимые для работы материалы, инструменты, кроме образцов изделия.
Перед внесением материалов в настольном боксе включают вентиляцию на время, достаточное для обеспечения полного обмена воздуха в нем.
За 1,5 - 2 часа до начала работы в боксе и предбокснике на 1 - 1,5 часа включают бактерицидные лампы.
Инструменты, посуду и спецодежду, используемые в работе, предварительно стерилизуют в паровом стерилизаторе. Металлические, стеклянные и тканевые изделия обрабатывают при следующем режиме: температура 132 ± 2 °С, время стерилизационной выдержки 20 минут; изделия из резины (перчатки и т.д.) - при температуре 120 + 2 °С в течение 45 минут.
Перед входом в бокс работники лаборатории тщательно моют руки теплой водой с мылом и щеткой, вытирают стерильным полотенцем, надевают в предбокснике на ноги бахилы, стерильные халаты, 4-слойные маски, шапочки, на руки - стерильные перчатки.
В процессе посева в боксе регулярно проверяют обсемененность воздуха. Для этого на рабочий стол ставят 2 чашки с питательным агаром, открывая их на 15 минут, затем чашки помещают в термостат при температуре 37 °С на 48 часов. Допускается рост не более трех колоний неспорообразующих сапрофитов.
В случае роста на чашках более 3 колоний проведение дальнейших работ в данном боксе запрещается, в нем дополнительно проводят тщательную обработку 6 % раствором перекиси водорода с 0,5 % моющих средств.
Приготовление растворов комплекса перекиси водорода с моющими средствами Триас-А, Астра, Лотос проводят в соответствии с расчетом, приведенным в таблице.
|
Состав рабочего раствора |
Количество пергидроля, воды, моющего средства, необходимое для приготовления 1 л раствора |
||||
|
Концентрация |
Пергидроля в зависимости от концентрации в нем перекиси водорода |
Воды, мл |
Моющего средства, г |
||
|
перекиси водорода |
моющего средства |
концентрация перекиси водорода в пергидроле |
количество пергидроля в мл на 1 л раствора |
||
|
3,0 |
0,5 |
30,0 |
100,0 |
895 |
|
|
|
|
31,0 |
97 |
898 |
|
|
|
|
32,0 |
94 |
901 |
5 |
|
|
|
33,0 |
90 |
905 |
|
|
6,0 |
0,5 |
30,0 |
200 |
795 |
|
|
|
|
31,0 |
194 |
801 |
|
|
|
|
32,0 |
188 |
807 |
5 |
|
|
|
33,0 |
180 |
815 |
|
При приготовлении раствора пергидроль приливают к раствору моющего средства.
При приготовлении растворов перекиси водорода и работе с 6 % растворами руки защищают резиновыми перчатками, а глаза - герметичными очками. При попадании пергидроля на кожу или в глаза их немедленно промывают обильным количеством водопроводной воды. При несоблюдении указанных правил техники безопасности могут развиваться дерматиты и конъюнктивиты. Запасы препарата хранят в местах, недоступных для общего пользования, в темной посуде, желательно, при температуре +4 °С.
3. Методика приготовления биотестов включает следующие этапы: подготовку тест-культуры, подготовку носителей (изготовление, мойка, стерилизация), обсеменение и высушивание носителей, упаковка биотестов, определение фактической плотности обсеменения носителей, контроль устойчивости тест-культуры на носителе, хранение приготовленных биотестов.
4. Тест-культуры Bacillus stearothermophilus BКM В-718 (контроль работы паровых стерилизаторов) и Bacillus licheniformis штамм G (контроль воздушных стерилизаторов) хранятся в музее культур ВНИИ профилактической токсикологии и дезинфекции МЗ СССР.
Адрес института: 117246, г. Москва, Научный проезд, д. 18.
5. Согласно "Положению о порядке учета, хранения, обращения, отпуска и пересылки культур бактерий, вирусов, риккетсий, грибов, простейших, микоплазм, бактериальных токсинов, ядов биологического происхождения" МЗ СССР, 1980 г., отпуск тест-культур производится по официальному требованию за подписью руководителя учреждения, скрепленному печатью учреждения, запрашивающего тест-культуру.
6. Биотесты приготавливают партиями. Партией считают определенное количество биотестов, приготовленных из исходной культуры в условиях производства, считающихся одинаковыми (получение спор на одной партии питательной среды, одновременное высушивание носителей и т.д.).
7. Методика приготовления питательных сред для получения спор тест-культур изложена в приложении 6.
8. Биотесты, используемые для контроля работы паровых и воздушных стерилизаторов, должны иметь стандартизированные показатели устойчивости тест-культур: время выживания тест-культур на носителе.
8.1. Устойчивость тест-культур должна быть воспроизводимой характеристикой от даты приготовления до истечения срока годности биотеста.
8.2. Каждую приготовленную партию биотестов проверяют соответственно на устойчивость тест-культур на носителе к водяному насыщенному пару под избыточным давлением (приложение 6, п. 19) или сухому горячему воздуху (приложение 7, п. 19).
8.2.1. Из каждой партии биотестов методом случайной выборки отбирают две группы биотестов в количестве не менее 10 образцов каждая.
8.2.2. Для определения показателей устойчивости одну группу биотестов подвергают действию стерилизующего агента на соответствие показателю времени выживания спор тест-культуры на 100 % исследуемых носителей, другую - времени гибели спор тест-культуры на 100 % исследуемых носителей.
8.2.3. При получении неудовлетворительных результатов испытаний биотестов (п. 8.2) проводят повторный контроль удвоенного количества биотестов от той же партии. Результаты повторных испытаний распространяют на всю партию.
8.3. Показатели устойчивости тест-культур в соответствии с приложением 6, п. 19 (7, п. 19) обеспечивают надежный контроль работы паровых и воздушных стерилизаторов на режимы стерилизации изделий медицинского назначения.
9. Биотесты маркируют. Маркировка включает следующие данные: наименование тест-культуры; метод стерилизации, который подлежит контролю; номер партии; число спор на носителе; показатели устойчивости тест-культур; срок годности; условия хранения; наименование организации-изготовителя.
К наборам биотестов следует прилагать методику культивирования тест-культур после стерилизации и методику обеззараживания инфицированного материала.
10. Биотесты хранят при комнатной температуре. Срок хранения 2 года от даты изготовления. По истечении этого срока проводят повторно контроль устойчивости.
11. Для культивирования тест-культур после определения устойчивости к соответствующему стерилизующему агенту (приложения 6, 7 п. 19) и после бактериологического контроля работы стерилизаторов (раздел 4) в бактериологической лаборатории с соблюдением правил асептических условий биотесты вынимают из упаковки. Во флаконы вносят 1 мл питательной среды и закрывают стерильными резиновыми пробками (№ 7, 5) с целью предупреждения высыхания питательной среды (в случае отсутствия резиновых пробок во флаконы вносят 5 мл питательной среды и закрывают стерильными ватно-марлевыми пробками), диски из фильтровальной бумаги и чашечки из фольги пинцетом, который обжигают в пламени, помещают в бактериологические пробирки с 5 мл питательной среды.
12. Методика приготовления питательных сред для культивирования тест-культур после стерилизации изложена в приложении 6.
13. Учет результатов бактериологического контроля проводят путем ежедневного визуального осмотра всех биотестов с питательной средой:
13.1. при использовании бульона Хоттингера, питательного бульона сухого, мясопептонного бульона, бульона из перевара кровяных сгустков, сухой питательной среды для контроля стерильности рост тест-культур определяют по помутнению питательной среды;
13.2. при использовании полусинтетической среды с индикатором феноловым красным рост тест-культур определяют по изменению красного цвета среды (рН 7,7 ± 0,1) на желто-оранжевый (рН 6,7 ± 0,1) за счет разложения глюкозы с образованием кислоты, под действием которой происходит изменение цвета индикатора. При использовании этой питательной среды необходимо обязательно использовать резиновые пробки (стерильные). Флаконы или бактериологические пробирки должны быть плотно закрыты резиновыми пробками (№ 7, 5 и № 12, 5 соответственно) с целью предупреждения ложного отрицательного результата (при наличии роста культуры отсутствует изменение цвета питательной среды - это происходит в результате улетучивания углекислого газа, образующегося при разложении глюкозы).
Биотесты считают стерильными, если помутнение (изменение цвета) питательной среды отсутствует, что указывает на гибель спор тест-культуры, т.е. на эффективность работы стерилизатора.
Предварительное заключение о неудовлетворительном результате контроля делают по помутнению (изменению цвета) питательной среды.
14. Окончательный ответ выдают после высева из пробирок (флаконов) с признаками роста и сравнения выделенной культуры с контролем. Рост других культур микроорганизмов относят за счет вторичного обсеменения.
15. В качестве контроля используют биотест, который не подвергают действию стерилизующего агента, и питательную среду, которую применяют для культивирования тест-культур после стерилизации. Контрольные тесты культивируют аналогично биотестам, которые подвергали действию стерилизующего агента.
16. При отсутствии роста тест-культур в контрольном биотесте, который не подвергали действию стерилизующего агента, устанавливают причины (нежизнеспособность тест-культуры, нарушение методики приготовления биотестов, питательных сред, культивирования). Результаты бактериологического исследования аннулируют и повторяют контроль работы аппарата.
17. После регистрации результатов бактериологического исследования лабораторную посуду (чашки Петри, пробирки, пипетки), пробки, посевы обеззараживают в паровых стерилизаторах под давлением при температуре (126 ± 2) °С (0,15 МПа (1,5 кгс/см2), время выдержки 120 минут.
18. При обнаружении неудовлетворительных результатов бактериологического контроля работы стерилизатора бактериологическая лаборатория извещает об этом по телефону руководителя медицинского учреждения и направляет заключение о результате бактериологического контроля.
Приложение 6
1. Штамм бактерий B. stearothermophilus BКM В-718 получен из Всесоюзной коллекции микроорганизмов Института биохимии и физиологии микроорганизмов АН СССР.
Подвижная термофильная палочка, по Граму окрашивается положительно, культивируется при температуре 55 ± 1 °С, исключающей развитие других широко распространенных микроорганизмов. Споры овальные, расположенные центрально. На мясопептонном бульоне (рН 7,3 ± 0,1) через 24 часа образует помутнение среды; на мясопептонном агаре (рН 7,3 ± 0,1) - слабо выпуклые колонии диаметром 2 - 4 мм с ровным краем. Штамм непатогенен для человека и животных.
2. Ампулу с лиофилизированной культурой B. stearothermophilus BKM В-718 вскрывают в асептических условиях следующим образом: тампоном ваты, смоченным этиловым спиртом, обрабатывают поверхность ампулы. Затем, держа ампулу в левой руке, нагревают ее запаянный конец в пламени. Чтобы на ампуле образовалась трещина, к накаленному концу ампулы прикладывают ватную пробку, смоченную стерильной водой. После этого металлическим инструментом (скальпель, пинцет) откалывают по трещине конец ампулы. Стерильной пастеровской пипеткой в ампулу вливают 0,2 мл стерильной водопроводной воды и оставляют в течение 30 минут при комнатной температуре. Суспензию отсасывают стерильной пастеровской пипеткой и переносят по 1 - 2 капли в две пробирки с бульоном (бульон Хоттингера, питательный бульон сухой, мясопептонный бульон), содержащим 0,5 % глюкозы.
Посевы инкубируют при температуре 55 ± 1 °С в течение 24 часов. При росте культуры происходит помутнение питательной среды.
3. Суточную бульонную культуру бактериологической петлей или пастеровской пипеткой (по 1 - 2 капли) пересевают в 10 - 20 пробирок на скошенную питательную среду (агар Хоттингера, питательный агар сухой, мясопептонный агар).
Посевы инкубируют при температуре 55 ± 1 °С в течение 24 часов.
4. Для получения спор культуру, выращенную на твердой питательной среде (п. 3), смывают 5 мл стерильной водопроводной воды и переносят во флаконы вместимостью 250 - 500 мл (10 - 20 штук в зависимости от потребности в суспензии спор), содержащие соответственно 100 - 200 мл скошенного картофельно-пептонного агара. Для обсеменения каждого флакона в зависимости от его вместимости используют суспензию, смытую с 1 - 2 пробирок соответственно. Взвесь покачиванием флакона равномерно распределяют по поверхности среды. Флаконы закрывают ватно-марлевыми пробками с бумажными колпачками и инкубируют при температуре 55 ± 1 °С в течение 10 - 12 суток в наклонном положении (под углом 45°) агаром вверх. Для создания достаточной влажности в термостат помещают открытые емкости с водой (до 2 л на термостат вместимостью 80 л).
5. На 7, 10 и 12 сутки культуру проверяют на интенсивность спорообразования (выборочно 2 - 3 флакона). Культуру забирают петлей с верхнего, среднего и нижнего участков агара, все три пробы растирают вместе на одном предметном стекле, распределяя тонким слоем. Мазок фиксируют, окрашивают по Граму или генцианвиолетом (по Синеву). Окрашенные препараты промывают водопроводной водой, подсушивают и микроскопируют с иммерсионной системой - споры имеют вид неокрашенных пустот, находящихся внутри клеток. Исследуют 3 - 5 полей зрения, подсчитывают количество спор, выражая в процентах. Достаточным количеством считают 80 - 90 % спор в поле зрения от общего числа клеток.
6. После завершения споруляции культуру осторожно при помощи шпателя из проволоки смывают с поверхности агара 5 - 10 мл стерильной дистиллированной воды в зависимости от вместимости флакона.
7. Для удаления вегетативных клеток и получения чистых спор суспензию прогревают при температуре от 65 до 70 °С в течение 30 минут в водяной бане (экспозиция с момента достижения температуры на термометре, опущенном в контрольную аналогичную емкость с таким же количеством воды), центрифугируют в стерильных центрифужных пробирках, закрытых ватно-марлевыми пробками, с частотой вращения 33,33 с-1 (2000 об/мин) в течение 15 минут. Надосадочную жидкость осторожно удаляют, а осадок трехкратно промывают стерильной дистиллированной водой, чередуя с центрифугированием, после чего споры суспендируют в стерильной дистиллированной воде в соотношении 1:1 по объему.
8. Суспензию спор хранят в холодильнике при температуре 4 °С в стерильных пробирках, закрытых ватно-марлевыми пробками с резиновыми колпачками. Срок хранения - 2 года.
9. Для получения культур производят высев из пробирок с суспензией, заложенной на хранение, в пробирки с бульоном (бульон Хоттингера, питательный бульон сухой, мясопептонный бульон), содержащим 0,5 % глюкозы (2 пробирки), и далее получают споры по описанной выше методике (приложение 6, п. 2 - 7).
10. Чистоту культур на всех этапах культивирования контролируют высевом на чашки Петри с агаром (агар Хоттингера, питательный агар сухой, мясопептонный агар).
11. Для определения титра жизнеспособных спор 0,1 мл исходной суспензии пипеткой переносят в пробирку, содержащую 0,9 мл стерильной дистиллированной воды (разведение 10-1). Подобным образом последовательно получают десятикратные разведения исходной суспензии, меняя пипетку для каждого разведения. Из трех последовательных десятикратных разведений исходной суспензии (предел разведения зависит от титра полученных спор - ориентировочно от 10-5 до 10-7) производят высев по 0,1 мл суспензии на поверхность трех чашек Петри с агаром (агар Хоттингера, сухой питательный агар).
Чашки Петри инкубируют при температуре 55 ± 1 °С в течение 48 часов, после чего производят подсчет выросших колоний.
12. Титр жизнеспособных спор в исходной суспензии определяют как среднее арифметическое числа колоний с учетом разведения исходной суспензии и объема пробы для посева.
Пример расчетов. Предположим, что при посеве на три чашки Петри с агаром суспензии в разведении 1:100000 (10-5 подсчитано 140, 110 и 134 колонии. Аналогичные высевы из разведений 1:1000000 (10-6) привели к образованию 12, 14 и 16 колоний; 1:10000000 (10-7) - 5, 3 и 7 колоний.
Вычисляем общее число колоний, найденных во всех трех чашках Петри соответствующих разведений:
1:100000 (10-5) 140 + 110 + 130 = 348
1:1000000 (10-6) 12 + 14 + 16 = 42
1:10000000 (10-7) 5 + 3 + 7 = 15
Среднее число колоний на чашках составит для разведения
1:100000 (10-5) 384 : 3 = 128
1:1000000 (10-6) 42 : 3 = 14
1:10000000 (10-7) 15 : 3 = 5
Из расчета посевной дозы (0,1 мл на каждую чашку) вычисляем титр жизнеспособных спор в 1 мл исходной суспензии с учетом разведений, далее находим средние арифметические числа колоний:
128 × 10 × 105 = 12,8 × 107.
14 × 10 × 106 = 14,0 × 107.
5 × 10 × 107 = 50,0 × 107.
Таким образом, титр исходной суспензии составит:
(12,8 + 14,0 + 50,0) × 107 : 3 = 25,6 × 107 = 2,5 × 108 спор в 1 мл.
13. В качестве носителей тест-культуры B. stearothermophilus ВКМ В-718 используют флаконы или чашечки из алюминиевой фольги. Флаконы тщательно моют, закрывают ватно-марлевыми пробками. Из алюминиевой фольги вырезают диски размером 14 мм, неоточенной стороной карандаша в дисках делают вдавление - луночку.
14. Подготовленные носители стерилизуют паровым методом при
температуре 120 + 2 °С, время стерилизационной выдержки 45 минут или воздушным
методом при температуре ![]() °C, время стерилизационной выдержки 60
минут в упаковке из бумаги (чашечки из фольги раскладывают в чашки Петри).
°C, время стерилизационной выдержки 60
минут в упаковке из бумаги (чашечки из фольги раскладывают в чашки Петри).
15. Стерильные носители с помощью дозатора пипеточного (ТУ 64-1-3329-81) обсеменяют суспензией спор тест-культуры B.stearothermophilus ВКМ В-718 из расчета 5 × 105 - 5 × 106 спор на носитель, что достигается нанесением на каждый носитель 0,02 мл суспензии спор в дистиллированной воде титром 2,5 × 107 - 2,5 × 108 спор в 1 мл.
16. Носители высушивают в термостате при температуре 37 ± 1 °С или эксикаторе под осушителем (силикагель, хлористый кальций) при комнатной температуре в течение 24 часов.
17. Каждый биотест закладывают в пакет из упаковочной бумаги (флаконы) или заворачивают в бумагу упаковочную по типу порошка (чашечки из алюминиевой фольги), раскладывают в полиэтиленовые пакеты, маркируют и запаивают.
18. Для определения фактической плотности обсеменения используют не менее трех биотестов от каждой партии. Во флаконы вносят 1,0 мл стерильной дистиллированной воды (чашечки из алюминиевой фольги отмывают в широкогорлых пробирках с бусами в 10 мл) и встряхивают в течение 10 минут на аппарате для встряхивания жидкостей с последующим высевом на поверхность трех чашек Петри с агаром (агар Хоттингера, питательный агар сухой) по 0,1 мл суспензии из трех последовательных десятикратных разведений исходной суспензии. Среднее число спор в биотесте должно быть в соответствии с приложением 6, п. 15.
19. Определение устойчивости спор тест-культуры B. stearothermophilus BКM В-718 к действию водяного насыщенного пара под избыточным давлением проводят при температуре 120 + 2 °С.
Биотесты в упаковочной бумаге помещают в стерилизационной коробке в камеру парового стерилизатора (ВК-75). После набора давления в водопаровой камере (0,11 ± 0,1) МПа (1,1 ± 0,1 кгс/см2) проводят продувку парового стерилизатора (вытеснение воздуха паром из камеры парового стерилизатора) в течение 10 минут (при открытом спускном кране и давление в стерилизационной камере от 0,01 до 0,02 МПа (от 0,1 до 0,2 кгс/см2). После продувки доводят давление пара в стерилизационной камере до 0,11 ± 0,01 МПа (1,1 ± 0,1 кгс/см2), температура 120 + 2 °С и через 5 минут времени выдержки (время выживания спор тест-культуры на носителе) с момента установления давления спускают пар. Для уменьшения времени воздействия пара до и после экспозиции подъем давления проводят максимум в течение 8 минут, спуск - в течение 3 минут.
Аналогичное исследование проводят в течение 15 минут времени выдержки (время гибели спор тест-культуры на носителе).
Контроль температуры осуществляют максимальными термометрами.
По окончании времени выдержки биотесты вынимают из стерилизатора. Культивирование тест-культуры B.stearothermophilus BКM В-718 осуществляют в бактериологической лаборатории в соответствии с приложением 5, п. 11 - 19.
Таблица
Показатели устойчивости тест-культуры B. stearothermophilus ВКМ В-718 на носителе к действию водяного насыщенного пара под избыточным давлением
|
Наименование показателя |
Норма |
Метод исследования |
|
Устойчивость спор тест-культуры B. stearothermophilus ВКМ В-718 на носителе к действию водяного насыщенного пара под избыточным давлением при температуре (120 + 2) °С в паровом стерилизаторе |
|
|
|
- время выживания |
не менее 5 минут для каждого образца |
по приложению 6, п. 19 |
|
- время гибели |
не более 15минут для каждого образца |
по приложению 6, п. 19 |
20. Партию биотестов считают годной для использования, если показатели устойчивости спор тест-культуры B. stearothermophilus ВКМ В-718 соответствуют требованиям, указанным в таблице.
21. Для культивирования тест-культуры B. stearothermophilus ВКМ В-718 используют питательный бульон (бульон Хоттингера, питательный бульон сухой, мясопептонный бульон, бульон из перевара кровяных сгустков, полусинтетическую среду с индикатором феноловым красным), содержащий 0,5 % глюкозы.
Биотесты инкубируют при температуре 55 ± 1 °С в течение 7 суток.
22. Учет результатов бактериологического контроля проводят в соответствии с приложением 5, п. 13 - 18.
Приложение 7
1. Штамм бактерий B. licheniformis G выделен в 1984 году при контроле стерильности чашек Петри, подвергнутых стерилизации сухим горячим воздухом.
Подвижная грамположительная палочка. Споры эллиптические, расположенные центрально. На мясопептонном бульоне (рН 7,3 ± 0,1) через 48 часов инкубации при температуре 37 ± 1 °С образует помутнение среды, на поверхности сухую пленку; на мясопептонном агаре (рН 7,3 ± 1) - слабо выпуклые сухие колонии вытянутой звезчатой формы с неровными краями диаметром 4 - 6 мм, врастающие в питательную среду. Штамм непатогенен для человека и животных.
2. Ампулу с лиофилизированной культурой B. licheniformis штамм G вскрывают аналогично приложению 5, п. 2. Суспензию переносят по 1 - 2 капли в две пробирки с бульоном (бульон Хоттингера, питательный бульон сухой, мясопептонный бульон), содержащим 0,5 % глюкозы.
Посевы инкубируют при температуре 37 ± 1 °С в течение 24 часов. При росте культуры происходит помутнение питательной среды.
3. Суточную бульонную культуру бактериологической петлей или пастеровской пипеткой по 1 - 2 капли пересевают в 10 - 20 пробирок на скошенную питательную среду (агар Хоттингера, питательный агар сухой, мясопептонный агар).
Посевы инкубируют при температуре 37 ± 1 °С в течение 24 часов.
4. Для получения спор культуру, выращенную на твердой питательной среде (п. 3), бактериологической петлей пересевают в бактериологические пробирки или смывают 5 мл стерильной дистиллированной воды и переносят во флаконы вместимостью 250 - 500 мл (10 - 20 штук в зависимости от потребности в суспензии спор), содержащие соответственно 100 - 200 мл скошенного агара (пшеничный агар, картофельный агар).
Для обсеменения каждого флакона в зависимости от его вместимости используют суспензию, смытую с 1 - 2 пробирок соответственно. Взвесь покачиванием флакона равномерно распределяют по поверхности среды. Флаконы закрывают ватномарлевыми пробками с бумажными колпачками и инкубируют при температуре 37 ± 1 °С в течение 7 - 10 суток в наклонном положении (под углом 45°) агаром вверх.
5. На 5, 7 и 10 сутки культуру проверяют на интенсивность спорообразования (выборочно 2 - 3 флакона) аналогично приложению 6, п. 5.
6. После завершения споруляции культуру осторожно при помощи шпателя из проволоки смывают с поверхности агара 5 - 10 мл стерильной дистиллированной воды в зависимости от вместимости флакона.
7. Для удаления вегетативных клеток полученную суспензию прогревают при температуре от 65 до 70 °С в течение 30 минут в водяной бане (экспозиция с момента достижения температуры на термометре, опущенном в контрольную аналогичную емкость с таким же количеством воды), центрифугируют в стерильных центрифужных пробирках, закрытых ватно-марлевыми пробками, с частотой вращения 33,33 с-1 (2000 об/мин) в течение 15 минут. Далее надосадочную жидкость осторожно удаляют, а осадок трехкратно промывают стерильной дистиллированной водой, чередуя с центрифугированием, после чего споры суспендируют в стерильной дистиллированной воде в соотношении 1:1 по объему.
8. Суспензию спор хранят в холодильнике при температуре 4 °С в стерильных пробирках, закрытых ватно-марлевыми пробками с резиновыми колпачками. Срок хранения 2 года.
9. Для получения культуры производят высев из пробирок с суспензией, заложенной на хранение, в пробирки с бульоном (бульон Хоттингера, питательный бульон сухой, мясопептонный бульон), содержащим 0,5 % глюкозы (2 пробирки), и далее получают споры по описанной выше методике (приложение 7, п. 2 - 7).
10. Чистоту культуры на всех этапах культивирования контролируют высевом на чашки Петри с агаром (агар Хоттингера, мясопептонный агар).
11. Для определения титра жизнеспособных спор 0,1 мл исходной суспензии пипеткой переносят в пробирку, содержащую 0,9 мл стерильной дистиллированной воды (разведение 10-1). Подобным образом последовательно получают десятикратные разведения культуры, меняя пипетку для каждого разведения. Из трех последовательных десятикратных разведений исходной суспензии (предел разведения зависит от титра полученных спор - ориентировочно от 10-7 до 10-9) производят высев по 0,1 мл суспензии на поверхность трех чашек Петри с агаром (агар Хоттингера, мясопептонный агар).
Чашки Петри инкубируют при температуре 37 ± 1 °С в течение 48 часов, после чего производят подсчет выросших колоний.
12. Титр жизнеспособных спор в исходной суспензии определяют аналогично приложению 6, п. 12.
13. В качестве носителей тест-культуры B. licheniformis штамм G используют флаконы, чашечки из алюминиевой фольги или диски из фильтровальной бумаги. Флаконы тщательно моют, закрывают ватно-марлевыми пробками. Из алюминиевой фольги, фильтровальной бумаги вырезают диски диаметром 14 мм, неоточенной стороной карандаша в дисках из алюминиевой фольги делают вдавление - луночку.
14. Подготовленные носители стерилизуют паровым методом при
температуре 120 + 2 °С, время стерилизационной выдержки 45 минут или воздушным
методом при температуре ![]() °С, время стерилизационной выдержки 60
минут в упаковке из бумаги (чашечки из фольги и диски из фильтровальной бумаги
раскладывают в чашки Петри).
°С, время стерилизационной выдержки 60
минут в упаковке из бумаги (чашечки из фольги и диски из фильтровальной бумаги
раскладывают в чашки Петри).
15. Стерильные носители с помощью дозатора пипеточного (ТУ 64-1-3329-81) обсеменяют суспензией спор тест-культуры B. licheniformis штамм G из расчета 5 × 102 - 5 × 103 спор на носитель, что достигается нанесением на каждый носитель 0,02 мл суспензии спор в дистиллированной воде титром 2,5 × 104 - 2,5 × 105 спор в 1 мл.
16. Носители высушивают в термостате при температуре 37 ± 1 °С или эксикаторе под осушителем (силикагель, хлористый кальций) при комнатной температуре в течение 24 часов.
17. Каждый биотест закладывают в пакет из упаковочной бумаги (флаконы без ватно-марлевых пробок во избежание возгорания) или заворачивают в бумагу упаковочную по типу порошка (чашечки из алюминиевой фольги, диски из фильтровальной бумаги), раскладывают в полиэтиленовые пакеты, маркируют и запаивают.
18. Для определения фактической плотности обсеменения используют не менее трех биотестов от каждой партии. Во флаконы вносят 1,0 мл стерильной дистиллированной воды (чашечки из алюминиевой фольги и диски из фильтровальной бумаги отмывают в бактериологических пробирках с бусами в 1 мл) и встряхивают в течение 10 минут на аппарате для встряхивания жидкостей с последующим высевом на поверхность трех чашек Петри с агаром (агар Хоттингера, питательный агар сухой, мясопептонный агар) по 0,1 мл суспензии из исходной суспензии и двух последовательных десятикратных разведений исходной суспензии. Среднее число спор в биотесте должно быть в соответствии с приложением 7, п. 15.
19. Определение устойчивости спор тест-культуры B. licheniformis штамм G к действию сухого горячего воздуха проводят при температуре 160 ± 2 °С в воздушных стерилизаторах с принудительной циркуляцией и скоростью движения воздуха более 1 м/с, которые обеспечивают допустимые перепады от номинального значения температуры (ГП-20, ГП-40, ГП-80).
Биотесты в упаковочной бумаге помещают на полку воздушного стерилизатора, предварительно прогретого до 160 °С при исследовании биотестов с использованием чашечек из алюминиевой фольги и дисков из фильтровальной бумаги и до 140 °С при использовании флаконов в качестве носителей. Стерилизатор закрывают и после достижения температуры 160 ± 2 °С начинают отсчет времени воздействия. Через 4 минуты времени выдержки (время выдерживания спор тест-культуры на носителе) аппарат отключают.
Аналогичное исследование проводят в течение 30 минут времени выдержки (время гибели спор тест-культуры на носителе).
Контроль температуры осуществляют по наружному термометру.
По окончании времени выдержки биотесты вынимают из стерилизатора. Культивирование тест-культуры B. licheniformis штамм G осуществляют в бактериологической лаборатории в соответствии с приложением 5, п. 11 - 19.
20. Партию биотестов считают годной для использования, если показатели устойчивости спор тест-культуры B. licheniformis штамм G соответствуют требованиям, указанным в таблице.
Таблица
|
Наименование показателя |
Норма |
Метод исследования |
|
Устойчивость спор тест-культуры B. licheniformis штамм G на носителе к действию сухого горячего воздуха температурой 160 ± 2 °С в воздушном стерилизаторе |
|
|
|
- время выживания |
не менее 4 минут для каждого образца |
по приложению 7, п. 19 |
|
- время гибели |
не более 30 минут для каждого образца |
по приложению 7, п. 19 |
21. Для культивирования тест-культуры B. licheniformis штамм G используют питательный бульон (бульон Хоттингера, питательный бульон сухой, мясопептонный бульон, бульон из перевара кровяных сгустков, полусинтетическую среду с индикатором феноловым красным), содержащий 0,5 % глюкозы, среду питательную для контроля стерильности.
Биотесты инкубируют при температуре 37 + 1 °С в течение 7 суток.
22. Учет результатов бактериологического контроля проводят в соответствии с приложением 5, п. 13 - 18.
Приложение 8
Методика приготовления питательных сред
1. Картофельный агар
|
Пептон |
- 5,0 г |
|
Мел |
- 1,0 г |
|
Агар |
- 25,0 г |
|
Картофельная вода |
- 1000 мл |
|
рН 7,1 ± 0,1 |
|
Сырой картофель (из расчета 200 г очищенного картофеля на 1 л водопроводной воды) тщательно моют, очищают от кожуры и глазков, нарезают мелкими ломтиками, заливают водопроводной водой и кипятят 30 минут после закипания (молодой картофель употреблять нельзя). Отвар отстаивают и фильтруют в холодном состоянии через ватно-марлевый фильтр. Доводят объем фильтрата до первоначального. Устанавливают рН 7,1 ± 0,1. Добавляют пептон и агар. Нагревают, помешивая, до полного расплавления агара, фильтруют через ватно-марлевый фильтр, после чего добавляют мел. Разливают по флаконам, стерилизуют при 120 °С в течение 30 минут. После стерилизации среду во флаконах скашивают.
2. Пшеничный агар
|
Пшеничная крупа "Артек" (или "Полтавская") |
- 500 г |
|
Агар |
- 25,0 г |
|
Дистиллированная вода |
- 1000 мл |
|
рН 7,3 ± 0,1 |
|
Пшеничную крупу "Артек" (или "Полтавская") заливают дистиллированной водой. Через 12 часов настой аккуратно сливают, не выжимая, доводят до первоначального объема, добавляют агар и растапливают на водяной бане или автоклаве (текучим паром 1 час). Остывший агар выкладывают на противень и срезают осадок. Агар растапливают на водяной бане, постоянно помешивая. Устанавливают рН 7,3 ± 0,1. Разливают в нужную посуду. Стерилизуют текучим паром по 1 часу в течение 3 суток. После стерилизации среду скашивают.
3. Бульон Хоттингера
|
Мясной перевар по Хоттингеру до разведения аминного азота |
от 140 до 160 мг% |
|
Натрий хлористый |
- 5,0 г |
|
Глюкоза |
- 5,0 г |
|
Дистиллированная вода |
- до 1000 мл |
|
рН 7,3 ± 0,1 |
|
Смешивают мясной перевар по Хоттингеру с водой в таком соотношении, чтобы в среде содержалось от 140 до 160 мг% аминного азота, добавляют хлористый натрий. Кипятят на слабом огне с закрытой крышкой 10 минут до полного растворения соли. Если есть выкипание, доводят объем до первоначального дистиллированной водой. Устанавливают рН 7,3 ± 0,1, кипятят повторно. Фильтруют, прибавляют глюкозу. Разливают в стерильную посуду. Стерилизуют при 110 °С в течение 30 минут.
4. Агар Хоттингера
|
Мясной перевар по Хоттингеру (аминный азот) |
140 - 160 мг% |
|
Натрий хлористый |
- 5,0 г |
|
Агар |
- 20,0 г |
|
Дистиллированная вода |
- до 1000 мл |
|
рН 7,3 ± 0,1 |
|
К готовому бульону Хоттингера (содержание аминного азота от 140 до 160 мг%) без глюкозы добавляют агар и кипятят на слабом огне при постоянном помешивании до полного расплавления. Фильтруют и стерилизуют при температуре 120 °С в течение 30 минут.
5. Полусинтетическая среда с индикатором феноловым красным
|
Аммоний фосфорнокислый однозамещенный (NH4H2PО4) |
- 1,0 г |
|
Магнии сернокислый (MgSО4) |
- 0,2 г |
|
Калий хлористый (KCl) |
- 0,2 г |
|
Глюкоза |
- 5,0 г |
|
Феноловый красный |
- 0,02 г |
|
Бульон Хоттингера (содержание аминного азота от 140 до 160 мг%) |
- 200 |
|
Дистиллированная вода |
- 800 мл |
|
рН 6,7 ± 0,1 |
|
Компоненты смешивают и растворяют при нагревании на водяной бане. Доводят ph до 7,7 ± 0,1, разливают во флаконы и стерилизуют при 110 °С в течение 30 минут.
6. Питательный бульон сухой (Дагестанский НИИ питательных сред, г. Махачкала, ул. Леваневского, 24)
|
Триптический гидролизат кильки |
- 10,05 г |
|
Натрия хлорид |
- 4,95 г |
|
рН 7,1 ± 0,1 |
|
Готовят согласно прописи на этикетке. Для приготовления бульона с глюкозой добавить 0,5 % глюкозы.
7. Питательный агар сухой (Дагестанский НИИ питательных сред, г. Махачкала, ул. Леваневского, 24)
|
Гидролизат кильки |
- 17,9 г |
|
Агар |
- 11,2 г |
|
Натрия хлорид |
- 5,9 г |
|
рН 7,3 ± 0,1 |
|
Готовят согласно прописи на этикетке.
8. Среда питательная для контроля стерильности сухая. (Предприятие Центрального НИИВС им. И.М. Мечникова, 143422, Моск. обл., Красногорский р-н, с. Петрово-Дальнее)
|
Ферментативный гидролизат казеина неглубокой степени расщепления |
- 15,0 г |
|
Витаминный препарат ЭКД |
- 5,0 г |
|
Натрий хлористый |
- 6,4 г |
|
Глюкоза медицинская |
- 5,0 г |
|
Тиогликолят натрия |
- 0,5 г |
|
Цестеин дигидрохлорид |
- 0,75 г |
|
Агар порошкообразный |
- 0,6 г |
|
Натрий углекислый |
- 0,5 - 0,95 г |
|
рН 7,0 ± 0,1 |
|
Готовят согласно прописи на этикетке.
9. Бульон из перевара кровяных сгустков
Методика приготовления изложена в "Справочнике по микробиологическим ивирусологическим методам исследований" (Под ред. М.О. Биргера. М., Медицина, 1982). Для приготовления бульона с глюкозой добавить 0,5 % глюкозы.
СОДЕРЖАНИЕ