МИНИСТЕРСТВО ПРИРОДНЫХ РЕСУРСОВ И ЭКОЛОГИИ
РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральная служба по гидрометеорологии
и мониторингу окружающей среды (Росгидромет)
|
РУКОВОДЯЩИЙ ДОКУМЕНТ |
РД |
МАССОВАЯ КОНЦЕНТРАЦИЯ ЦИАНИДОВ В ВОДАХ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
ФОТОМЕТРИЧЕСКИМ МЕТОДОМ С НИКОТИНАМИДОМ
Ростов-на-Дону
2011
Предисловие
1 РАЗРАБОТАН Государственным учреждением Гидрохимический институт (ГУ ГХИ)
2 РАЗРАБОТЧИК Л.В. Боева, канд. хим. наук, О.А. Михайленко, Е.Л. Селютина
3 СОГЛАСОВАН с УМЗА Росгидромета 25.04.2011
ГУ «НПО «Тайфун»
4 УТВЕРЖДЕН Заместителем Руководителя Росгидромета 26.04.2011
5 АТТЕСТОВАН ГУ ГХИ, свидетельство об аттестации методики выполнения измерений № 520.01.00175-2011 от 11.09.2010 г.
6 ЗАРЕГИСТРИРОВАН ЦМТР ГУ НПО «Тайфун» за номером РД 52.24.520-2011 от 29.04.2011
7 РАЗРАБОТАН ВПЕРВЫЕ
СОДЕРЖАНИЕ
Введение
Цианиды (соединения, содержащие группу - CN) в бытовых сточных водах отсутствуют и попадают в природные воды исключительно в результате загрязнения промышленными сточными водами, преимущественно металлургических, химических производств и рудообогатительных фабрик. Неорганические цианиды являются весьма токсичными как для человека, так и для гидробионтов, что и обусловливает необходимость контроля их содержания в природных и сточных водах.
Различают цианиды свободные, простые, комплексные, а также органические (циангидрины и нитрилы). По степени токсичности они неравноценны. Наибольшую опасность представляют свободные и простые цианиды (т.е. циановодородная кислота HCN, цианид-ион, малорастворимые в нейтральной среде, но растворимые при подкислении, цианиды металлов) и наиболее лабильные комплексные цианиды.
Циановодородная кислота является весьма слабой (рН = 9,2), вследствие чего растворимые простые цианиды существуют в природных водах преимущественно в виде недиссоциированной формы HCN.
Комплексные цианиды имеют разную степень устойчивости и, соответственно, их опасность различна Комплексные соединения кобальта (III), железа и некоторых других металлов (платина, палладий, золото) настолько прочны, что в природной среде выделение из них свободных цианидов маловероятно. Трансформация этих соединений преимущественно идет по пути окисления в малотоксичные цианаты, которые далее окисляются до СО2 и N2 или NH4+. В разбавленных растворах при достаточно большой интенсивности ультрафиолетового излучения комплексы железа могут медленно разлагаться с выделением HCN; однако, скорость выделения циановодородной кислоты, как правило, не превышает скорости биохимического окисления, поэтому накопления свободных цианидов из этого источника не происходит. Менее прочные комплексные цианиды металлов при определенных условиях могут высвобождать свободные цианиды сравнительно легко и поэтому представляют большую опасность.
В связи с вышеизложенным, определение цианидов обычно включает раздельное определение токсичных (свободных и легкоразлагаемых) цианидов и их общего содержания, включающего и трудноразлагаемые комплексные цианиды. Однако даже при этом наиболее прочные цианиды (например, цианокобальтат) разлагаются лишь частично. Полное разложение цианокобальтата достигается лишь при УФ-облучении, однако, поскольку он встречается редко и в малых количествах, потерями за счет неполного разложения обычно пренебрегают.
Органические цианосодержащие соединения - нитрилы, устойчивые в водных растворах циангидрины или цианамиды, как правило, в условиях определения неорганических цианидов не разлагаются с выделением HCN или CN- и их определение проводится специфическими методами.
Понижение концентрации цианидов в воде связано в основном с процессами окисления, биохимической деградации и осаждения в виде трудно растворимых соединений.
Предельно допустимая концентрация (ПДК) цианидов в воде водных объектов хозяйственно-питьевого и культурно-бытового водопользования составляет 0,07 мг/дм3, так и рыбохозяйственного значения - 0,05 мг/дм3.
РУКОВОДЯЩИЙ ДОКУМЕНТ
МАССОВАЯ КОНЦЕНТРАЦИЯ ЦИАНИДОВ В ВОДАХ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
ФОТОМЕТРИЧЕСКИМ МЕТОДОМ С НИКОТИНАМИДОМ
Дата введения - 2011-06-01
1 Область применения
1.1 Настоящий руководящий документ устанавливает методику выполнения измерений (далее - методика) массовой концентрации токсичных (легкоразлагаемых) и общих цианидов в диапазоне от 0,005 мг/дм3 до 0,300 мг/дм3 в пробах природных и очищенных сточных вод фотометрическим методом.
1.2 Допускается выполнение измерений в пробах с массовой концентрацией цианидов, превышающей 0,300 мг/дм3 при разбавлении пробы дистиллированной водой, таким образом, чтобы концентрация цианидов в разбавленной пробе находилась в пределах указанного в 1.1 диапазона концентраций.
1.3 Настоящий руководящий документ предназначен для применения в лабораториях, осуществляющих анализ природных и очищенных сточных вод.
2 Нормативные ссылки
В настоящем руководящем документе использованы ссылки на следующие нормативные документы:
ГОСТ 12.1.005-88 ССБТ. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 ССБТ. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 17.1.5.04-81 Охрана природы - Гидросфера. Приборы и устройства для отбора, первичной обработки и хранения проб природных вод. Общие технические условия
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ Р 51592-2000 Вода. Общие требования к отбору проб
МИ 2881-2004 Рекомендация. ГСИ. Методики количественного химического анализа. Процедуры проверки приемлемости результатов анализа.
Примечание - Ссылки на остальные нормативные документы, приведены в разделах 4, Б.3, Б.4 (приложение Б) и В.3, В.4 (приложение В).
3 Приписанные характеристики погрешности измерения
3.1 При соблюдении всех регламентируемых методикой условий проведения измерений характеристики погрешности результата измерения с вероятностью 0,95 не должны превышать значений, приведенных в таблице 1.
Таблица 1 - Диапазон измерений массовой концентрации цианидов, значения характеристик погрешности и ее составляющих при принятой вероятности Р = 0,95
|
Диапазон измерений массовой концентрации цианидов, X, мг/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости) σr, мг/дм3 |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) σR, мг/дм3 |
Показатель правильности (границы систематической погрешности) ± Δс мг/дм3 |
Показатель точности (границы погрешности) ± Δ, мг/дм3 |
|
От 0,005 до 0,300 включ. |
0,0001 + 0,011 ∙ Х |
0,0008 + 0,020 ∙ Х |
0,0003 + 0,027 ∙ Х |
0,0014 + 0,046 ∙ Х |
При выполнении измерений в пробах с массовой концентрацией цианидов свыше 0,300 мг/дм3 после соответствующего разбавления границы погрешности измерений (± Δ) массовой концентрации цианидов в исходной пробе находят по формуле
± Δ = (± Δ1) ∙ η, (1)
где ± Δ1 - показатель точности измерения массовой концентрации в разбавленной пробе, рассчитанный согласно таблице 1;
η - степень разбавления.
Предел обнаружения цианидов составляет 0,003 мг/дм3.
3.2 Значения показателя точности методики используют при:
- оформлении результатов измерений, выдаваемых лабораторией;
- оценке деятельности лабораторий на качество проведения измерений;
- оценке возможности использования результатов измерений при реализации методики в конкретной лаборатории.
4 Средства измерений, вспомогательные устройства, реактивы, материалы
4.1 Средства измерений, вспомогательные устройства
При выполнении измерений применяют следующие средства измерений и другие технические средства:
4.1.1 Фотометр или спектрофотометр любого типа (КФК-3, КФК-2, СФ-46, СФ-56 и др.).
4.1.2 Весы лабораторные высокого (II) класса точности по ГОСТ Р 53228-2008.
4.1.3 Весы лабораторные среднего (III) класса точности по ГОСТ Р 53228-2008 с наибольшим пределом взвешивания 200 г.
4.1.4 рН-метр или иономер любого типа (рН-150, рН-155, Экотест-2000, Анион-410 и др.) с комплектом электродов.
4.1.5 Государственный стандартный образец состава водных растворов ионов роданида (тиоцианат-ионов) ГСО 7958-2001 (далее - ГСО).
4.1.6 Колбы мерные 2 класса точности по ГОСТ 1770-74 исполнения 2, 2а вместимостью: 25 см3 - 12 шт., 50 см3 - 1 шт., 100 см3 - 4 шт., 200 см3 - 1 шт., 1000 см3 - 1 шт.
4.1.7 Пипетки градуированные 2 класса точности, исполнения 1, 2 по ГОСТ 29227-91 вместимостью: 1 см3 - 5 шт., 2 см3 - 2 шт., 5 см3 - 5 шт., 10 см3 - 4 шт.
4.1.8 Пипетки с одной отметкой 2 класса точности исполнения 2 по ГОСТ 29169-91 вместимостью: 10 см3 - 2 шт., 20 см3 - 1 шт.
4.1.9 Бюретка не ниже 2 класса точности по ГОСТ 29251-91 вместимостью: 25 см3 - 1 шт.
4.1.10 Цилиндры мерные исполнения 1,3 по ГОСТ 1770-74 вместимостью: 10 см3 - 4 шт., 25 см3 - 1 шт., 100 см3 - 2 шт.
4.1.11 Установка из стекла для отдувки цианидов: круглодонная колба К-1 вместимостью 250 см3 с конусным шлифом 29/32, насадка к склянке для промывания газов типа СН с конусным шлифом 29/32, каплеуловитель, склянка для промывания газов исполнения СПЖ вместимостью 250 см3 по ГОСТ 25336-82, поглотительный сосуд (цилиндр мерный исполнения 1 по ГОСТ 1770-74 вместимостью 10 см3 и пипетка Пастера по ТУ 9464-001-52876351-2000, либо поглотитель с пористой пластиной, либо поглотитель Рихтера).
4.1.12 Стаканы В-1, ТХС, по ГОСТ 25336-82 вместимостью: 50 см3 - 2 шт., 100 см3 - 2 шт., 400 см3 - 1 шт., 600 см3 - 4 шт., 1000 см3 - 1 шт.
4.1.13 Мензурки по ГОСТ 1770-74 вместимостью: 250 см3 - 1 шт., 1000 см3 - 1 шт.
4.1.14 Колбы конические Кн-2, ТХС по ГОСТ 25336-82 с притертыми пробками вместимостью: 25 см3 - 12 шт., 250 см3 - 3 шт.
4.1.15 Стаканчики для взвешивания (бюксы) СВ-19/9, СВ-24/10 по ГОСТ 25336-82 - 4 шт.
4.1.16 Палочки стеклянные по ГОСТ 27460-87 - 2 шт.
4.1.17 Шпатель по ГОСТ 9147-80.
4.1.18 Микрокомпрессор аквариумный с расходом не менее 0,5 дм3/мин.
4.1.19 Вакуумный насос любого типа (далее - вакуум-насос); например, водоструйный насос по ГОСТ 25336-82.
4.1.20 Баня водяная терморегулируемая, например, баня четырехместная водяная ЛАБ ТБ-4.
4.1.21 Ротаметр РМФК-0,1 ГУЗ по ТУ 4213-002-48318935-99 или другого типа с диапазоном измерения воздушного потока от 100 см3/мин.
4.1.22 Эксикатор по ГОСТ 25336-82.
4.1.23 Холодильник бытовой.
4.1.24 Шкаф сушильный общелабораторного назначения.
4.1.25 Электроплитка с закрытой спиралью по ГОСТ 14919-83.
4.1.26 Посуда полиэтиленовая (полипропиленовая) для хранения проб вместимостью 0,25 дм3.
4.1.27 Посуда стеклянная (в том числе темного стекла) для хранения проб и растворов вместимостью 0,25 дм3, 0,5 дм3, и 1,0 дм3.
Примечание - Допускается использование других типов средств измерений, посуды и оборудования, в том числе импортных, с характеристиками не хуже, чем у приведенных в 4.1.
4.2 Реактивы и материалы
4.2.1 Калий роданистый (тиоцианат калия) по ГОСТ 4139-75, ч.д.а. (при отсутствии ГСО).
4.2.2 Калий железосинеродистый (гексацианоферрат (III) калия) по ГОСТ 4206-75, ч.д.а.
4.2.3 Натрия гидроокись (гидроксид натрия) по ГОСТ 4328-77, ч.д.а.
4.2.4 Кислота соляная по ГОСТ 3118-77, х.ч.
4.2.5 Кислота уксусная по ГОСТ 61-75, ч.д.а.
4.2.6 Натрий углекислый кислый (гидрокарбонат натрия) по ГОСТ 4201-79, х.ч.
4.2.7 Натрий уксуснокислый 3-водный (ацетат натрия) по ГОСТ 199-78, ч.д.а.
4.2.8 Калий двухромовокислый (дихромат калия) по ГОСТ 4220-75, х.ч.
4.2.9 Цинк уксуснокислый 2-водный (ацетат цинка) по ГОСТ 5823-78, ч.д.а.
4.2.10 Кадмий уксуснокислый 2-водный (ацетат кадмия) по ГОСТ 5824-79, ч.д.а.
4.2.11 Калий йодистый (иодид калия) по ГОСТ 4232-74, ч.д.а.
4.2.12 Натрий серноватистокислый (тиосульфат натрия) 5-водный, по ГОСТ 27068-86, ч.д.а.
4.2.13 Крахмал растворимый по ГОСТ 10163-76, ч.д.а.
4.2.14 Никотиновой кислоты амид (никотинамид) по ТУ 6-09-08-852-82, ч.
4.2.15 Натрий N-хлор-n-толуолсульфамид (хлорамин Т) 1-водный, по ТУ 6-09-11-1218-79, ч. или натрия гипохлорит, полученный в соответствии с приложением А.
4.2.16 Медь (II) сернокислая 5-водная (сульфат меди) по ГОСТ 4165-78, ч.д.а.
4.2.17 Олово (II) хлорид, 2-водное по ТУ 6-09-5393-88, ч.
4.2.18 Кальций окись по ГОСТ 8677-76, ч.
4.2.19 Вода дистиллированная по ГОСТ 6709-72.
4.2.20 Универсальная индикаторная бумага по ТУ 6-09-1181-76.
Примечание - Допускается использование реактивов, изготовленных по другой нормативной и технической документации, в том числе импортных, с квалификацией не ниже указанной в 4.2.
4.3 Дополнительное оборудование, реактивы и материалы для получения гипохлорита натрия
4.3.1 Воронка капельная по ГОСТ 25336-82 вместимостью: 50 см3 - 1 шт.
4.3.2 Склянки для промывания газов СН-1 по ГОСТ 25336-82 вместимостью: 100 см3 - 2 шт.
4.3.3 Склянка для промывания газов СН-2 по ГОСТ 25336-82 вместимостью: 200 см3 - 1 шт.
4.3.4 Колба для перегонки (колба круглодонная с отводом), тип КП, исполнение 2 по ГОСТ 25336-82 вместимостью 100 см3 - 1 шт.
4.3.5 Калий марганцовокислый (перманганат калия) по ГОСТ 20490-75, ч.д.а.
5 Метод измерений
Выполнение измерений массовой концентрации цианидов фотометрическим методом основано на превращении цианидов под действием активного хлора в хлорциан, реагирующий с никотинамидом с образованием интенсивно окрашенного полиметинового красителя.
Максимум оптической плотности красителя наблюдается при 400 - 402 нм.
Выделение из воды и концентрирование легкоразлагаемых цианидов и циановодородной кислоты проводится путем отдувки HCN из горячего раствора в присутствии уксуснокислого буферного раствора (рН 4) и поглощении ее щелочью.
Общие цианиды выделяют из воды и концентрируют путем отдувки из сильнокислой среды в присутствии сульфата меди и хлорида олова (II).
6 Требования безопасности, охраны окружающей среды
6.1 При выполнении измерений массовой концентрации цианидов в пробах природных и очищенных сточных вод соблюдают требования безопасности, установленные в национальных стандартах и соответствующих нормативных документах.
6.2 По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся к 2-му и 3-му классам опасности по ГОСТ 12.1.007.
6.3 Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005.
6.4 Получение гипохлорита натрия, а также концентрирование и определение цианидов следует проводить при включенной вытяжной вентиляции.
7 Требования к квалификации операторов
К выполнению измерений и обработке их результатов допускаются лица со средним профессиональным образованием, имеющие стаж работы в лаборатории не менее 2 лет и освоившие методику.
8 Условия выполнения измерений
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
- температура окружающего воздуха (22 ± 5) °С;
- атмосферное давление от 84,0 до 106,7 кПа (от 630 до 800 мм рт.ст.);
- влажность воздуха не более 80 % при 25 °С;
- напряжение в сети (220 ± 10) В;
- частота переменного тока в сети питания (50 ± 1) Гц.
9 Отбор и хранение проб
Отбор и хранение проб производят в соответствии с ГОСТ 17.1.5.05 и ГОСТ Р 51592. Оборудование для отбора проб должно соответствовать ГОСТ 17.1.5.04 и ГОСТ Р 51592. Объем отбираемой пробы должен быть не менее 0,25 дм3.
Пробы помещают в стеклянную или полиэтиленовую посуду с плотно закрывающейся пробкой. Если анализ не может быть произведен в день отбора пробы, ее консервируют, добавляя на каждые 100 см3 пробы 3 см3 раствора ацетатов кадмия и цинка и 2 см3 раствора гидроксида натрия, 2 моль/дм3. Хранить пробу до анализа следует при температуре 3 - 6 °С не более 5 суток. Незаконсервированную пробу допустимо хранить при температуре 3 - 6 °С не более суток.
10 Подготовка к выполнению измерений
10.1 Приготовление растворов и реактивов
10.1.1 Раствор ацетата кадмия и ацетата цинка
Растворяют 100 г ацетата кадмия и 100 г ацетата цинка в 1 дм3 дистиллированной воды. Раствор устойчив.
10.1.2 Ацетатный буферный раствор, рН 4,0 ± 0,1
Помещают в мензурку вместимостью 1 дм3 136 г ацетата натрия, добавляют 500 см3 дистиллированной воды, затем приливают 360 см3 ледяной уксусной кислоты и перемешивают стеклянной палочкой до полного растворения. Доводят раствор в мензурке дистиллированной водой до объема 1000 см3 и вновь тщательно перемешивают. Проверяют рН буферного раствора по рН-метру, корректируя при необходимости добавлением ацетата натрия или уксусной кислоты.
Раствор хранят в плотно закрытой склянке темного стекла в течение месяца при комнатной температуре и в течение 3 месяцев при температуре от 4 °С - 6 °С.
10.1.3 Раствор гидроксида натрия, 2 моль/дм3
Растворяют 40 г гидроксида натрия в 500 см3 дистиллированной воды. Хранят в плотно закрытой полиэтиленовой посуде.
10.1.4 Раствор гидроксида натрия, 0,2 моль/дм3
Растворяют 4 г гидроксида натрия в 500 см3 дистиллированной воды. Хранят в плотно закрытой полиэтиленовой посуде.
10.1.5 Раствор гидроксида натрия, 0,04 моль/дм3
К 500 см3 дистиллированной воды приливают 10 см3 раствора гидроксида натрия, 2 моль/дм3 и перемешивают. Раствор устойчив при хранении в плотно закрытой полиэтиленовой посуде.
10.1.6 Раствор гидрокарбоната натрия, 1 моль/дм3
Растворяют 42 г гидрокарбоната натрия в 500 см3 дистиллированной воды. Раствор устойчив при хранении в плотно закрытой полиэтиленовой посуде.
10.1.7 Раствор никотинамида, 12 %-ный
Растворяют 6 г никотинамида в 44 см3 дистиллированной воды. Раствор хранят в холодильнике не более 10 дней.
10.1.8 Раствор хлорамина Т, 1 %-ный
Растворяют 1 г хлорамина Т в 99 см3 дистиллированной воды. Раствор хранят в темной плотно закрытой склянке в холодильнике не более 3 дней. Для приготовления раствора не допускается использовать препарат хлорамина Т с истекшим сроком хранения.
10.1.9 Раствор сульфата меди, 200 г/дм3
Помещают в мензурку вместимостью 250 см3 50 г сульфата меди, добавляют дистиллированной воды до объема 250 см3 и перемешивают до растворения. Раствор устойчив.
10.1.10 Раствор хлорида олова, 35 %-ный
Помещают в стакан вместимостью 100 см3 25 г хлорида олова, добавляют 5 см3 концентрированной соляной кислоты, 36 см3 дистиллированной воды и перемешивают. При хранении в плотно закрытой склянке в холодильнике раствор устойчив в течение 2 недель.
10.1.11 Гипохлорит натрия, концентрированный раствор
Получение концентрированного раствора гипохлорита натрия приведено в приложении А.
10.1.12 Раствор гипохлорита натрия, 0,015 % активного хлора
1,0 см3 концентрированного раствора гипохлорита смешивают с раствором гидроксида натрия, 0,04 моль/дм3, объем которого равен 10 ∙ (Сах - 0,015) см3, где Сах - массовая доля активного хлора в концентрированном растворе гипохлорита. При хранении в темной плотно закрытой склянке в холодильнике раствор устойчив не более суток.
10.1.13 Суспензия оксида кальция
В стакан помещают 100 см3 дистиллированной воды, добавляют 1,0 г оксида кальция и перемешивают. Полученную суспензию переносят в склянку для промывания газов СПЖ вместимостью 250 см3.
10.1.14 Раствор дихромата калия, 2 %-ный
В 50 см3 дистиллированной воды растворяют 1,0 г дихромата калия. Хранят раствор в склянке темного стекла с притертой пробкой не более 6 мес.
10.2 Приготовление градуировочных растворов
10.2.1 Градуировочные растворы готовят из ГСО с массовой концентрацией тиоцианат-иона 1,00 мг/см3, что соответствует 0,448 мг/см3 цианид-иона. Вскрывают ампулу ГСО и ее содержимое переносят в сухую чистую градуированную пробирку. Для приготовления градуировочного раствора с массовой концентрацией цианид-ионов 0,0202 мг/см3 (20,2 мкг/см3) отбирают 4,50 см3 образца с помощью чистой сухой градуированной пипетки вместимостью 5 см3 и переносят его в мерную колбу вместимостью 100 см3. Доводят объем в колбе до метки дистиллированной водой и перемешивают. Раствор хранят в плотно закрытой склянке темного стекла при комнатной температуре не более недели, в холодильнике - в течение 2 недель.
10.2.2 Для приготовления градуировочного раствора с массовой концентрацией цианид - ионов 2,0 мкг/см3 с помощью чистой сухой пипетки с одной отметкой вместимостью 10 см3 отбирают 10,0 см3 градуировочного раствора с массовой концентрацией цианид-ионов 0,0200 мг/см3, помещают его в мерную колбу вместимостью 100 см3, доводят до метки раствором гидроксида натрия 0,04 моль/дм3 и перемешивают. Раствор используют в течение рабочего дня.
10.2.3 Если массовая концентрация тиоцианат - ионов в ГСО не равна точно 1,00 мг/см3, рассчитывают массовую концентрацию цианид - ионов в полученных градуировочных растворах в соответствии с концентрацией конкретного образца.
10.2.4 При отсутствии ГСО допускается использовать аттестованный раствор тиоцианат - ионов, приготовленный из тиоционата калия. Методика приготовления аттестованного раствора приведена в приложении Б.
10.3 Установление градуировочной зависимости
Для приготовления градуировочных образцов в мерные колбы вместимостью 25 см3 приливают по 20 см3 раствора гидроксида натрия, 0,04 моль/дм3, с помощью градуированных пипеток 1 и 5 см3 приливают 0,25; 0,5; 1,0; 1,5; 2,0; 2,5; 3,0; 3,5; 4,5 см3 градуировочного раствора тиоцианата калия с массовой концентрацией цианид-ионов 2,0 мкг/см3, доводят объемы растворов в колбах до метки раствором гидроксида натрия, 0,04 моль/дм3. Содержание цианид-ионов в полученных образцах составляет 0,5; 1,0; 2,0; 3,0; 4,0; 5,0; 6,0; 7,0; 9,0 мкг.
С помощью пипетки с одной отметкой вместимостью 10 см3 отбирают по 10,0 см3 каждого из полученных растворов, помещают их в сухие конические колбы вместимостью 25 см3 и проводят определение цианидов согласно 11.1.3 - 11.1.4. Одновременно выполняют холостой опыт, используя 10 см3 раствора гидроксида натрия, 0,04 моль/дм3.
Оптическую плотность градуировочных образцов с содержанием цианид-ионов от 0,5 мкг до 4,0 мкг измеряют в кювете с толщиной поглощающего слоя 3 см, образцы с концентрацией от 3,0 мкг до 9,0 мкг - в кювете с толщиной поглощающего слоя 1 см относительно дистиллированной воды. Оптическую плотность холостого опыта измеряют в обеих кюветах. Значения оптической плотности холостого опыта вычитают из оптической плотности градуировочных образцов.
Градуировочную зависимость оптической плотности образцов от массовой концентрации цианид-ионов для каждого из диапазонов измерений рассчитывают методом наименьших квадратов.
Градуировочную зависимость устанавливают при замене измерительного прибора, использовании новой партии хлорамина Т или никотинамида, но не реже 1 раза в год.
10.4 Контроль стабильности градуировочной характеристики
10.4.1 Контроль стабильности градуировочной характеристики проводят при приготовлении нового буферного раствора, раствора хлорирующего агента или никотинамида. Средствами контроля являются образцы, используемые для установления градуировочной зависимости по 10.3 (не менее трёх для каждой градуировочной зависимости). Градуировочная характеристика считается стабильной при выполнении условий:
|X - C| ≤ d, (2)
где X - результат контрольного измерения содержания цианид-ионов в градуировочном образце, мкг;
С - приписанное градуировочному образцу значение содержания цианид-ионов, мкг;
d - допустимое расхождение между измеренным и приписанным значениями содержания цианид-ионов в образце, мкг (см. таблицу 2).
Допускается проводить контроль стабильности градуировочной характеристики для одной зависимости, если другая зависимость не будет использована для расчета концентрации цианидов в анализируемых пробах воды.
Если условие стабильности не выполняется для одного градуировочного образца, необходимо выполнить повторное измерение этого образца для исключения результата, содержащего грубую погрешность. При повторном невыполнении условия, выясняют причины нестабильности, устраняют их и повторяют измерение с использованием других образцов, предусмотренных методикой. Если градуировочная характеристика вновь не будет удовлетворять условию (2), устанавливают новую градуировочную зависимость.
Таблица 2 - Допустимые расхождения между измеренными и приписанными значениями содержания цианидов в образцах при контроле стабильности градуировочной зависимости
|
Допустимое расхождение d, мкг |
|
|
0,5 |
0,09 |
|
1,0 |
0,10 |
|
2,0 |
0,12 |
|
3,0 |
0,14 |
|
4,0 |
0,16 |
|
5,0 |
0,18 |
|
6,0 |
0,20 |
|
7,0 |
0,22 |
|
9,0 |
0,26 |
10.4.2 При выполнении условия (2) учитывают знак разности между измеренными и приписанными значениями массовой концентрации цианидов в образцах. Эта разность должна иметь как положительное, так и отрицательное значение, если же все значения имеют один знак, это говорит о наличии систематического отклонения. В таком случае требуется установить новую градуировочную зависимость.
11 Выполнение измерений
11.1 Выполнение измерений массовой концентрации токсичных цианидов
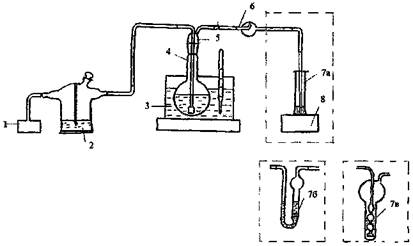
11.1.1 Собирают установку для отдувки цианидов, схема которой представлена на рисунке 1.
В качестве поглотительного сосуда могут быть использованы мерный цилиндр вместимостью 10 см3, в который почти до дна цилиндра опущена стеклянная трубка диаметром 5 - 6 мм с сильно оттянутым концом (пипетка Пастера), либо поглотитель с пористой пластиной, либо поглотитель Рихтера.
При использовании цилиндра для подачи воздуха может использоваться только микрокомпрессор аквариумный. Если в качестве поглотительного сосуда используются поглотитель с пористой пластиной или поглотитель Рихтера, может использоваться как микрокомпрессор, так и вакуум-насос, который подсоединяется к выходному отростку поглотителя. Элементы установки соединяются стеклянными или тефлоновыми трубками, которые пристыковываются друг к другу и к элементам установки отрезками трубок из силиконовой резины подходящего диаметра.
1 - микрокомпрессор; 2 - склянка для промывания газов СПЖ; 3 - водяная баня с терморегулятором; 4 - круглодонная колба; 5 - насадка к склянке для промывания газов СН; 6 - каплеуловитель; 7 - поглотительный сосуд (7а - цилиндр мерный с пипеткой Пастера, 7б - поглотитель с пористой пластиной, 7в - поглотитель Рихтера); 8 - подставка
Рисунок 1 - Схема установки для отдувки цианидов
Для очистки воздуха используется склянка СПЖ, в которую помещают насыщенный раствор оксида кальция. Если насадка, через которую подается воздух в колбу для отдувки, не имеет на конце шарика с отверстиями, к ней следует присоединить керамический распылитель для аквариумного микрокомпрессора, промытый раствором соляной кислоты и дистиллированной водой.
Скорость продувки устанавливают от 180 до 200 см3/мин. Измерение скорости воздушного потока проводится ротаметром на выходе из каплеуловителя, если используется микрокомпрессор, или на входе склянки СПЖ, если используется вакуум-насос.
11.1.2 Мерным цилиндром вместимостью 100 см3 отбирают 100 см3 анализируемой воды, помещают ее в круглодонную колбу для отдувки вместимостью 250 см3. Если проба была законсервирована, то перед отбором аликвоты нужно тщательно, не менее 3 мин, перемешивать пробу и отобрать дополнительно еще 5 см3 пробы для учета разбавления её за счет добавления консервантов. Законсервированную пробу нейтрализуют соляной кислотой (1:1) до рН 5 - 6 по универсальной индикаторной бумаге. Добавляют 10 см3 ацетатного буферного раствора, соединяют элементы установки, опускают круглодонную колбу в водяную баню, нагретую до температуры от 92 °С до 95 °С, включают микрокомпрессор или вакуум-насос и проводят отдувку в течение 40 мин, поглощая выделяющуюся HCN в поглотительном сосуде, куда предварительно приливают 4,0 см3 раствора гидроксида натрия, 0,20 моль/дм3.
Одновременно с серией анализируемых проб выполняют обработку холостой пробы (без отгонки), используя 10 см3 раствора гидроксида натрия 0,04 моль/дм3.
11.2 Выполните измерений массовой концентрации общих цианидов
11.2.1 Мерным цилиндром вместимостью 100 см3 отбирают 100 см анализируемой воды и помещают ее в круглодонную колбу для отдувки вместимостью 250 см3. Если проба была законсервирована, то перед отбором аликвоты нужно тщательно, не менее 3 мин, перемешивать пробу и отобрать дополнительно еще 5 см3 пробы для учета разбавления её за счет добавления консервантов. Добавляют 10 см3 раствора сульфата меди 200 г/дм3, 2 см3 35 %-ного раствора хлорида олова и 10 см3 концентрированной соляной кислоты, соединяют элементы установки, опускают круглодонную колбу в водяную баню, нагретую до температуры от 92 °С до 95 °С, включают микрокомпрессор или вакуум-насос и проводят отдувку в течение 60 мин, поглощая выделяющуюся HCN в поглотительном сосуде, куда предварительно приливают 4,0 см3 раствора гидроксида натрия, 0,20 моль/дм3.
Далее проводят измерение концентрации цианидов в соответствии с 11.1.3 - 11.1.5.
11.3 Мешающие влияния и их устранение
Мешающее влияние сульфидов устраняют добавлением солей кадмия и цинка при определении легкоразлагаемых цианидов, и добавлением соли меди при определении общих цианидов.
В случае присутствия в пробе трудно разлагаемого цианида меди (I), при определении общих цианидов в сточных водах к пробе добавляют для окисления 1 см3 2 %-ного раствора дихромата калия.
Формальдегид мешает определению цианидов, за счет образования циангидринов, которые при нагревании переходят в нитрилы, не отгоняющиеся из воды и не реагирующие с никотинамидом. Мешающее влияние формальдегида проявляется при концентрации превышающей концентрацию цианидов более чем в 500 раз.
При определении легкоразлагаемых соединений цианидов добавление солей цинка и кадмия предотвращает частичное разложение гексацианоферрат-ионов.
12 Вычисление результатов измерений
12.1 Массовую концентрацию цианид-ионов X, мг/дм3, в анализируемой пробе воды рассчитывают по формуле
![]() (3)
(3)
где С - содержание цианид-ионов, найденное по градуировочной зависимости, мкг;
V - объём аликвоты пробы воды, взятый для анализа, см3;
b - поправочный коэффициент учитывающий потери цианидов в процессе отдувки.
Коэффициент b находят для конкретной установки в соответствии с приложением В. Ориентировочное значение коэффициента b при определении цианидов составляет 1,2.
12.2 Результат измерения в документах, предусматривающих его использование, представляют в виде:
Х ± Δ, мг/дм3 (Р = 0,95), (4)
где ±Δ - границы характеристики погрешности результата измерения для данной массовой концентрации цианидов, мг/дм3 (см. таблицу 1).
Численные значения результата измерения должны оканчиваться цифрой того же разряда, что и значения характеристики погрешности; последние не должны содержать более двух значащих цифр.
12.3 Допустимо представлять результат в виде:
Х ± Δл (Р = 0,95) при условии Δл < Δ, (5)
где ±Δл - границы характеристики погрешности результатов измерений, установленные при реализации методики в лаборатории и обеспечиваемые контролем стабильности результатов измерений, мг/дм3.
Примечание - Допустимо характеристику погрешности результатов измерений при внедрении методики в лаборатории устанавливать на основе выражения Δл = 0,84 ∙ Δ с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов измерений.
12.4 Результаты измерений оформляют протоколом или записью в журнале, по формам, приведенным в Руководстве по качеству лаборатории.
13 Контроль качества результатов измерений при реализации методики в лаборатории
13.1 Общие положения
13.1.1 Контроль качества результатов измерений при реализации методики в лаборатории предусматривает:
- оперативный контроль исполнителем процедуры выполнения измерений (на основе оценки повторяемости, погрешности при реализации отдельно взятой контрольной процедуры);
- контроль стабильности результатов измерений (на основе контроля стабильности повторяемости, внутрилабораторной прецизионности погрешности).
13.1.2 Периодичность оперативного контроля исполнителем процедуры выполнения измерений, а также реализуемые процедуры контроля стабильности результатов выполняемых измерений регламентируются в Руководстве по качеству лаборатории.
13.2 Алгоритм оперативного контроля повторяемости
13.2.1 Контроль повторяемости осуществляют для одной пробы из серии 10 - 12 рабочих проб. Для этого отобранную пробу воды делят на две части, и выполняют измерения в соответствии с разделом 11 одновременно в обеих аликвотах.
13.2.2 Результат контрольной процедуры rк, мг/дм3, рассчитывают по формуле
rк = |Х1 - Х2|, (6)
где Х1, Х2 - результаты параллельных измерений массовой концентрации цианид-ионов X в пробе, мг/дм3
13.2.3 Предел повторяемости rп, мг/дм3, рассчитывают по формуле
rп = 2,77 ∙ σr, (7)
где σr - показатель повторяемости, мг/дм3 (см. таблицу 1).
13.2.4 Результат контрольной процедуры должен удовлетворять условию
rк ≤ rп. (8)
13.2.5 При несоблюдении условия (8) выполняют еще два измерения и сравнивают разницу между максимальным и минимальным результатами с нормативом контроля равным 3,6 ∙ σr. В случае повторного превышения предела повторяемости, поступают в соответствии с разделом 5 ГОСТ Р ИСО 5725-6.
13.3 Алгоритм оперативного контроля процедуры выполнения измерений с использованием метода добавок
13.3.1 Оперативный контроль исполнителем процедуры выполнения измерений проводят путем сравнения результатов отдельно взятой контрольной процедуры Кк с нормативом контроля К.
Для цианидов проводится оперативный контроль процедуры выполнения измерений массовой концентрации общих цианидов; в качестве добавки при этом используется раствор гексацианоферрата калия (см. приложение Г).
13.3.2 Результат контрольной процедуры Кк, мг/дм3, рассчитывают по формуле
Кк = |Х' - Х - С|, (9)
где Х' - результат контрольного измерения массовой концентрации цианидов в пробе с известной добавкой, мг/дм3;
Х - результат измерения массовой концентрации цианидов в рабочей пробе, мг/дм3;
С - величина добавки, мг/дм3.
13.3.3 Норматив контроля К, мг/дм3, рассчитывают по формуле
![]() (10)
(10)
где Δлх' - значения характеристики погрешности результатов измерений установленные в лаборатории при реализации методики, соответствующие массовой концентрации цианидов в пробе с добавкой, мг/дм3;
Δлх - значения характеристики погрешности результатов измерений, установленные в лаборатории при реализации методики, соответствующие массовой концентрации цианидов в рабочей пробе, мг/дм3.
Примечание - Допустимо для расчета норматива контроля использовать значения характеристик погрешности, полученные расчетным путем по формулам Δлх' = 0,84 ∙ Δх' и Δлх = 0,84 ∙ Δх.
13.3.4 Если результат контрольной процедуры удовлетворяет условию
|Кк| ≤ К, (11)
процедуру признают удовлетворительной.
При невыполнении условия (11) контрольную процедуру повторяют. При повторном невыполнении условия (11), выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
14 Проверка приемлемости результатов, полученных в условиях воспроизводимости
14.1 Расхождение между результатами измерений, полученными в двух лабораториях, не должно превышать предела воспроизводимости. При выполнении этого условия приемлемы оба результата измерений и в качестве окончательного может быть использовано их общее среднее значение. Значение предела воспроизводимости R, мг/дм3, рассчитывают по формуле
R = 2,77σR (12)
где σR - показатель воспроизводимости методики, мг/дм3 (см. таблицу 1).
14.2 При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов измерений согласно разделу 5 ГОСТ Р ИСО 5725-6 или МИ 2881.
14.3 Проверка приемлемости проводится при необходимости сравнения результатов измерений, полученных двумя лабораториями.
Приложение
А
(обязательное)
Получение концентрированного раствора гипохлорита натрия
А.1 Приготовление растворов и реактивов
А.1.1 Раствор тиосульфата натрия с молярной концентрацией количества вещества эквивалента (КВЭ) 0,1 моль/дм3
Растворяют 25 г Na2S2O3 ∙ 5Н2O в 1 дм3 дистиллированной воды, которую предварительно кипятят в течение 1 - 1,5 ч и охлаждают до комнатной температуры. Раствор используют не ранее, чем через 5 дней после приготовления. Хранят раствор в склянке из темного стекла. Точную концентрацию раствора тиосульфата натрия устанавливают в соответствии с А.2 не реже одного раза в месяц.
А.1.2 Раствор дихромата калия с молярной концентрацией 0,1000 моль/дм3 КВЭ
Для приготовления раствора из навески 4,904 г дихромата калия (K2Cr2О7), предварительно высушенного в сушильном шкафу при температуре 105 °С в течение от 1 до 2 ч, переносят количественно в мерную колбу вместимостью 1000 см3, растворяют в дистиллированной воде, доводят объем раствора до метки и перемешивают.
Хранят раствор дихромата калия в склянке с притертой пробкой в темном месте не более 6 мес.
А.1.3 Раствор иодида калия, 10 %-ный
Растворяют 10 г иодида калия в 90 см3 дистиллированной воды. Раствор хранят в темной склянке до появления желтоватой окраски.
А.1.4 Раствор уксусной кислоты, 2 моль/дм3
Растворяют 60 см3 уксусной кислоты в 440 см3 дистиллированной воды. Раствор устойчив.
А.1.5 Раствор соляной кислоты, (2:1)
Смешивают 2 части (по объему) концентрированной соляной кислоты с 1 частью дистиллированной воды. Раствор устойчив.
А.1.6 Раствор крахмала, 0,5 %-ный
0,25 г растворимого (рисового, пшеничного) крахмала перемешивают с 50 см3 дистиллированной воды и нагревают до кипения. Раствор хранят до помутнения.
А.2 Установление точной концентрации раствора тиосульфата натрия
В коническую колбу вместимостью 250 см3 приливают 70 - 80 см3 дистиллированной воды, добавляют с помощью пипетки с одной отметкой 10 см3 раствора дихромата калия, приливают мерным цилиндром 10 см3 раствора иодида калия и 10 см3 раствора соляной кислоты (2:1). Закрывают колбу пробкой и выдерживают в течение 5 мин в темном месте. Затем титруют пробу раствором тиосульфата натрия до слабо-желтой окраски, добавляют 1 см3 раствора крахмала и вновь титруют до исчезновения окраски. Одновременно выполняют титрование холостой пробы.
Определение повторяют и при отсутствии расхождения в объемах титранта более 0,1 см3, за результат принимают среднее арифметическое. Рассчитывают молярную концентрацию тиосульфата натрия в растворе по формуле
![]() (А.1)
(А.1)
где СТ - молярная концентрация раствора тиосульфата натрия, моль/дм3, КВЭ;
VT - объем раствора тиосульфата, пошедший на титрование раствора дихромата калия, см3.
А.3 Получение концентрированного раствора гипохлорита натрия
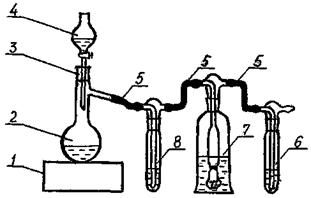
Для получения раствора гипохлорита натрия собирают установку, изображенную на рисунке А.1.
1 - электроплитка; 2 - колба круглодонная с отводом; 3 - резиновая пробка; 4 - капельная воронка; 5 - соединительные резиновые трубки; 6 - склянка с разбавленным раствором гидроксида натрия; 7 - склянка-приемник; 8 - склянка с безаммиачной водой
Рисунок А.1 - Схема установки для получения гипохлорита натрия
Получение гипохлорита необходимо проводить в вытяжном шкафу. В круглодонную колбу с отводом помещают 25 г перманганата калия и закрывают ее резиновой пробкой, в которую вставлена капельная воронка с 50 см3 концентрированной соляной кислоты. Колба с отводом с помощью резиновых (не силиконовых!) трубок соединяется с промывными склянками. Первая склянка заполняется 25 см3 безаммиачной воды; во вторую (склянку-приемник) помещают 100 см3 безаммиачной воды, содержащей около 4 г гидроксида натрия; в третью склянку добавляют немного разбавленного раствора гидроксида натрия в безаммиачной воде для улавливания хлора, не поглощенного в склянке-приемнике. Соединения должны быть выполнены так, чтобы длина резиновых трубок была минимальна.
При добавлении соляной кислоты к перманганату калия выделяется газообразный хлор, который, в основном, поглощается в склянке-приемнике. Чтобы избежать значительных потерь хлора следует обеспечить герметичность соединений элементов установки. При достаточно полном протекании реакции и поглощении хлора в склянке-приемнике можно получить раствор с концентрацией активного хлора от 2 % до 4 % и более. Пропускание хлора ведут до практически полного прекращения его выделения (2 - 3 ч). Ускорить реакцию можно слабым нагреванием, но не следует допускать слишком бурного выделения хлора, поскольку он при этом не будет достаточно эффективно поглощаться в склянке-приемнике. При эффективном поглощении раствор в склянке-приемнике постепенно становится зеленовато-желтым.
По окончании реакции отсоединяют склянку-приемник, добавляют в нее понемногу сухой гидроксид натрия до исчезновения явной желтой окраски, затем добавляют еще 2 г гидроксида натрия и перемешивают. Приготовленный раствор гипохлорита хранят в темной склянке, упакованной в полиэтиленовый пакет, в холодильнике в течение года или более, периодически проверяя концентрацию активного хлора (2 раза в месяц). Аналогично можно поступить с раствором гипохлорита, получающимся в склянке (6), если массовая доля активного хлора в нем более 0,5 %, однако этот раствор будет менее устойчивым.
Примечание - Если соединения стеклянных и резиновых трубок, а также резиновой пробки с колбой, окажутся недостаточно герметичными, можно стыки замазать обычным детским пластилином.
А.4 Определение массовой доли активного хлора в концентрированном растворе гипохлорита
В коническую колбу вместимостью 250 см3 добавляют 80 - 90 см3 дистиллированной воды, приливают пипеткой 2 см3 раствора гипохлорита, 5 см3 раствора иодида калия и 10 см3 раствора уксусной кислоты. Выделившийся йод титруют раствором тиосульфата натрия до бледно-желтой окраски, затем добавляют 1 см3 раствора крахмала и продолжают титрование до обесцвечивания раствора. Одновременно выполняют титрование холостой пробы.
Определение повторяют и при отсутствии расхождения в объемах титранта более 0,1 см3 за результат принимают среднее арифметическое. В противном случае повторяют титрование до получения результатов, расхождение между которыми не превышает 0,1 см3. Массовую долю активного хлора Сах в растворе, %, вычисляют по формуле
Cах = 1,77 ∙ CТ ∙ VT, (A.2)
где 1,77 - коэффициент, учитывающий все постоянные величины, применяемые для расчета.
Приложение
Б
(рекомендуемое)
Методика приготовления аттестованных растворов тиоцианата калия AP1-CN и AP2-CN для установления градуировочных характеристик приборов при выполнении измерений массовой концентрации цианидов фотометрическим методом
Б.1 Назначение и область применения
Настоящая методика регламентирует процедуру приготовления аттестованных растворов тиоцианата калия, предназначенных для установления градуировочных характеристик приборов при выполнении измерений массовой концентрации цианидов в природных и очищенных сточных водах фотометрическим методом.
Б.2 Метрологические характеристики
Метрологические характеристики аттестованных растворов приведены в таблице Б.1.
Таблица Б.1 - Метрологические характеристики аттестованных растворов API-CN и AP2-CN
|
Значение характеристики для аттестованных растворов |
||
|
AP1-CN |
AP2-CN |
|
|
Аттестованное значение массовой концентрации цианид-ионов, мг/см3 |
4,480 |
0,448 |
|
Границы погрешности аттестованного значения массовой концентрации цианид-ионов, мг/см3, (Р = 0,95) |
± 0,046 |
± 0,005 |
Б.3 Средства измерений, вспомогательные устройства, реактивы
Б.3.1 Весы лабораторные высокого (II) класса точности по ГОСТ Р 53228-2008.
Б.3.2 Колбы мерные 2 класса точности исполнения 2, 2а по ГОСТ 1770-74 вместимостью 100 см3 - 2 шт.
Б.3.3 Пипетка с одной отметкой 2 класса точности по ГОСТ 29227-91 вместимостью 10 см3 - 1 шт.
Б.3.4 Воронка лабораторная по ГОСТ 25336-82 диаметром 36 мм - 1 шт.
Б.3.5 Палочка стеклянная.
Б.3.6 Стаканчик для взвешивания (бюкс) СВ-19/9 по ГОСТ 25336-82.
Б.3.7 Полиэтиленовая (полипропиленовая) посуда для хранения аттестованных растворов.
Б.4 Исходные компоненты аттестованного раствора
Б.4.1 Калий роданистый (тиоцианат калия) по ГОСТ 4139-75, ч.д.а.
Б.4.2 Вода дистиллированная по ГОСТ 6709-72.
Б.5 Процедура приготовления аттестованных растворов
Б.5.1 Для приготовления аттестованного раствора AP1-CN взвешивают в бюксе с точностью до четвертого знака после запятой 1,6732 - 1,6734 г тиоцианата калия, предварительно высушенного в сушильном шкафу при температуре 105 °С в течение часа. Количественно переносят навеску в мерную колбу вместимостью 100 см3, растворяют в дистиллированной воде, доводят объём раствора до метки и перемешивают.
Полученному раствору приписывают массовую концентрацию тиоцианат-ионов 10,0 мг/см3, что соответствует 4,48 мг/см3 цианид-ионов.
Б.5.2 Для приготовления аттестованного раствора AP2-CN пипеткой с одной отметкой отбирают 10,0 см3 раствора AP1-CN, помещают его в мерную колбу вместимостью 100 см3, доводят до метки дистиллированной водой и перемешивают.
Полученному раствору приписывают массовую концентрацию цианид-ионов 0,448 мг/см3.
Б.6 Расчет метрологических характеристик аттестованных растворов
Б.6.1 Аттестованное значение массовой концентрации цианид-ионов С, мг/см3, в растворе AP1-CN рассчитывают по формуле
![]() (Б.1)
(Б.1)
где m - масса навески тиоцианата калия, г;
V - вместимость мерной колбы, см3;
26,02 - молярная масса цианид-ионов, г/моль;
97,18 - молярная масса тиоцианата калия, г/моль.
Б.6.2 Расчет погрешности приготовления аттестованного раствора AP1-CN Δ, мг/см3, выполняют по формуле
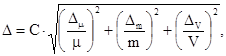 (Б.2)
(Б.2)
где С - приписанное раствору значение массовой концентрации цианид-ионов, мг/см3;
μ - массовая доля основного вещества (KSCN), приписанная реактиву квалификации «ч.д.а», %;
Δµ - предельное значение возможного отклонения массовой доли основного вещества в реактиве от приписанного значения µ, %;
Δm - предельная возможная погрешность взвешивания, г;
ΔV - предельное значение возможного отклонения вместимости мерной колбы от номинального значения, см3.
Предел возможных значений погрешности приготовления аттестованного раствора AP1-CN равен
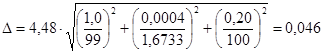 мг/см3.
мг/см3.
Б.6.3 Аттестованное значение массовой концентрации цианид-иона в растворе AP2-CN С1, мг/дм3, рассчитывают по формуле
![]() (Б.3)
(Б.3)
Б.6.4 Расчет предела возможных значений погрешности приготовления аттестованных растворов AP2-CN Δ1, мг/см3, выполняют по формуле
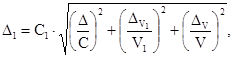 (Б.4)
(Б.4)
где V1 - номинальный объем раствора, отбираемый пипеткой, см3;
![]() - предельное значение возможного
отклонения объема раствора, отбираемого пипеткой, от номинального значения, см3.
- предельное значение возможного
отклонения объема раствора, отбираемого пипеткой, от номинального значения, см3.
Предел возможных значений погрешности приготовления аттестованного раствора AP2-CN равен
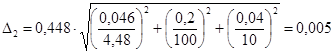 мг/см3.
мг/см3.
Б.7 Требования безопасности
Необходимо соблюдать общие требования техники безопасности при работе в химических лабораториях.
Б.8 Требования к квалификации операторов
Аттестованный раствор может готовить инженер или лаборант со средним профессиональным образованием, прошедший специальную подготовку и имеющий стаж работы в химической лаборатории не менее года.
Б.9 Требования к маркировке
На склянку с аттестованным раствором должна быть наклеена этикетка с указанием условного обозначения раствора, массовой концентрации цианидов, погрешности ее установления и даты приготовления.
Б.10 Условия хранения
Аттестованный раствор AP1-CN хранят в плотно закрытой посуде темного стекла при комнатной температуре не более месяца, в холодильнике - в течение 3 мес.
Аттестованный раствор AP2-CN хранят в плотно закрытой посуде темного стекла при комнатной температуре не более недели, в холодильнике - в течение 2 недель.
Приложение
В
(обязательное)
Определение поправочного коэффициента для учета потерь цианидов при отдувке из воды
Поправочный коэффициент b может изменяться в зависимости от конфигурации конкретной установки для отдувки. Для определения поправочного коэффициента в круглодонную колбу помещают 100 см3 дистиллированной воды, добавляют 1,0 см3 аттестованного раствора гексацианоферрата калия с массовой концентрацией цианид-ионов 5,0 мкг/см3, добавляют 10 см3 раствора сульфата меди 200 г/дм3, 2 см3 50 %-ного раствора хлорида олова и 10 см3 концентрированной соляной кислоты. Соединяют элементы установки, опускают круглодонную колбу в водяную баню, нагретую до 92 - 95 °С, включают микрокомпрессор или вакуум-насос и проводят отдувку в течение 60 минут, поглощая выделяющуюся HCN в поглотительном сосуде, куда предварительно приливают 4,0 см3 раствора гидроксида натрия, 0,2 моль/дм3.
Полученный концентрат из цилиндра количественно переносят в мерную колбу вместимостью 25 см3, обмывая стенки цилиндра дистиллированной водой, и доводят до метки этим же раствором. Затем отбирают пипеткой с одной отметкой 10,0 см3 полученного раствора, переносят в коническую колбу вместимостью 25 см3 и проводят анализ концентратов согласно 11.1.3 - 11.1.4.
Расчет поправочного коэффициента выполняют по формуле
![]() (Г.1)
(Г.1)
где q - количество цианидов, добавленное в пробу, мкг;
q0 - количество цианидов в 25 см3 концентрата, найденное по градуировочной зависимости, мкг.
Процедуру повторяют 5 раз и за окончательную величину b принимают среднее арифметическое из полученных значений.
Приложение
Г
(обязательное)
Методика приготовления аттестованных растворов гексацианоферрата калия AP3-CN и AP4-CN для контроля точности измерений массовой концентрации цианидов фотометрическим методом
Г.1 Назначение и область применения
Настоящая методика регламентирует процедуру приготовления аттестованного раствора гексацианоферрата калия, предназначенного для контроля точности выполнения измерений массовой концентрации цианидов в природных и очищенных сточных водах фотометрическим методом.
Г.2 Метрологические характеристики
Метрологические характеристики аттестованных растворов приведены в таблице В.1.
Таблица В.1 - Метрологические характеристики аттестованных растворов AP3-CN и AP4-CN
|
Значение характеристики для аттестованных растворов |
||
|
AP3-CN |
AP4-CN |
|
|
Аттестованное значение массовой концентрации цианид-ионов |
1,000 мг/см3 |
5,00 мкг/см3 |
|
Границы погрешности аттестованного значения массовой концентрации цианид-ионов, (Р = 0,95) |
0,010 мг/см3 |
0,072 мкг/см3 |
Г.3 Средства измерений, вспомогательные устройства, реактивы
Г.3.1 Весы лабораторные высокого (II) класса точности по ГОСТ Р 53228-2008.
Г.3.2 Колбы мерные 2 класса точности исполнения 2, 2а по ГОСТ 1770-74 вместимостью: 100 см3 - 1 шт., 200 см3 - 1 шт.
Г.3.3 Пипетка градуированная 2-го класса точности исполнения 1 по ГОСТ 29227-91 вместимостью 1 см3 - 1 шт.
Г.3.4 Воронка лабораторная по ГОСТ 25336-82 диаметром 36 мм - 1 шт.
Г.3.5 Стаканчик для взвешивания (бюкс) СВ-19/9 по ГОСТ 25336-82.
Г.3.6 Шпатель по ГОСТ 9147-80.
Г.4 Исходные компоненты аттестованного раствора
Г.4.1 Калий железосинеродистый (гексацианоферрат (III) калия) по ГОСТ 4206-75, ч.д.а.
Г.4.2 Вода дистиллированная по ГОСТ 6709-72.
Г.5 Процедура приготовления аттестованных растворов
Г.5.1 Для приготовления аттестованного раствора AP3-CN взвешивают в бюксе с точностью до четвертого знака после запятой 0,212 г гексацианоферрата калия. Количественно переносят навеску в мерную колбу вместимостью 100 см3, растворяют в дистиллированной воде, доводят объём раствора до метки и перемешивают.
Полученному раствору приписывают массовую концентрацию цианид-ионов 1,00 мг/см3.
Г.5.2 Для приготовления аттестованного раствора AP4-CN пипеткой вместимостью 1 см3 отбирают 1,00 см3 раствора AP3-CN, помещают его в мерную колбу вместимостью 200 см3, доводят до метки дистиллированной водой и перемешивают.
Полученному раствору приписывают массовую концентрацию цианид-ионов 5,00 мкг/см3.
Г.6 Расчет метрологических характеристик аттестованных растворов
Г.6.1 Аттестованное значение массовой концентрации цианид-ионов С, мг/см3, в растворе AP3-CN рассчитывают по формуле
![]() (В.1)
(В.1)
где m - масса навески гексацианоферрата калия, г;
V - вместимость мерной колбы, см3;
26,02 - молярная масса цианид-ионов, г/моль; (6 - количество групп - CN в молекуле гексацианоферрата калия);
329,25 - молярная масса гексацианоферрата калия, г/моль.
Г.6.2 Расчет погрешности приготовления аттестованного раствора AP3-CN Δ, мг/см3, выполняют по формуле
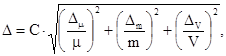 (B.2)
(B.2)
где µ - массовая доля основного вещества (K3[Fe(CN)6]), приписанная реактиву квалификации «ч.д.а», %;
Δµ - предельное значение возможного отклонения массовой доли основного вещества в реактиве от приписанного значения µ, %;
Δm - предельная возможная погрешность взвешивания, г;
ΔV - предельное значение возможного отклонения вместимости мерной колбы от номинального значения, см3.
Предел возможных значений погрешности приготовления аттестованного раствора AP3-CN равен
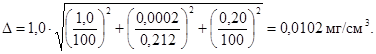
Г.6.3 Аттестованное значение массовой концентрации цианид-иона в растворе AP4-CN С1, мкг/см3, рассчитывают по формуле
![]() (B.3)
(B.3)
Г.6.4 Расчет предела возможных значений погрешности приготовления аттестованных растворов AP4-CN Δ1, мкг/см3 выполняют по формуле
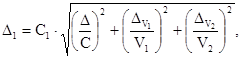 (В.4)
(В.4)
где C1 - приписанное раствору AP4-CN значение массовой концентрации цианид-иона, мкг/см3;
V1 - номинальный объем раствора, отбираемый пипеткой, см3;
![]() - предельное значение возможного
отклонения объема раствора, отбираемого пипеткой, от номинального значения, см3;
- предельное значение возможного
отклонения объема раствора, отбираемого пипеткой, от номинального значения, см3;
V2 - вместимость мерной колбы, см3;
![]() - предельное значение возможного
отклонения вместимости мерной колбы от номинального значения, см3.
- предельное значение возможного
отклонения вместимости мерной колбы от номинального значения, см3.
Предел возможных значений погрешности приготовления аттестованного раствора AP4-CN равен
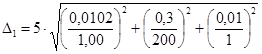 = 0,072 мкг/см3.
= 0,072 мкг/см3.
Г.7 Требования безопасности
Необходимо соблюдать общие требования техники безопасности при работе в химических лабораториях.
Г.8 Требования к квалификации операторов
Аттестованный раствор может готовить инженер или лаборант со средним профессиональным образованием, прошедший специальную подготовку и имеющий стаж работы в химической лаборатории не менее года.
Г.9 Требования к маркировке
На склянку с аттестованным раствором должна быть наклеена этикетка с указанием условного обозначения раствора, массовой концентрации цианидов, погрешности ее установления и даты приготовления.
Г.10 Условия хранения
Аттестованный раствор AP3-CN хранят в холодильнике не более 5 дн., раствор AP4-CN используют в течение рабочего дня.