Государственное санитарно-эпидемиологическое
нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств
протиоконазола по метаболиту
протиоконазол-дестио в зерне, соломе и
зеленой массе риса, корнеплодах и ботве
сахарной свеклы методом капиллярной
газожидкостной хроматографии
Методические
указания
МУК 4.1.3447-17
Москва 2017
1. Разработаны сотрудниками ФГБНУ «Всероссийский НИИ фитопатологии» (Л.В. Дубовая, А.М. Макеев).
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 22 декабря 2016 г. № 2).
3. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А.Ю. Поповой 14 марта 2017 г.
4. Введены впервые.
|
УТВЕРЖДАЮ Руководитель Федеральной службы А.Ю. Попова 14 марта 2017 г. |
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств протиоконазола
по метаболиту протиоконазол-дестио в зерне, соломе и
зеленой массе риса, корнеплодах и ботве сахарной
свеклы методом капиллярной газожидкостной
хроматографии
Методические указания
МУК 4.1.3447-17
Свидетельство о метрологической аттестации № РОСС RU.001.310430/260 23.06.16.
Настоящие методические указания устанавливают порядок применения метода капиллярной газожидкостной хроматографии для определения массовых концентраций протиоконазола по метаболиту протиоконазол-дестио в зерне риса в диапазоне 0,02 - 0,2 мг/кг, в зеленой массе риса, ботве и корнеплодах сахарной свеклы в диапазоне 0,05 - 0,5 мг/кг, в соломе риса в диапазоне 0,1 - 1,0 мг/кг.
Методические указания носят рекомендательный характер.
Протиоконазол
2-[(2RS)-2-(1-хлорциклопропил)-3-(2-хлорфенил)-2-оксипропил]-2Н-1,2,4-триазол-3(4Н)-тион
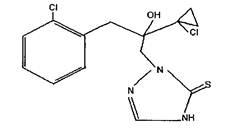
C14H15Cl2N3OS
Молекулярная масса: 344,3.
Бесцветное или светло-бежевое твердое вещество без запаха.
Температура плавления: 139,1 - 144,5 °С. Давление паров при 20 °С: ![]() 4×10-7
Па. Коэффициент распределения н-октанол/вода: KowlogР = 4,16 (pH 4);
3,82 (pH 7) и 2,0 (pH 9). Растворимость (г/дм3) при 20 °С: ацетон
> 250, этилацетат > 250, дихлорметан - 88, ацетонитрил - 69;
растворимость в воде - 0,005 (pH 4); 0,3 (pH 8) и 2,0 (pH 9).
4×10-7
Па. Коэффициент распределения н-октанол/вода: KowlogР = 4,16 (pH 4);
3,82 (pH 7) и 2,0 (pH 9). Растворимость (г/дм3) при 20 °С: ацетон
> 250, этилацетат > 250, дихлорметан - 88, ацетонитрил - 69;
растворимость в воде - 0,005 (pH 4); 0,3 (pH 8) и 2,0 (pH 9).
Вещество стабильно при хранении на воздухе, а также в кислой (DT50 = 120 дней) и щелочной (DT50 ≥ 1 года) средах.
В присутствии света в водных фотолитических условиях протиоконазол достаточно быстро деградирует с периодом полураспада 47,7 ч.
Краткая токсикологическая характеристика. Острая пероральная токсичность (LD50) для крыс > 6200 мг/кг; острая дермальная токсичность (LD50) для крыс > 2000 мг/кг; острая ингаляционная токсичность (LС50) для крыс > 4990 мг/м3 воздуха.
Протиоконазол не оказывает раздражающего действия на кожу и слизистую оболочку глаз, не обладает эмбриотоксическим или тератогенным действием. LС50 для рыб - 1,83 мг/дм3 (96 ч).
Фунгицид нетоксичен для птиц, пчел, дождевых червей, дафний и почвенных микроорганизмов.
Основной метаболит протиоконазола: протиоконазол-дестио (SXX 0665)
α-(1-хлорциклопропил)-α-(2-хлорфенил)метил-1Н-1,2,4-триазол-1-этанол
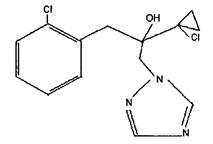
С14Н15Сl2N3O
Молекулярная масса: 312,2.
Бесцветный порошок без запаха. Температура плавления: 108,5 °С. Давление паров при 20 °С: 2,7×10-7 Па. Коэффициент распределения н-октанол/вода: KowlogР = 3,04. Растворимость (г/дм3) при 20 °С: гексан - 3, толуол - 84, ацетон - 100, ацетонитрил - 43, дихлорметан - более 200, вода - 0,051.
Метаболит стабилен в кислой и щелочной средах (DT50 ≥ 500 ч).
Область применения препарата. Протиоконазол - фунгицид системного действия из группы ингибиторов синтеза эргостерина. Вещество обладает защитным, искореняющим и лечебным действием.
Применяется в России в качестве фунгицида системного действия в составе смесевых препаратов для протравливания зерна колосовых культур и обработки вегетирующих растений зерновых злаков и рапса с нормой расхода 37 - 50 г д.в./т семян или 80 - 100 г д.в./га.
Протиоконазол весьма лабильное вещество и при поступлении в растение очень быстро метаболизируется до более устойчивого соединения - протиоконазол-дестио (α-(1-хлорциклопропил)-α-(2-хлорфенил)метил-1Н-1,2,4-триазол-1-этанол). В связи с этим разработан метод, позволяющий осуществлять контроль за содержанием остаточных количеств протиоконазола в зерне, соломе и зеленой массе риса, ботве и корнеплодах свеклы по протиоконазол-дестио.
1. Метрологические характеристики
При соблюдении всех регламентированных условий и проведении анализа в точном соответствии с данной методикой погрешность (и ее составляющие) результатов измерений при доверительной вероятности Р = 0,95 не превышает значений, приведенных в табл. 1 для соответствующих диапазонов концентраций.
Полнота извлечения вещества, стандартное отклонение, доверительный интервал среднего результата для всего диапазона измерений (n = 20) приведены в табл. 2.
Метрологические параметры
|
Анализируемый объект |
Диапазон определяемых концентраций, мг/кг |
Показатель точности (границы относительной погрешности, Р = 0,95), ±δ, % |
Показатель повторяемости (среднеквадратичное отклонение повторяемости), σr, % |
Показатель воспроизводимости (среднеквадратичное отклонение воспроизводимости), σR, % |
Предел повторяемости (значение допустимого расхождения между двумя результатами параллельных определений), r, % |
Предел воспроизводимости (значение допустимого расхождения между двумя результатами измерений, полученных в разных лабораториях), R, % (Р = 0,95) |
|
Зеленая масса риса |
0,05 - 0,5 |
50 |
2,0 |
3,8 |
7,6 |
10,6 |
|
Зерно риса |
0,02 - 0,2 |
50 |
2,2 |
3,1 |
6,2 |
8,7 |
|
Солома риса |
0,1 - 1,0 |
50 |
3,2 |
4,5 |
9,0 |
12,6 |
|
Ботва свеклы |
0,05 - 0,5 |
50 |
2,5 |
3,5 |
7,0 |
9,8 |
|
Корнеплоды свеклы |
0,05 - 0,5 |
50 |
3,0 |
4,2 |
8,4 |
11,8 |
Полнота извлечения вещества, стандартное отклонение, доверительный интервал среднего результата
|
Анализируемый объект |
Метрологические параметры, Р = 0,95, n = 20 |
||||
|
предел обнаружения, мг/кг |
диапазон определяемых концентраций, мг/кг |
средняя полнота извлечения, % |
стандартное отклонение, % |
доверительный интервал среднего результата, % |
|
|
Зеленая масса риса |
0,05 |
0,05 - 0,5 |
86,8 |
3,17 |
±1,65 |
|
Зерно риса |
0,02 |
0,02 - 0,2 |
87,6 |
2,38 |
±1,26 |
|
Солома риса |
0,10 |
0,10 - 1,0 |
85,9 |
3,71 |
±1,96 |
|
Ботва свеклы |
0,05 |
0,05 - 0,5 |
87,9 |
2,62 |
±1,39 |
|
Корнеплоды свеклы |
0,05 |
0,05 - 0,5 |
88,2 |
3,36 |
±1,78 |
2. Метод измерений
Методика основана на определении протиоконазола по метаболиту протиоконазол-дестио с использованием капиллярной газожидкостной хроматографии (ГЖХ) с термоионным детектором (ТИД) после извлечения метаболита из анализируемых матриц водным раствором ацетона, очистки экстракта перераспределением в системе несмешивающихся растворителей и на колонке с оксидом алюминия.
Количественное определение метаболита проводится методом абсолютной калибровки.
3. Средства измерений, вспомогательные устройства, реактивы и материалы
3.1. Средства измерений
|
Газовый хроматограф с термоионным детектором |
|
|
Весы аналитические с пределом взвешивания до 110 г и допустимой погрешностью 0,0001 г |
|
|
Весы лабораторные с пределом взвешивания до 160 г и допустимой погрешностью 0,005 г |
|
|
Колбы мерные вместимостью 2-100-2, 2-500-2, 2-1000-2 |
|
|
Пипетки градуированные 1-1-2-1; 1-1-2-2; 1-2-2-5; 1-2-2-10 |
|
|
Пробирки градуированные с пришлифованной пробкой П-2-5-0,1; П-2-10-0,2 |
|
|
Цилиндры мерные 1 - 25; 1 - 50; 1 - 100; 1 - 250; 1 - 500; 1 - 1000 |
|
|
Микрошприц для ввода образцов для газового хроматографа вместимостью 1 - 10 см3 |
ТУ 64-1-2850 |
Примечание. Допускается использование средств измерения с аналогичными или лучшими характеристиками.
3.2. Реактивы
|
Протиоконазол-дестио, аналитический стандарт с содержанием основного вещества 98,5 % |
|
|
Ацетон, осч |
ТУ 6-09-3513-86 |
|
Вода для лабораторного анализа (деионизованная, бидистиллированная) |
|
|
Гелий газообразный, очищенный (или азот) |
ТУ-0271-135-31323949-05 |
|
н-Гексан, хч |
ТУ 2631-003-05807999-98 |
|
Калий марганцовокислый, хч |
|
|
Калий углекислый, хч |
|
|
Кальций хлористый (хлорид кальция), хч |
ГОСТ 4161-77 |
|
Кислота серная концентрированная, хч |
|
|
Метилен хлористый (дихлорметан), хч |
|
|
Натрий углекислый, хч |
|
|
Натрий сернокислый безводный, хч |
|
|
Натрий хлористый, хч |
|
|
Этиловый эфир уксусной кислоты (этилацетат), хч |
ГОСТ 1138-84 |
Примечание. Допускается использование реактивов с более высокой квалификацией, не требующих дополнительной очистки растворителей.
3.3. Вспомогательные средства измерений, устройства и материалы
|
Аппарат для встряхивания проб |
ТУ 64-1-2851-78 |
|
Ванна ультразвуковая с рабочей частотой 35 кГц |
|
|
Генератор водорода |
|
|
Гомогенизатор с металлическим стаканом вместимостью не менее 500 см3 и скоростью вращения ножа не менее 10000 об./мин |
|
|
Компрессор |
|
|
Воронка Бюхнера |
|
|
Воронки делительные вместимостью 100 и 250 см3 |
|
|
Воронки лабораторные, стеклянные |
|
|
Колба Бунзена вместимостью 250 см3 |
|
|
Колбы круглодонные на шлифе вместимостью 10, 50, 100 см3 |
|
|
Колбы плоскодонные вместимостью 250 см3 |
|
|
Колонка хроматографическая капиллярная кварцевая длиной 30 м, внутренним диаметром 0,32 мм с нанесенной пленкой из смеси: 5 % дифенилполисилоксана и 95 % диметилполисилоксана толщиной 0,5 мкм |
|
|
Колонка хроматографическая стеклянная длиной 25 см и внутренним диаметром 8 - 10 мм |
ТУ 46-22-236-79 |
|
Мельница электрическая лабораторная |
|
|
Оксид алюминия нейтральный для колоночной хроматографии с размером частиц 0,063 - 0,200 мм |
|
|
Ротационный вакуумный испаритель с мембранным насосом, обеспечивающим вакуум до 10 мбар |
|
|
Стаканы химические вместимостью 100 и 250 см3 |
|
|
Стекловата |
|
|
Установка для перегонки растворителей с дефлегматором |
|
|
Фильтры бумажные средней плотности |
ТУ 6-09-1678-86 |
Примечание. Допускается использование вспомогательных средств измерений, устройств и материалов с аналогичными пли лучшими техническими характеристиками.
4. Требования безопасности
4.1. При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007-76, требования электробезопасности при работе с электроустановками по ГОСТ 12.1.019-09, а также требования, изложенные в технической документации на газовый хроматограф.
4.2. Помещение должно соответствовать требованиям пожаробезопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83. Содержание вредных веществ в воздухе не должно превышать норм, установленных ГН 2.2.5.1313-03 и ГН 2.2.5.2308-07. Организация обучения работников безопасности труда - по ГОСТ 12.0.004-90.
5. Требования к квалификации оператора
Измерения в соответствии с настоящей методикой может выполнять специалист, имеющий опыт работы на газовом хроматографе, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений.
6. Условия измерений
При выполнении измерений соблюдают следующие условия:
- процессы приготовления растворов и подготовки проб к анализу проводят при температуре воздуха (20 + 5) °С и относительной влажности не более 80 %;
- выполнение измерений на газовом хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к выполнению измерений
Измерениям предшествуют следующие операции: очистка органических растворителей (при необходимости), приготовление градуировочных растворов, раствора внесения, кондиционирование хроматографической колонки, установление градуировочной характеристики, приготовление смесей растворителей, подготовка колонки с оксидом алюминия, проверка хроматографического поведения протиоконазол-дестио на колонке.
7.1. Очистка органических растворителей и приготовление растворов
7.1.1. Ацетон. Ацетон перегоняют над калием марганцовокислым и прокаленным калием углекислым (на 1 дм3 ацетона 10 г калия марганцевокислого и 2 г калия углекислого). Срок хранения - 1 неделя.
7.1.2. н-Гексан. Растворитель последовательно промывают порциями концентрированной серной кислоты до прекращения окрашивания последней в желтый цвет, затем водой до нейтральной реакции промывных вод, перегоняют над поташом.
7.1.3. Хлористый метилен и этилацетат. Приготовление раствора натрия углекислого с массовой долей 5 %. Навеску (5 ± 0,1) г натрия углекислого растворяют в конической колбе в 40 - 60 см3 деионизованной воды. Полученный раствор количественно переносят в мерную колбу вместимостью 100 см3 и доводят объем раствора до метки деионизованной водой. Срок хранения раствора 1 неделя.
Хлористый метилен и этилацетат промывают последовательно раствором натрия углекислого с массовой долей 5 %, насыщенным раствором хлористого кальция, сушат над безводным карбонатом калия и перегоняют. Растворители хранят в темной посуде при комнатной температуре не более 14 дней.
7.2. Кондиционирование хроматографической колонки
Капиллярную кварцевую колонку устанавливают в термостат хроматографа и, не подсоединяя к детектору, кондиционируют при температуре 290 °С и скорости газа-носителя 2 см3/мин в течение 8 - 10 ч.
7.3. Приготовление градуировочных растворов
7.3.1. Исходный градуировочный раствор протиоконазол-дестио с массовой концентрацией 100 мкг/см3. В мерную колбу вместимостью 100 см3 помещают 0,0102 г протиоконазол-дестио (содержание основного компонента 98,5 %), растворяют в 40 - 50 см3 этилацетата, доводят объем раствора этим же растворителем до метки, тщательно перемешивают. Раствор хранят в морозильной камере при температуре не выше -12 °С не более 3 месяцев.
7.3.2. Градуировочный раствор протиоконазол-дестио с массовой концентрацией 10 мкг/см3 (раствор № 1). В мерную колбу вместимостью 100 см3 помещают 10 см3 исходного раствора протиоконазол-дестио с концентрацией 100 мкг/см3 (п. 7.3.1), разбавляют этилацетатом до метки. Этот раствор используют для приготовления градуировочных растворов № 2 - 5.
Для приготовления проб зерна, зеленой массы, соломы, ботвы и корнеплодов с внесением при оценке полноты извлечения протиоконазол-дестио методом «внесено-найдено» и контроле точности методом добавок используют ацетоновый раствор протиоконазол-дестио с концентрацией 1 мкг/см3.
Градуировочный раствор № 1 и ацетоновый раствор протиоконазол-дестио хранят в морозильной камере при температуре не выше -12 °С не более месяца.
7.3.3. Градуировочные растворы протиоконазол-дестио с массовой концентрацией 0,1 - 1,0 мкг/см3 (растворы № 2 - 5). В 4 мерные колбы вместимостью 100 см3 помещают 1,0; 2,0; 5,0 и 10,0 см3 градуировочного раствора № 1 протиоконазол-дестио с массовой концентрацией 10 мкг/см3 (п. 7.3.2), доводят до метки смесью гексан-этилацетат с объемным соотношением компонентов 8:2, тщательно перемешивают, получают рабочие растворы № 2 - 5 с концентрацией протиоконазол-дестио 0,1; 0.2; 0,5 и 1,0 мкг/см3 соответственно.
Растворы готовят непосредственно перед использованием.
7.4. Установление градуировочной характеристики
Градуировочную характеристику, выражающую зависимость площади пика (мкВ) от концентрации протиоконазол-дестио в растворе (мкг/см3), устанавливают методом абсолютной градуировки по 4 градуировочным растворам.
В инжектор хроматографа вводят по 1 мм3 каждого градуировочного раствора (п. 7.3.3) и анализируют при условиях хроматографирования по п. 9.4. Осуществляют не менее 3 параллельных измерении. Расхождение между параллельными определениями не должно превышать предел повторяемости г.
По полученным данным строят градуировочную характеристику.
7.5. Приготовление смесей гексан-этилацетат для очистки экстрактов на колонке с оксидом алюминия
7.5.1. Смесь гексан-этилацетат (объемное соотношение 85:15). В мерную колбу вместимостью 500 см3 помещают 75 см3 этилацетата, доводят до метки гексаном, перемешивают. Срок хранения раствора - 1 неделя.
7.5.2. Смесь гексан-этилацетат (объемное соотношение 7:3). В мерную колбу вместимостью 500 см3 помешают 150 см3 этилацетата, доводят до метки гексаном, перемешивают. Срок хранения раствора - 1 неделя.
7.6. Подготовка колонки с оксидом алюминия для очистки экстракта
Нижнюю часть стеклянной колонки длиной 25 см и внутренним диаметром 8 - 10 мм уплотняют тампоном из стекловаты, медленно выливают в колонку (при открытом кране) суспензию 5 г оксида алюминия нейтрального III степени активности в 15 см3 гексана (оксид алюминия III степени активности по Брокману получают добавлением 6 % воды к навеске оксида алюминия I степени активности). Дают растворителю стечь до верхнего края сорбента и помещают на него слой безводного сульфата натрия высотой 1 см. Колонку промывают 15 см3 гексана со скоростью 1 - 2 капли в секунду, после чего она готова к работе.
7.7. Проверка хроматографического поведения протиоконазол-дестио на колонке с оксидом алюминия
В круглодонную колбу вместимостью 10 см3 помещают 0,2 см3 градуировочного раствора протиоконазол-дестио с концентрацией 10 мкг/см3 в этилацетате (п. 7.3.2). Растворитель упаривают досуха на роторном испарителе при температуре не выше 40 °С, остаток растворяют в 2 см3 смеси гексан-этилацетат с объемным соотношением компонентов 85:15, помещая в ультразвуковую ванну на 1 мин. Раствор наносят на колонку с оксидом алюминия, подготовленную по п. 7.6. Колбу обмывают 2 см3 смеси гексан-этилацетат (85:15, по объему), которые также наносят на колонку. Промывают колонку 20 см3 смеси гексан-этилацетат (85:15, по объему) со скоростью 1 - 2 капли в секунду, элюат отбрасывают. Затем через колонку пропускают 40 см3 смеси гексан-этилацетат (7:3, по объему), отбирая последовательно по 5 см3 элюата. Каждую фракцию упаривают досуха, остатки растворяют в 1 см3 смеси гексан-этилацетат (8:2, по объему), помещая в ультразвуковую ванну на 1 мин, и анализируют на содержание протиоконазол-дестио по п. 9.4.
По результатам обнаружения протиоконазол-дестио в каждой из фракций определяют объем смеси гексан-этилацетат (7:3, по объему), необходимый для полного вымывания вещества из колонки.
Примечание. Профиль вымывания протиоконазол-дестио может меняться при использовании новых партий сорбента и растворителей.
8. Отбор и хранение проб
Отбор проб производится в соответствии с правилами, определенными ГОСТ Р 50436-92 «Зерновые. Отбор проб зерна», ГОСТ 6293-90 «Рис. Требования при заготовках и поставках», ГОСТ Р 55289-12 «Рис. Технические условия», ГОСТ 52647-06 «Свекла сахарная. Технические условия» и «Унифицированными правилами отбора проб сельскохозяйственной продукции, продуктов питания и объектов окружающей среды для определения микроколичеств пестицидов» (№ 2051-79 от 21.08.79).
Пробы зеленой массы риса, ботвы и корнеплодов сахарной свеклы хранят в стеклянной или полиэтиленовой таре в холодильнике не более одного дня; для длительного хранения пробы замораживают и хранят при температуре не выше -18 °С до анализа. Пробы зерна и соломы высушивают до стандартной влажности и хранят в бумажных или тканевых мешочках в сухом, хорошо проветриваемом шкафу. Перед проведением анализа зерно размалывают, а зеленую массу, ботву, корнеплоды и солому измельчают.
9. Проведение определения
9.1. Экстракция протиоконазол-дестио
Приготовление водного раствора ацетона с объемной долей 80 %
В мерную колбу вместимостью 500 см3 помещают 100 см3 деионизованной воды и доводят объем раствора в колбе до метки ацетоном, перемешивают. Срок хранения раствора - 1 неделя.
9.1.1. Зеленая масса, ботва, корнеплоды. Образец измельченного растительного материала массой 20 г помещают в стакан гомогенизатора вместимостью 500 см3, добавляют 100 см3 водного раствора ацетона с объемной долей 80 % и гомогенизируют 3 минуты при 10000 об./мин. Гомогенат фильтруют под вакуумом на воронке Бюхнера через бумажный фильтр в колбу вместимостью 250 см3. Осадок на фильтре промывают 50 см3 водного раствора ацетона с объемной долей 80 %. Экстракт и промывную жидкость переносят в мерный цилиндр с пришлифованной пробкой вместимостью 250 см3 доводят общий объем раствора до 200 см3 ацетоном, перемешивают. Аликвоту раствора объемом 50 см3, эквивалентную 5 г образца, переносят в круглодонную колбу вместимостью 100 см3. Далее проводят очистку экстракта по п. 9.2.
9.1.2. Зерно, солома. Образец размолотого зерна (10 г) или измельченной соломы (5 г) помешают в плоскодонную колбу вместимостью 250 см3, добавляют 50 см3 водного раствора ацетона с объемной долей 80 % и помещают на аппарат для встряхивания на 40 минут. Суспензию фильтруют под вакуумом на воронке Бюхнера через бумажный фильтр в колбу Бунзена вместимостью 250 см3. Осадок на фильтре возвращают в колбу и повторяют экстракцию дополнительной порцией этого же растворителя объемом 30 см3, выдерживая на встряхивателе 20 мин. Осадок на фильтре промывают 20 см3 водного раствора ацетона с объемной долей 80 %. Экстракты и промывную жидкость переносят в мерный цилиндр с пришлифованной пробкой вместимостью 100 см3, доводят общий объем раствора до 100 см3 ацетоном, перемешивают и аликвоту раствора объемом 50 см3 (эквивалентную 5 г зерна или 2,5 г соломы) переносят в круглодонную колбу вместимостью 100 см3. Далее проводят очистку экстракта по п. 9.2.
9.2. Очистка экстракта перераспределением в системе несмешивающихся растворителей
Приготовление насыщенного раствора хлорида натрия
В коническую колбу вместимостью 200 см3 вносят навеску (50 ± 2) г хлорида натрия, приливают 100 см3 деионизованной воды, перемешивают в течение 5 мин, полученный раствор фильтруют. Фильтрат является насыщенным раствором хлорида натрия. Срок годности раствора - 1 неделя.
Отобранные экстракты растительных образцов, полученные по п. 9.1.1 и 9.1.2 и помещенные в круглодонные колбы, упаривают на ротационном вакуумном испарителе при температуре не выше 40 °С до водного остатка (7 - 10 см3). Водный остаток переносят в делительную воронку вместимостью 100 см3. Колбу ополаскивают 10 см3 деионизованной воды, которую также помещают в делительную воронку. В воронку вносят 15 см3 насыщенного раствора хлорида натрия, затем приливают 30 см3 хлористого метилена, интенсивно встряхивают в течение 2 мин. После разделения фаз нижний органический слой фильтруют через слой безводного сульфата натрия в круглодонную колбу вместимостью 100 см3. Операцию экстракции водной фазы повторяют еще дважды, используя 30 и 20 см3 хлористого метилена. Объединенную органическую фазу, пропущенную через слой сульфата натрия, упаривают досуха на ротационном вакуумном испарителе при температуре не выше 40 °С и остаток подвергают дополнительной очистке на колонке с оксидом алюминия по п. 9.3.
9.3. Очистка экстракта на колонке с оксидом алюминия
Сухой остаток в круглодонной колбе, полученный по п. 9.2, растворяют в 2 см3 смеси гексан-этилацетат в объемном соотношении 85:15, помещая в ультразвуковую ванну на 1 мин. Раствор наносят на колонку, подготовленную по п. 7.6. Колбу обмывают 2 см3 смеси гексан-этилацетат (85:15, по объему), которые также наносят на колонку. Промывают колонку 25 см3 смеси гексан-этилацетат (85:15, по объему) со скоростью 1 - 2 капли в секунду, элюат отбрасывают. Протиоконазол-дестио элюируют с колонки 30 см3 смеси гексан-этилацетат в объемном соотношении 7:3, собирая элюат непосредственно в круглодонную колбу вместимостью 100 см3. Раствор упаривают досуха на ротационном вакуумном испарителе при температуре не выше 40 °С. Остаток экстракта зерна растворяют в 1 см3, зеленой массы, ботвы, корнеплодов и соломы - в 2,5 см3 смеси гексан-этилацетат с объемным соотношением компонентов 8:2, помещая в ультразвуковую ванну на 1 мин, и растворы анализируют на содержание протиоконазол-дестио по п. 9.4.
9.4. Условия хроматографирования
Газовый хроматограф с термоионным детектором, снабженный приспособлениями для капиллярной колонки.
Хроматографическая кварцевая капиллярная колонка длиной 30 м, внутренним диаметром 0,32 мм с нанесенной пленкой из смеси: 5 % дифеннлполисилоксана и 95 % диметилполисилоксана толщиной 0,5 мкм.
|
Температура: |
детектора - 295 °С; |
|
|
испарителя -275 °С. |
Температура термостата колонки программированная. Начальная температура - 175 °С, выдержка 2 мин; нагрев колонки со скоростью 25 градусов в минуту до температуры 260 °С, выдержка - 0 мин: нагрев колонки со скоростью 5 градусов в минуту до температуры 270 °С, выдержка 3 мин; нагрев со скоростью 10 градусов в минуту до температуры 280 °С, выдержка - 10 мин.
|
Расход газов: |
газа-носителя (гелий) - 2,0 см3/мин; |
|
|
водорода - 4,6 см3/мин; |
|
|
воздуха - 175 см3/мин; |
|
|
поток поддува - 28 см3/мин. |
Объем вводимой пробы: 1 мм3.
Линейный диапазон детектирования: 0,10 - 1,0 нг.
Образцы, дающие пики большие чем градуировочный раствор с концентрацией 1,0 мкг/см3, разбавляют смесью гексан-этилацетат в объемном соотношении 8:2.
10. Обработка результатов анализа
Содержание протиоконазол-дестио в пробе (X, мг/кг) рассчитывают методом абсолютной калибровки по формуле:
![]()
С - концентрация протиоконазол-дестио, найденная по градуировочной характеристике в соответствии с величиной площади хроматографического пика, мкг/см3;
V - объем экстракта, подготовленного для хроматографирования, см3;
m - масса анализируемой части
образца, соответствующая доле экстракта, использованной для очистки на колонке
с оксидом алюминия и последующего хроматографического определения, г.![]()
При расчете содержания протиоконазол-дестио в эквивалентах протиоконазола полученное значение X умножают на 1,1.
11. Проверка приемлемости результатов параллельных определений
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предела повторяемости:
|
|
(1) |
X1, Х2 - результаты параллельных определений, мг/кг;
r - значение предела повторяемости (табл. 1), при этом r = 2,8σr. При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
12. Оформление результатов
Результат анализа представляют в виде:
(![]() ± ∆), мг/кг при вероятности Р
= 0,95, где
± ∆), мг/кг при вероятности Р
= 0,95, где
![]() - среднее арифметическое результатов
определений, признанных приемлемыми, мг/кг;
- среднее арифметическое результатов
определений, признанных приемлемыми, мг/кг;
∆ - граница абсолютной погрешности, мг/кг:
![]()
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций, табл. 1), %.
В случае если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
«содержание протиоконазол-дестио в пробах зерна риса менее 0,02 мг/кг»*;
«содержание протиоконазол-дестио в пробах зеленой массы риса, ботвы и корнеплодов сахарной свеклы менее 0,05 мг/кг»**;
«содержание протиоконазол-дестию в пробах соломы риса менее 0,1 мг/кг»***
* 0,02 мг/кг - предел обнаружения;
** 0,05 мг/кг - предел обнаружения;
*** 0,1 мг/кг - предел обнаружения.
13. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-02 «Точность (правильность и прецизионность) методов и результатов измерений».
13.1. Контроль стабильности градуировочной характеристики проводят в начале и по окончании каждой серии опытов.
При контроле стабильности градуировочной характеристики проводят измерения не менее двух образцов концентраций для градуировки, содержание протиоконазол-дестио в которых должно охватывать весь диапазон от 0,1 до 1,0 мкг/см3.
Градуировочная характеристика считается стабильной, если для каждого градуировочного раствора, используемого для контроля, сохраняется соотношение:
|
|
(2) |
X - содержание протиоконазол-дестио в пробе при контрольном измерении, мкг;
С - известное содержание протиоконазол-дестио в градуировочном растворе, взятом для контроля стабильности градуировочной характеристики, мкг;
В - норматив контроля погрешности градуировочной характеристики, % (равен 10 % при Р = 0,95).
Если величина расхождения (А) превышает 10 %, делают вывод о невозможности применения градуировочной характеристики для дальнейших измерений. В этом случае выясняют и устраняют причины нестабильности градуировочной характеристики и повторяют контроль ее стабильности с использованием других градуировочных растворов протиоконазол-дестио. предусмотренных МВИ. При повторном обнаружении нестабильности градуировочной характеристики устанавливают ее заново согласно п. 7.4.
Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
13.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки Сд должна удовлетворять условию:
![]()
![]() - характеристика погрешности
(абсолютная погрешность) результатов анализа, соответствующая содержанию
компонента в испытуемом образце (расчетному значению содержания компонента в
образце с добавкой соответственно), мг/кг.
- характеристика погрешности
(абсолютная погрешность) результатов анализа, соответствующая содержанию
компонента в испытуемом образце (расчетному значению содержания компонента в
образце с добавкой соответственно), мг/кг.
Допустимо характеристику погрешности результатов анализа при внедрении методики в лаборатории устанавливать на основе выражения ∆л = ±0,84∆ с последующим уточнением по мере накопления информации:
∆л = ±0,84∆, где
∆ - граница абсолютной погрешности, мг/кг.
![]()
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций, табл. 1), %.
Контроль проводят путем сравнения результата контрольной процедуры Кк с нормативом контроля К.
Результат контрольной процедуры Кк рассчитывают по формуле:
![]()
![]() Сд - среднее
арифметическое результатов параллельных определений (признанных приемлемыми по
п. 11) содержания
компонента в образце с добавкой, испытуемом образце, концентрация добавки
соответственно, мг/кг.
Сд - среднее
арифметическое результатов параллельных определений (признанных приемлемыми по
п. 11) содержания
компонента в образце с добавкой, испытуемом образце, концентрация добавки
соответственно, мг/кг.
Норматив контроля К рассчитывают по формуле:
![]()
Проводят сопоставление результата контрольной процедуры (Кк) с нормативом контроля (К).
Если результат контроля процедуры удовлетворяет условию
|
|Кк| ≤ К |
(3) |
процедуру анализа признают удовлетворительной.
При невыполнении условия (3) процедуру контроля повторяют. При повторном невыполнении условия (3) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
13.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости.
Расхождение между результатами измерений, выполненных в условиях воспроизводимости (разное время, разные операторы, разные лаборатории), не должно превышать предела воспроизводимости (R):
|
|
(4) |
X1, Х2 - результаты измерений, выполненных в условиях воспроизводимости (разное время, разные операторы, разные лаборатории), мг/кг;
R - предел воспроизводимости (в соответствии с диапазоном концентраций, табл. 1), %.
СОДЕРЖАНИЕ