ГОСТ Р 55748-2013
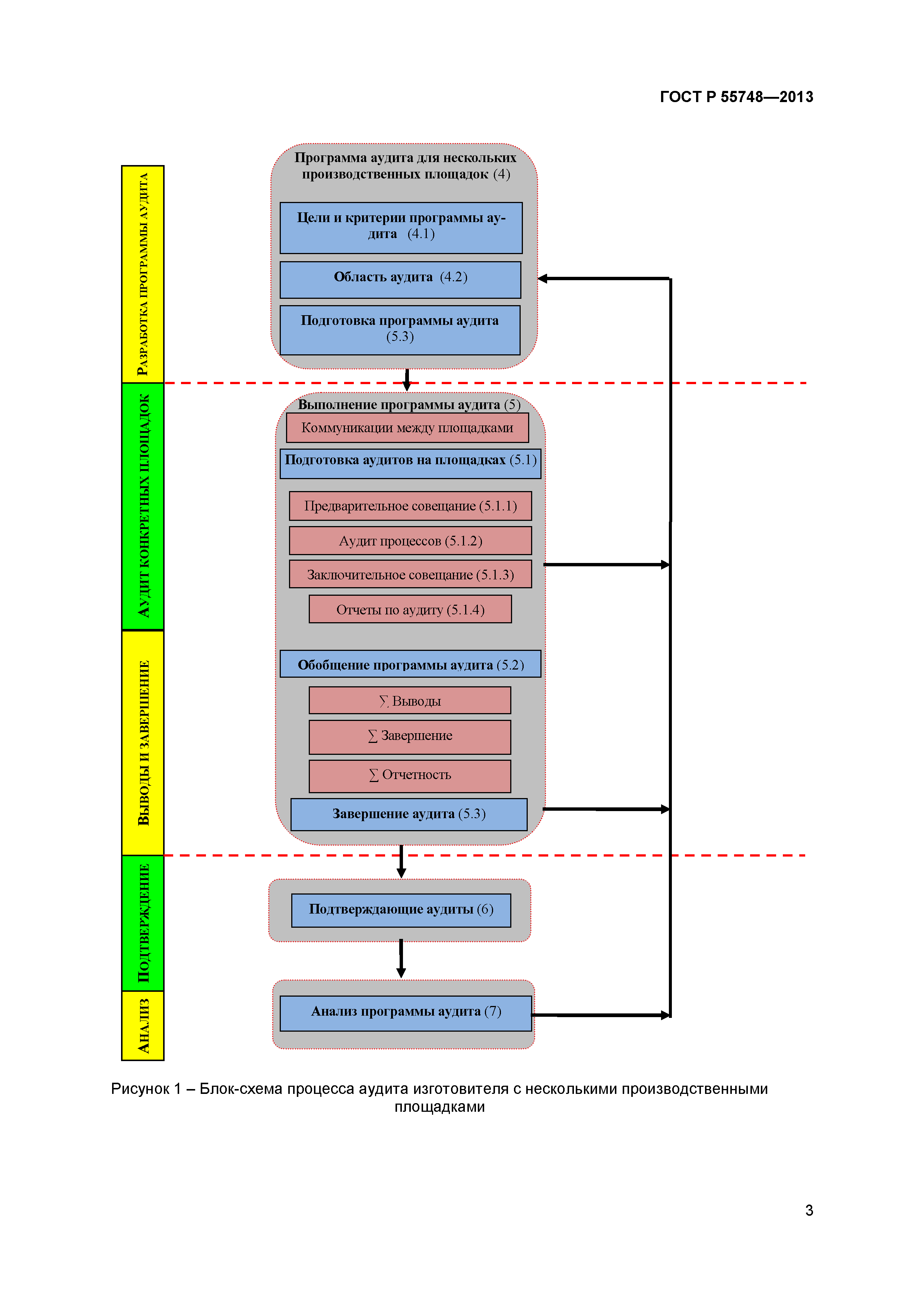
Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 4. Аудит нескольких производственных площадок
| Обозначение: | ГОСТ Р 55748-2013 |
| Обозначение англ: | GOST R 55748-2013 |
| Статус: | Введен впервые |
| Название рус.: | Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 4. Аудит нескольких производственных площадок |
| Название англ.: | Guidelines for regulatory auditing of quality management systems of medical device manufacturers. Part 4. Multiple site auditing |
| Дата добавления в базу: | 21.05.2015 |
| Дата актуализации: | 01.01.2021 |
| Дата введения: | 01.01.2015 |
| Область применения: | Стандарт является руководством для аудиторских организаций для планирования, организации, проведения, документирования, а также анализа программ аудита при проведении аудитов изготовителей медицинских изделий с несколькими производственными площадками, действующими в рамках той же системы менеджмента качества. Стандарт не распространяется на изготовителей, включающих в себя несколько предприятий, соответствующих различным системам менеджмента качества. Отношения между этими предприятиями необходимо рассматривать как отношения между поставщиками. Однако, если изготовитель имеет несколько предприятий с несколькими производственными площадками, действующими в рамках одной системы менеджмента качества, то настоящий стандарт может быть применен. |
| Оглавление: | 1 Область применения 2 Нормативные ссылки 3 Термины и определения 4 Программа аудита для изготовителей с несколькими производственными площадками 5 Выполнение программы аудита 6 Подтверждающие аудиты 7 Анализ программы аудита Приложение А (обязательное) Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям Приложение ДА (обязательное) Сравнение структуры настоящего стандарта со структурой документа GHTF/SG4/N83:2010 «Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 4. Аудит нескольких производственных площадок» Приложение ДБ (обязательное) Текст измененных структурных элементов настоящего стандарта и документа GHTF/SG4/N83:2010 «Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 4. Аудит нескольких производственных площадок» Приложение ДВ (справочное) Сведения о соответствии ссылочных национальных стандартов Российской Федерации международным стандартам, использованным в качестве ссылочных в примененном международном документе |
| Разработан: | ЗАО МЕДИ-ТЕСТ |
| Утверждён: | 08.11.2013 Федеральное агентство по техническому регулированию и метрологии (1494-ст) |
| Издан: | Стандартинформ (2014 г. ) |
| Расположен в: | |
| Нормативные ссылки: |
|












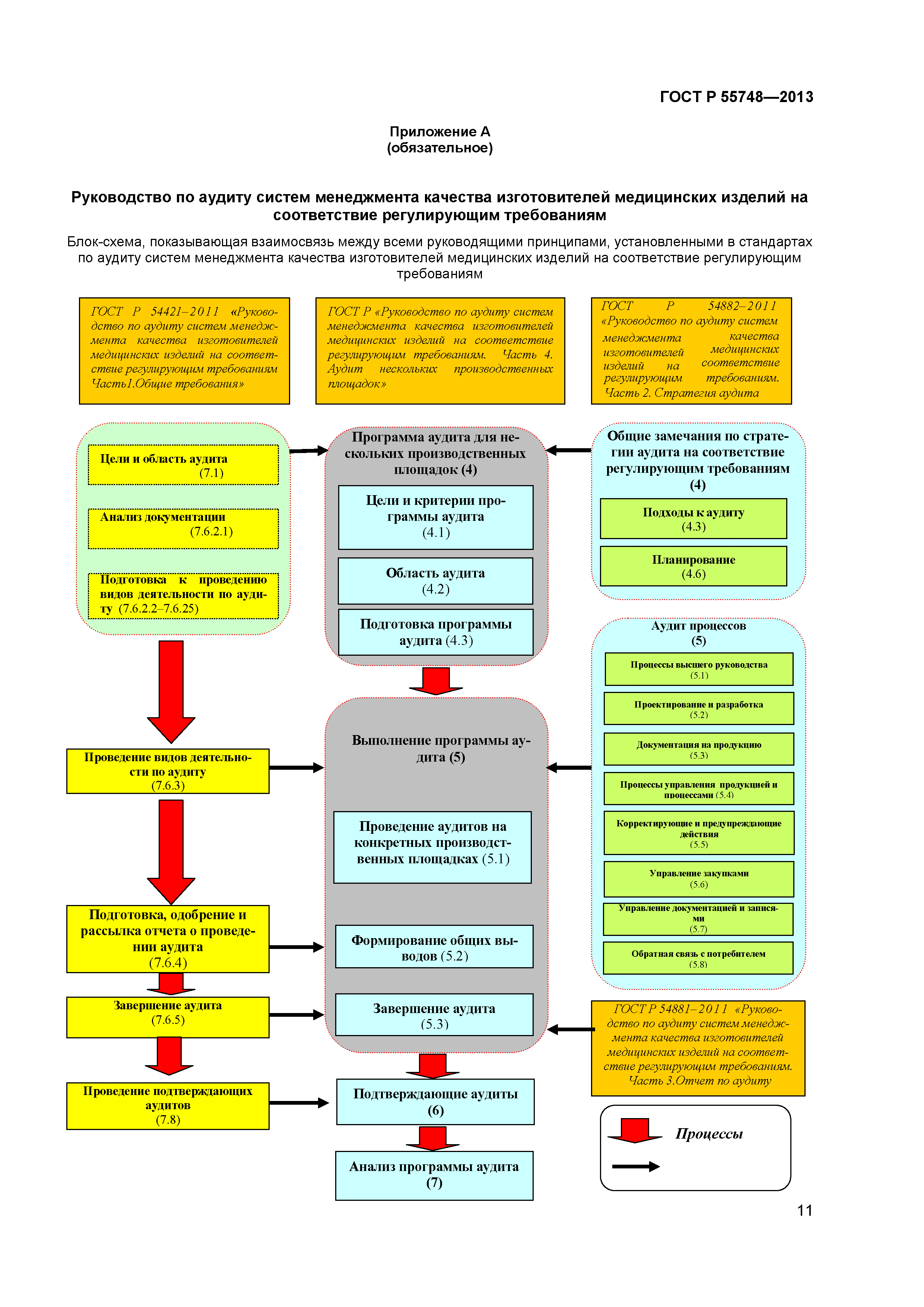






 ГОСТ Р 54881-2011 «Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 3. Отчет о проведении аудита»
ГОСТ Р 54881-2011 «Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 3. Отчет о проведении аудита»